Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Презентация на тему Оксиды углерода (2 и 4) в формате powerpoint.ppt
Содержание
- 1. Презентация на тему Оксиды углерода (2 и 4) в формате powerpoint.ppt
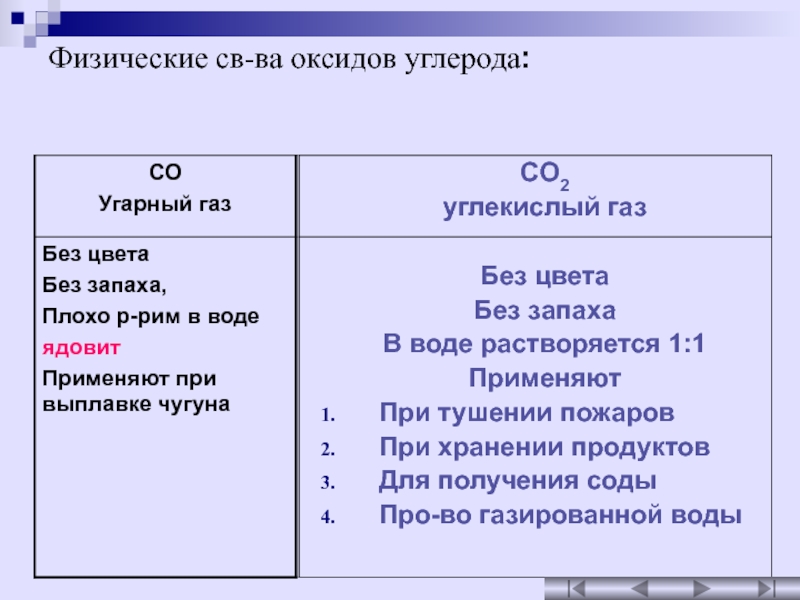
- 2. Физические св-ва оксидов углерода:CO2 углекислый газБез цветаБез
- 3. Классификация оксидов углеродаСублимация (возгонка) – переход из твердого состояния в газообразное минуя жидкое
- 4. Химические свойства углекислого газа:1. кислотный оксид, тяжелее
- 5. Получение CO2 1. В лаборатории:CaCO3 + 2HCl
- 6. Скачать презентанцию
Физические св-ва оксидов углерода:CO2 углекислый газБез цветаБез запахаВ воде растворяется 1:1ПрименяютПри тушении пожаровПри хранении продуктовДля получения содыПро-во газированной воды
Слайды и текст этой презентации
Слайд 2Физические св-ва оксидов углерода:
CO2
углекислый газ
Без цвета
Без запаха
В воде растворяется
1:1
Слайд 3Классификация оксидов углерода
Сублимация (возгонка) – переход из твердого состояния в
газообразное минуя жидкое
Слайд 4Химические свойства углекислого газа:
1. кислотный оксид, тяжелее воздуха, не поддерживает
горение и не горит, кроме Mg:
CO2 + Mg =
MgCO3 + C.Качественная р-ция на CO2
Ca(OH)2 + CO2 = CaCO3 + H2O
CO2 + H2O = H2CO3 – слабая угольная кислота
CO2