Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
ПРИОНЫ
Содержание
- 1. ПРИОНЫ
- 2. План:Почему их так назвали?Чем опасны?Чем они занимаются?Они непобедимы?Список литературы
- 3. РасшифровкаProtein «белок» + infection«инфекция» Стенли Прузинер
- 4. Сейчас наукой принято следующее:1.Возбудитель прионных болезней — это
- 5. Продолжение:2. Приобретение ифекционных свойств белком связано с
- 6. Продолжение3.PrPc содержит больше альфа-спиралей (42 %)и меньше
- 7. Какие болезни вызываютприоны?
- 8. Слайд 8
- 9. Слайд 9
- 10. Как происходит переход на «темную сторону» нормального
- 11. Слайд 11
- 12. Слайд 12
- 13. Слайд 13
- 14. Иммобилизованные мономеры PrP инкубировали в течение ночи
- 15. Слайд 15
- 16. Если биотинилированный PrP превращается в
- 17. Наши данные показали,
- 18. Эти результаты показывают, что мономерное
- 19. Слайд 19
- 20. Итоги эксперимента:N-концевой участок в присутствии ионов меди
- 21. В чем заключается биологическая функция приона?
- 22. Слайд 22
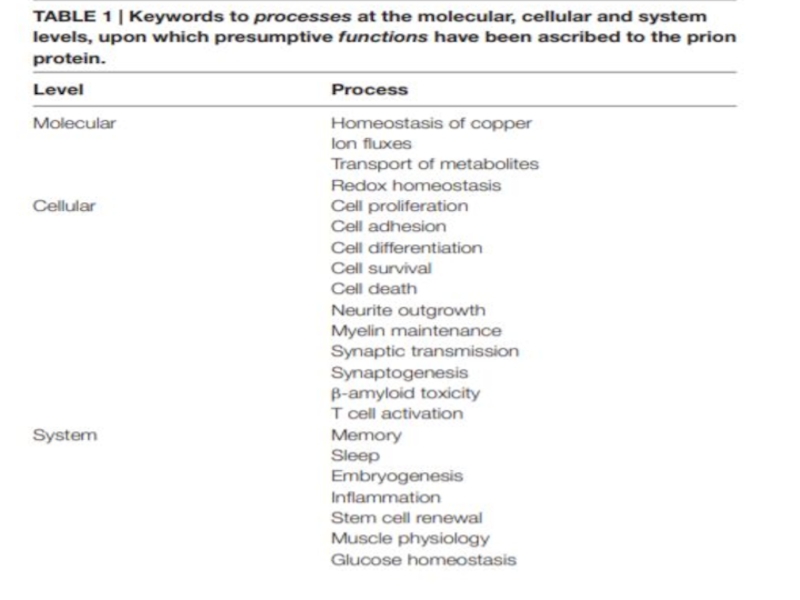
- 23. Экспериментальные исследования показывают, что PrPC
- 24. Что если он не играет никакой роли
- 25. Неясность в научном сообществе Передает амилоидный сигнал
- 26. Поиск Протеина Х
- 27. Функионально похож на каркасный белок
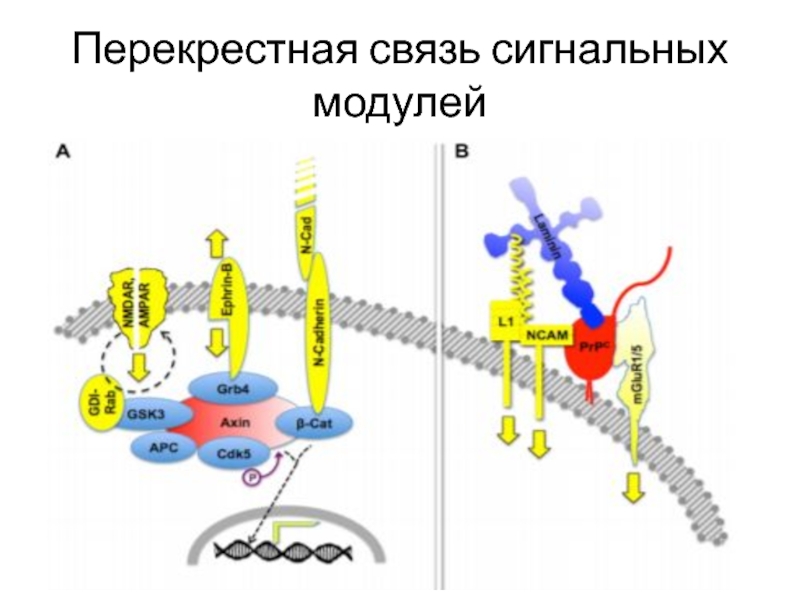
- 28. Перекрестная связь сигнальных модулей
- 29. Аллостерические свойства сигнальных модулей
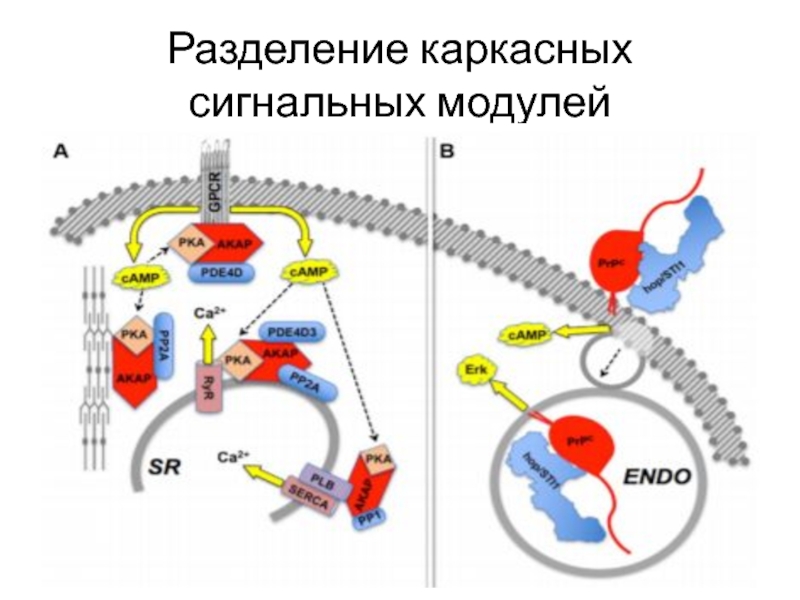
- 30. Разделение каркасных сигнальных модулей
- 31. Посттрансляционное регулирование каркасных белков
- 32. Прионные заболевания на данный момент неизлечимы.
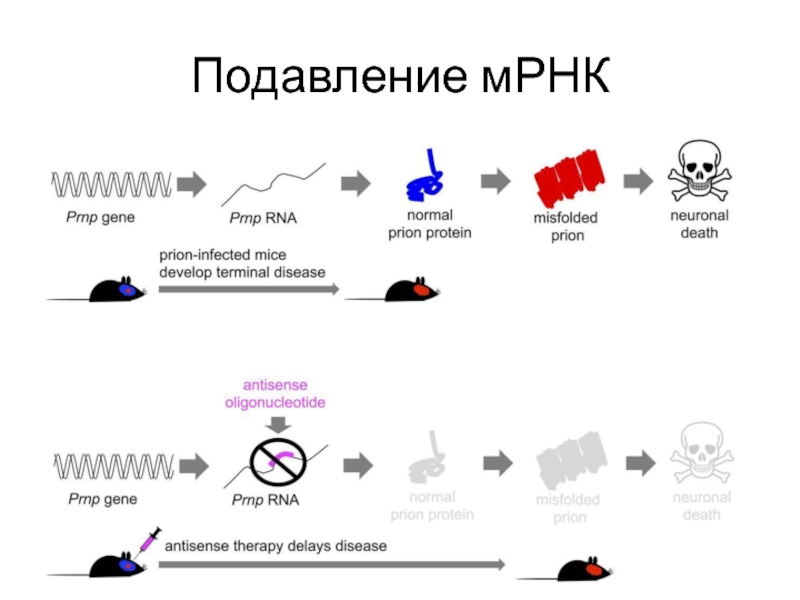
- 33. Подавление мРНК
- 34. Прионы будут побеждены!
- 35. Список литературы:https://www.ncbi.nlm.nih.gov/pubmed/28373833#https://advances.sciencemag.org/content/advances/2/7/e1600014.full.pdfhttps://insight.jci.org/articles/view/131175#sdAguzzi, A., Baumann, F., and Bremer,
- 36. Скачать презентанцию
План:Почему их так назвали?Чем опасны?Чем они занимаются?Они непобедимы?Список литературы
Слайды и текст этой презентации
Слайд 4Сейчас наукой принято следующее:
1.Возбудитель прионных болезней — это мутантная (инфекционная) форма
Слайд 5Продолжение:
2. Приобретение ифекционных свойств белком связано с конформационным переходом (PrPc
PrPSc)
А. Спонтанно спорадическая форма
Б.
Поступлением инфекционного белка ИЗВНЕ приобретенная форма В. Из-за мутаций в гене, кодирующего этот белок наследственная форма
Слайд 6Продолжение
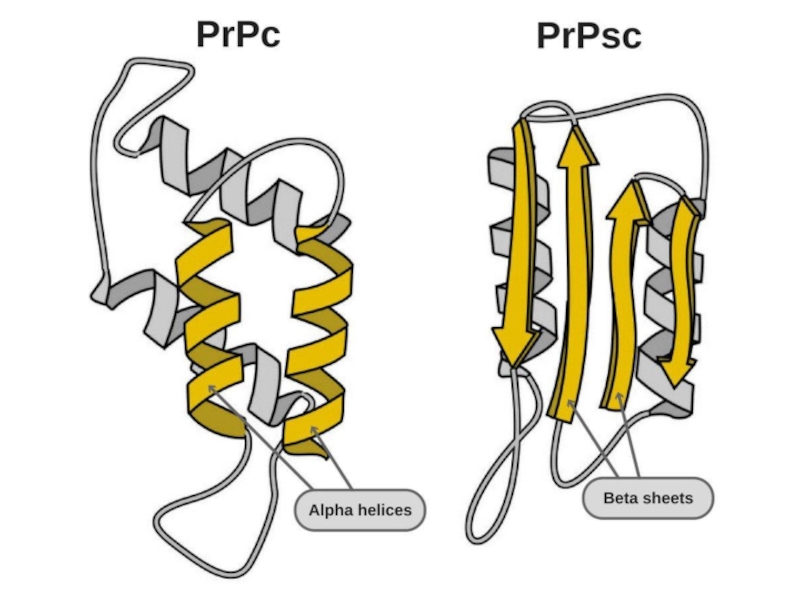
3.PrPc содержит больше альфа-спиралей (42 %)и меньше бета-структур (3%), тогда
как у его инфекционной формы все наоборот (30% - альфа,
43%- бета).4. Инфекционная форма белка устойчива к излучению, а также к различным ферментам, разрушающих обычную форму.
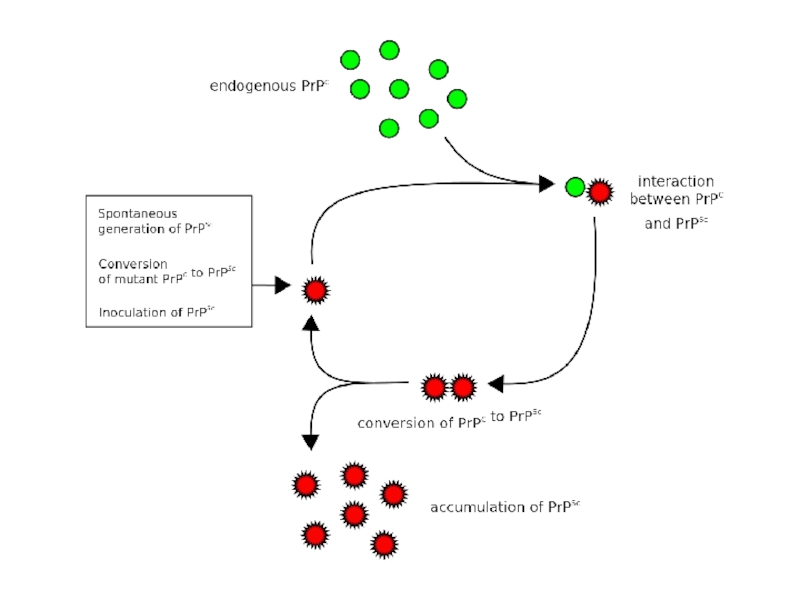
Слайд 10Как происходит переход на «темную сторону» нормального белка?
Как этот
белок потом распространяется в организме?
The dark side of the prion
Слайд 14Иммобилизованные мономеры PrP инкубировали в течение ночи либо в присутствии,
либо в отсутствии 1 мм Ионов Ni2+, Mn2+ или Cu2+;
константы диссоциации указывали на то, что PrP будет насыщен двухвалентными ионами в этих экспериментальных условиях. Затем образцы обрабатывали ПК в течение различных периодов времени (от 0 до 13 часов) и затем маркировали флуоресцентным стрептавидином.
ЭКСПЕРИМЕНТ
Слайд 16 Если биотинилированный PrP превращается в конформацию PrPres, он
не переваривается PK и поэтому может связываться с флуоресцентным стрептавидином
(рис. 2С). С другой стороны, биотинилированный PrPse легко расщепляется PK, что приводит к снижению связывания флуоресцентного стрептавидина (рис. 2, А и Б). В качестве положительного контроля мы ковалентно иммобилизовали PK-резистентную, флуоресцентно меченую, двухцепочечную ДНК на идентичные ПЭГ-функционализированные субстратыСлайд 17 Наши данные показали, что только полноразмерный
PrP [PrP(23-231)], инкубированный в Cu2+, превращается в стабильную
конформацию PrPres.Даже после 10-часового воздействия ПК интенсивность флуоресценции PrP (23-231) оставалась неизменной (рис. 2Д). Аналогично, интенсивность флуоресценции от положительного контроля оставалась неизменной после 10 часов инкубации ПК.
С другой стороны, сопротивление PK было значительно снижено для PrP (23-231), связанного с Mn2+ или Ni2+, и для PrP (23-231) в отсутствие двухвалентных ионов; интенсивность флуоресценции уменьшилась между 60 и90% после 10 часов инкубации ПК.
Аналогично, глобулярный PrP, у которого отсутствовала неструктурированная N-концевая область [PrP(90-231)], был чувствителен к расщеплению PK как в отсутствие, так и в присутствии Cu2+, Mn2+ и Ni2+; после 10-часового расщепления PK интенсивность флуоресценции уменьшалась между 60 и 100% В отличие от этого, сигнал флуоресценции от отрицательного контроля был полностью устранен через 10 часов переваривания ПК (рис. 2, D и E). Данные на фиг. 2E были получены из общей суммы(суммированной по всем временным точкам) 9634, 12 438, 10 680 и 8869 молекул PrP (90-231) в отсутствие и в присутствии Cu2+, Mn2+ и Ni2+, соответственно.
Слайд 18 Эти результаты показывают, что мономерное образование PrPres требует
как внутренне неупорядоченной N-концевой области, так и ионов Cu2+; устранение
любого из них приводит преимущественно к конформации PrPsen.Слайд 20Итоги эксперимента:
N-концевой участок в присутствии ионов меди приводит к образованию
резистентоного прионного белка
Резистентные прионные белки, содержащие N-концевой
участок в присутствии
ионов меди способны к агрегацииСлайд 23 Экспериментальные исследования показывают, что PrPC может связывать олигомеры
β-пептида и опосредовать трансдукцию сигнала, индуцированную последним
Слайд 24Что если он не играет никакой роли вообще?
Мыши,
у которых отсутствовал ген, кодирующий PrPc, были здоровы.
PrPC не имеет
никакой функцииего сохраненная аминокислотная
последовательность была естественным
образом выбрана как следствие смертельных
эффектов мутаций
Слайд 25Неясность в научном сообществе
Передает амилоидный сигнал или все-таки
нет?
Участвует
в продукции стволовых клеток или стимулирует их дифференцировку?
Нейропротектор или
стимулятор апоптоза?Слайд 32Прионные заболевания на данный момент неизлечимы.
Однако уже на
сегодняшний день разработана Антисмысловая терапия, замедляющая на генном уровне рост
прионного белка и тем самым достоверно повышает продолжительность жизни.Слайд 35Список литературы:
https://www.ncbi.nlm.nih.gov/pubmed/28373833#
https://advances.sciencemag.org/content/advances/2/7/e1600014.full.pdf
https://insight.jci.org/articles/view/131175#sd
Aguzzi, A., Baumann, F., and Bremer, J. (2008). The
prion’s elusive reason for being. Annu. Rev. Neurosci. 31, 439–477.
doi: 10.1146/annurev.neuro.31. 060407.125620Alfaidy, N., Chauvet, S., Donadio-Andrei, S., Salomon, A., Saoudi, Y., Richaud, P., et al. (2013). Prion protein expression and functional importance in developmental angiogenesis: role in oxidative stress and copper homeostasis.
Antioxid. Redox Signal. 18, 400–411. doi: 10.1089/ars.2012.4637
Покровский В.И., Киселёв О.И., Черкасский Б.Л., «Прионы и прионные болезни». М.: Изд-во РАМН, 2004, 381 с. (есть в читальном зале РГБ)













![ПРИОНЫ Наши данные показали, что только полноразмерный PrP [PrP(23-231)], Наши данные показали, что только полноразмерный PrP [PrP(23-231)], инкубированный в Cu2+,](/img/thumbs/10a5c72c66be0b7f50e13134da1f4391-800x.jpg)