Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Раздел 2 Молекулярная физика
Содержание
- 1. Раздел 2 Молекулярная физика
- 2. Тема 5 Молекулярная физика
- 3. П 17. Основные положения молекулярно-кинетической (МКТ) теории. Масса и размеры молекул.
- 4. Молекулярно-кинетическая теорияМКТ объясняет свойства макроскопических тел и
- 5. Основные положения мктВещество состоит из частицЧастицы непрерывно и хаотически движутсяЧастицы взаимодействуют друг с другом
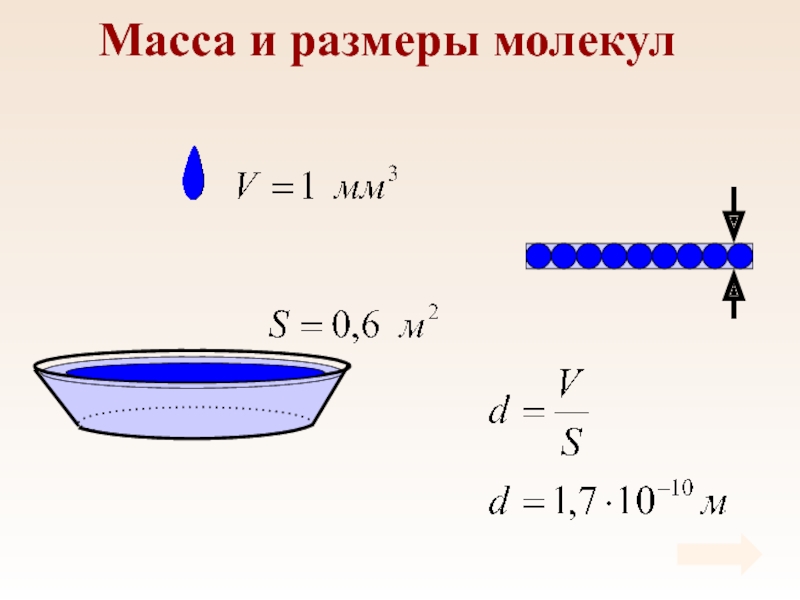
- 6. Масса и размеры молекул
- 7. Масса и размеры молекулМассы молекул в макроскопических масштабах чрезвычайно малы.
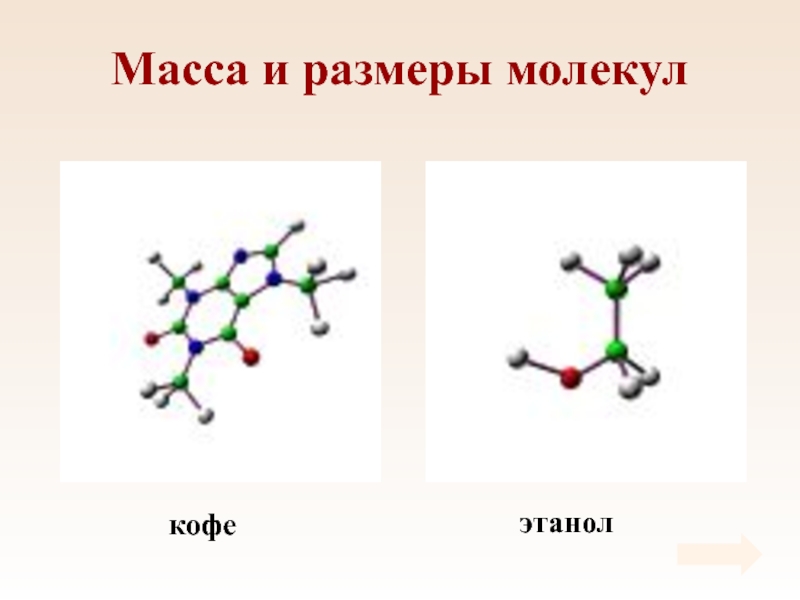
- 8. кофеэтанолМасса и размеры молекул
- 9. Масса и размеры молекулОтносительной молекулярной (или атомной)
- 10. Количество веществаКоличество вещества наиболее естественно было бы
- 11. Количество веществаВ 1 моле любого вещества содержится
- 12. Количество веществаМолярной массой вещества называют массу вещества,
- 13. Количество веществаm – масса вещества
- 14. Броуновское движение1827 г. Роберт Броун
- 15. Броуновское движениеПричина броуновского движения состоит в том,
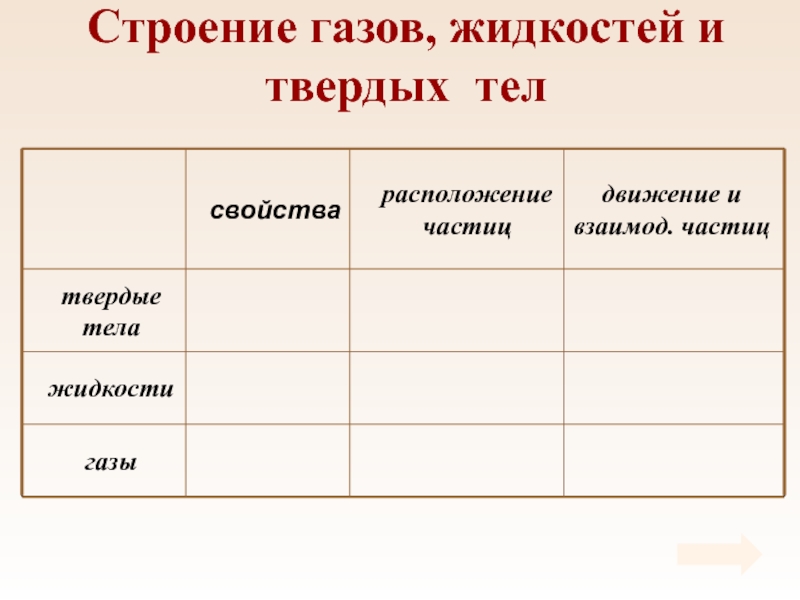
- 16. ТаблицаСвойства газов, жидкостей и твердых тел
- 17. Строение газов, жидкостей и твердых тел
- 18. СвойстваТвердые тела сохраняют объем и форму.
- 19. СвойстваЖидкости сохраняют объем и принимают форму сосуда.Обладают текучестью.
- 20. СвойстваГазы не имеют формы, занимают весь предоставленный объем.
- 21. Расположение частицЧастицы расположены в строгом порядке вплотную друг к другу.Кристаллическая решетка.
- 22. Расположение частицЧастицы расположены вплотную друг к другу, образуют только ближний порядок.
- 23. Расположение частицЧастицы расположены на значительных расстояниях (расстояния между частицами во много раз больше размеров самих частиц).
- 24. Движение и взаимодействие частицЧастицы совершают колебательные движения около положения равновесияСилы притяжения и отталкивания значительны
- 25. Движение и взаимодействие частицЧастицы совершают колебательные движения
- 26. Движение и взаимодействие частицЧастицы свободно перемещаются по
- 27. П. 18. Модель идеального газа. Основное уравнение МКТ идеального газа.
- 28. Идеальный газИдеальный газ – это газ, в
- 29. Среднее значение квадрата скорости молекулСкорость – величина
- 30. Среднее значение квадрата скорости молекул
- 31. Основное уравнение мктОсновное уравнение мкт устанавливает зависимость
- 32. Основное уравнение мкт
- 33. Основное уравнение мкт
- 34. П. 19. Тепловое движение. Уравнение состояния идеального газа.
- 35. Температура и тепловое равновесиеМакроскопические параметры (макропараметры) –
- 36. Температура и тепловое равновесиеЛюбое макроскопическое тело или
- 37. Температура и тепловое равновесиеТермометр – прибор для
- 38. Температура и тепловое равновесиеОсновная деталь термометра –
- 39. Температура и тепловое равновесиеИзобретателем термометра является Галилео
- 40. Температурные шкалышкалаЦельсияшкала Фаренгейташкала РеомюрашкалаКельвина
- 41. Определение температурыПри тепловом равновесии средняя кинетическая энергия поступательного движения молекул всех газов одинакова.
- 42. Определение температуры
- 43. Определение температуры
- 44. Температура – мера средней кинетической энергии молекул
- 45. Зависимость давления газа от температуры и концентрации молекул газа
- 46. Скорости молекул
- 47. Уравнение состояния идеального газа (ур-е Менделеева – Клапейрона)- универсальная газовая постоянная
- 48. Уравнение состояния идеального газа (ур-е Менделеева – Клапейрона)Если в ходе процесса масса газа остается неизменной, то
- 49. П. 20. Изопроцессы и их графики.
- 50. ИзопроцессыИзотермический процессИзобарный процессИзохорный процесс
- 51. Изотермический процессПроцесс, происходящий с газом неизменной массы
- 52. Изобарный процессПроцесс, происходящий с газом неизменной массы
- 53. Изохорный процессПроцесс, происходящий с газом неизменной массы
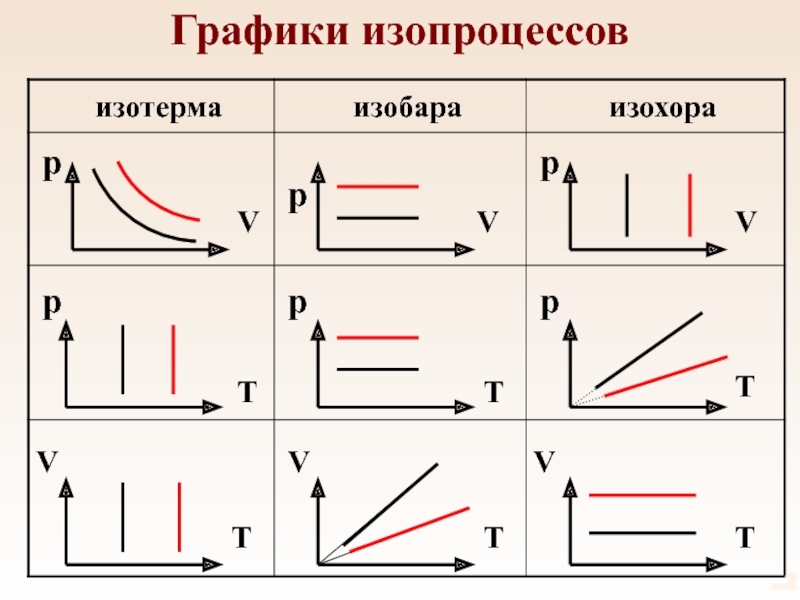
- 54. Графики изопроцессовppppppVVVVVVTTTTTT
- 55. Тема 6. Термодинамика.П. 21 Агрегатные состояния вещества и их фазовые переходы. Аморфные тела.
- 56. Насыщенный парНенасыщенный парНасыщенный парПеренасыщенный пар
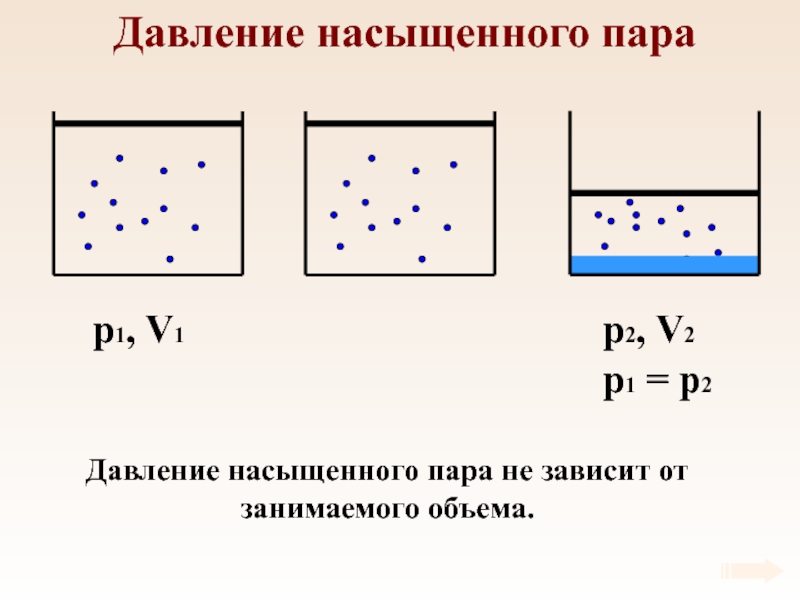
- 57. Давление насыщенного параp1, V1Давление насыщенного пара не зависит от занимаемого объема.
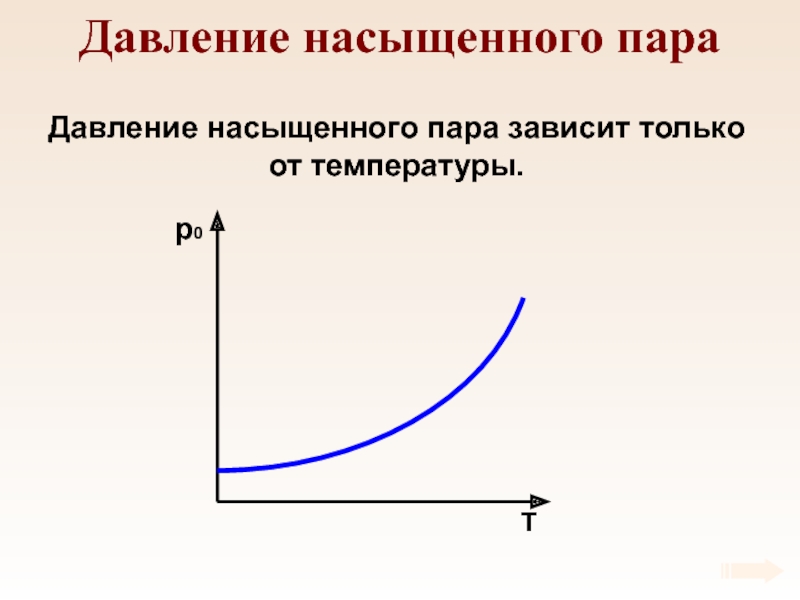
- 58. Давление насыщенного параДавление насыщенного пара зависит только от температуры.
- 59. Давление насыщенного параpTTрТочка росы – это температура при, при которой ненасыщенный пар становится насыщенным .
- 60. Испарение и кипениеПроцесс парообразования с поверхности жидкости.Процесс
- 61. КипениеКипение начинается при температуре, при которой давление
- 62. ВлажностьабсолютнаяотносительнаяПлотность водяных паров в воздухе.Отношение парциального давления
- 63. Измерение влажностиПриборы для измерения влажности:ПсихрометрГигрометр
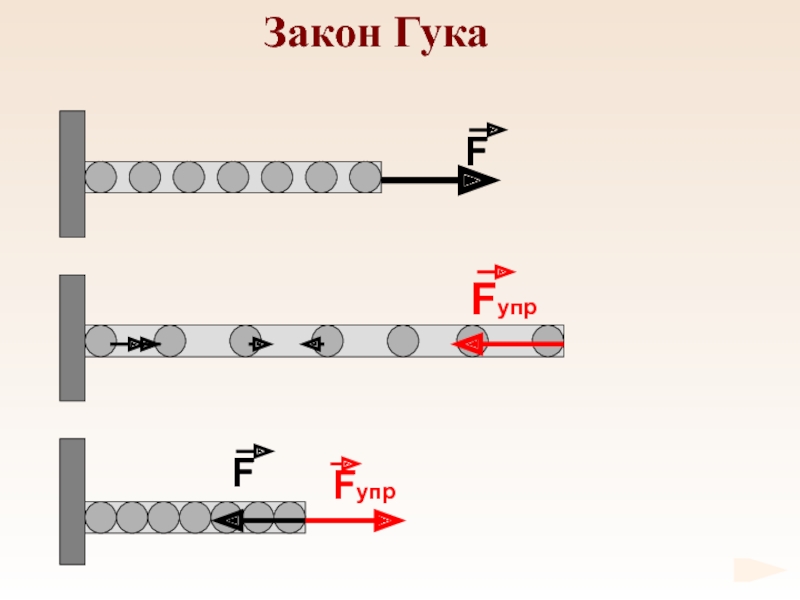
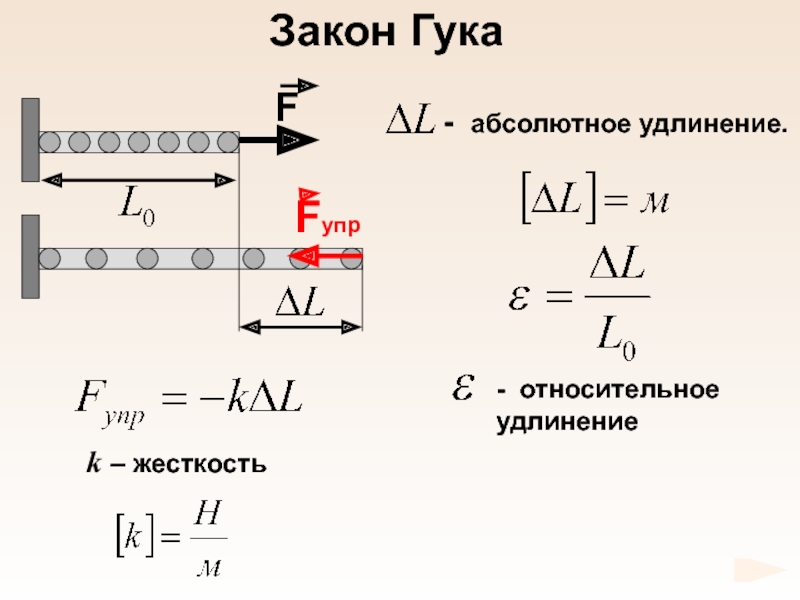
- 64. Закон Гука
- 65. k – жесткостьЗакон Гука
- 66. Е – модуль Юнга1660 г.Закон Гука
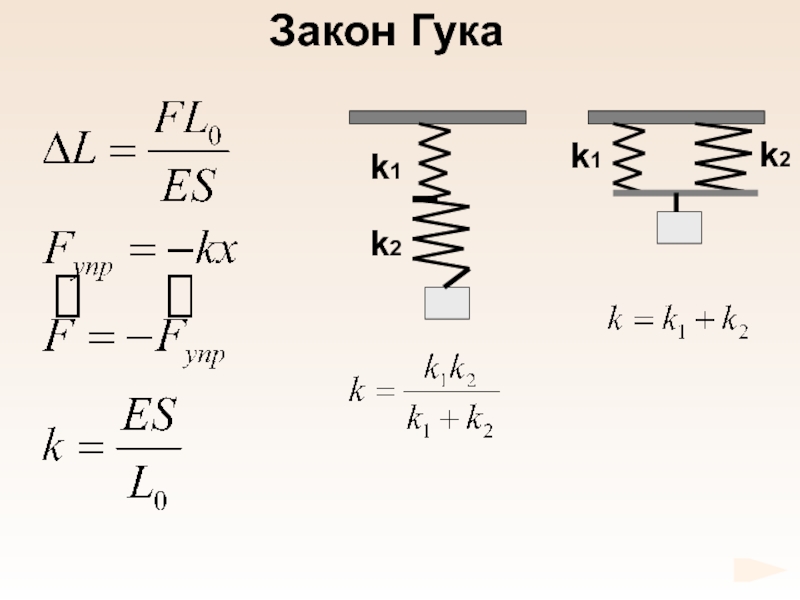
- 67. Закон Гука
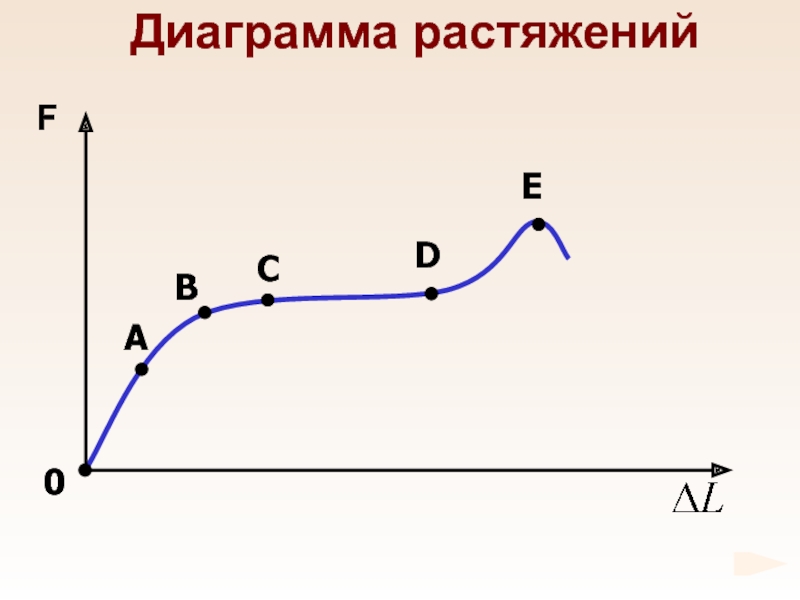
- 68. Диаграмма растяжений
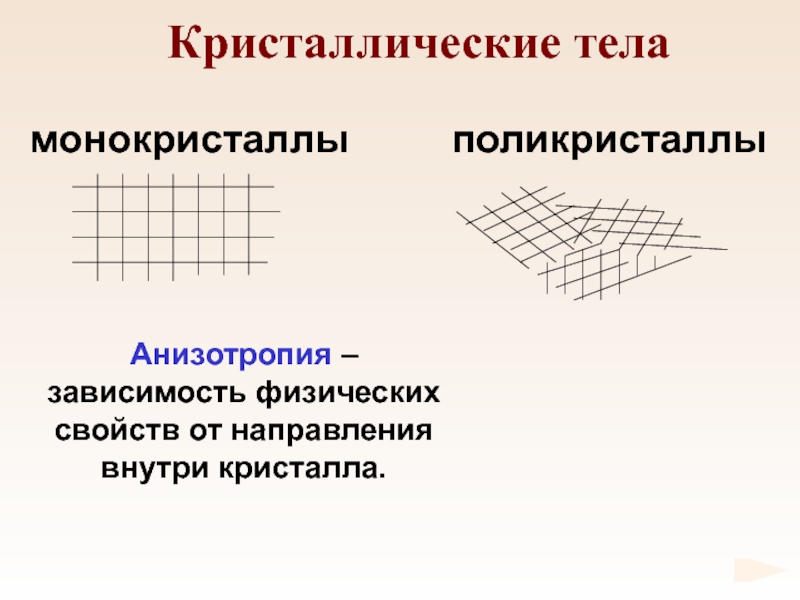
- 69. Кристаллические теламонокристаллыполикристаллыАнизотропия – зависимость физических свойств от направления внутри кристалла.
- 70. Аморфные телаНет строгого порядка в расположении атомов.Все
- 71. П.22. Внутренняя энергия и работа газа. Уравнение теплового баланса.
- 72. Внутренняя энергияВнутренняя энергия макроскопического тела равна сумме
- 73. Внутренняя энергияВ идеальном газе частицы не взаимодействуют между собой, следовательно их потенциальные энергии равны нулю.
- 74. Внутренняя энергияОдноатомный газ (неон, аргон, гелий) –
- 75. Внутренняя энергияСпособы изменения внутренней энергии:Передача теплотыСовершение работы
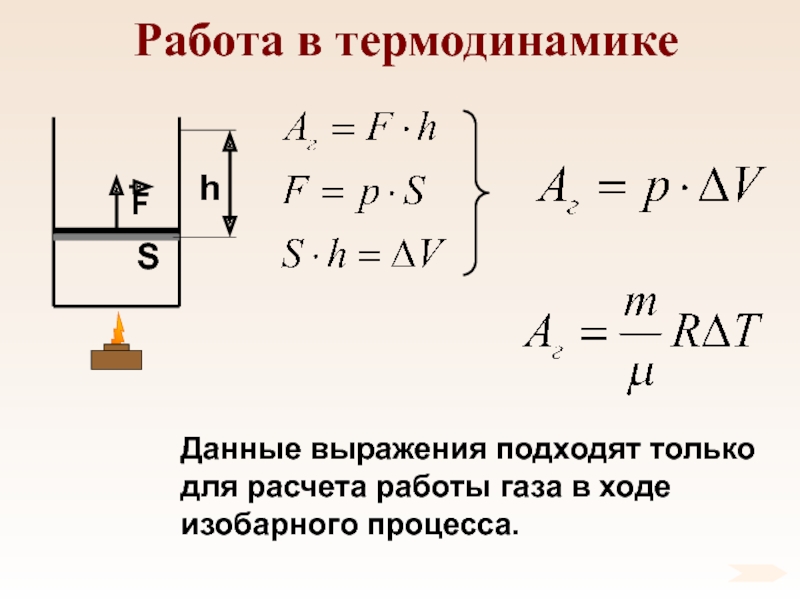
- 76. Работа в термодинамикеДанные выражения подходят только для расчета работы газа в ходе изобарного процесса.
- 77. Работа в термодинамикеЕсли процесс не изобарный, используется
- 78. Количество теплотыКоличество теплоты – это энергия полученная или отданная телом в процессе теплопередачи.Виды теплопередачи:ТеплопроводностьКонвекцияизлучение
- 79. Количество теплотыпотребляетсявыделяетсянагреваниеохлаждениес – удельная теплоемкость вещества –
- 80. Количество теплотыпотребляетсявыделяетсяплавлениекристаллизация
- 81. Количество теплотыпотребляетсявыделяетсяпарообразованиеконденсацияL - удельная теплота парообразования вещества
- 82. Количество теплотыпотребляетсявыделяетсяСгорание топливаq – удельная теплота сгорания
- 83. П. 23 Первый закон термодинамики и применение его к изопроцессам .
- 84. Первый закон термодинамикиИзменение внутренней энергии системы при
- 85. Применение первого закона термодинамики к различным процессамИзотермический процессИзобарный процессИзохорный процессАдиабатный процесс
- 86. Изотермический процессВ ходе изотермического процесса все полученное системой количество теплоты идет на совершение работы.
- 87. Изобарный процессДанный способ расчета внутренней энергии и количества теплоты подходит только для одноатомного газа.
- 88. Изобарный процессЕсли газ не одноатомный, тоМожно воспользоваться следующими выражениями:i – число степеней свободы движения частиц.
- 89. Изохорный процессВ ходе изохорного процесса все полученное системой количество теплоты идет на изменение внутренней энергии системы.
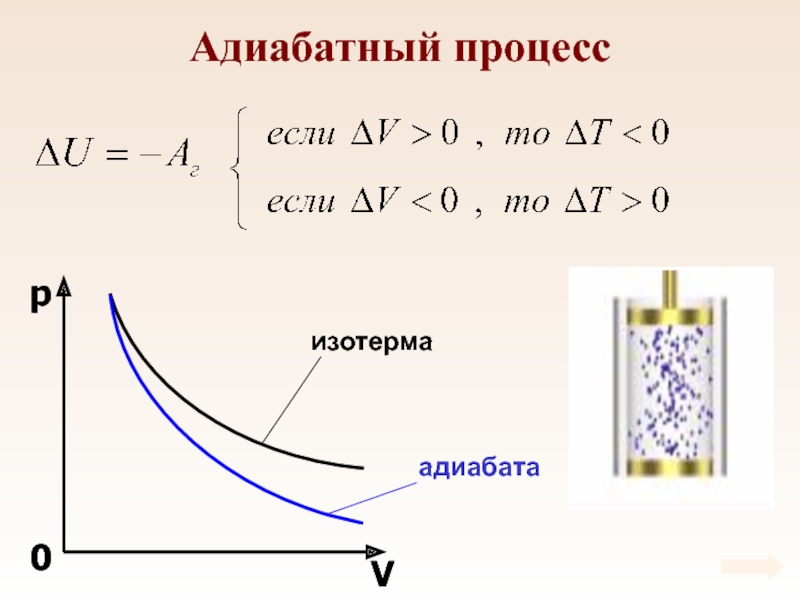
- 90. Адиабатный процессПроцесс, который происходит без теплообмена с
- 91. Адиабатный процесс
- 92. П.24. Тепловые двигатели. Второй закон термодинамики
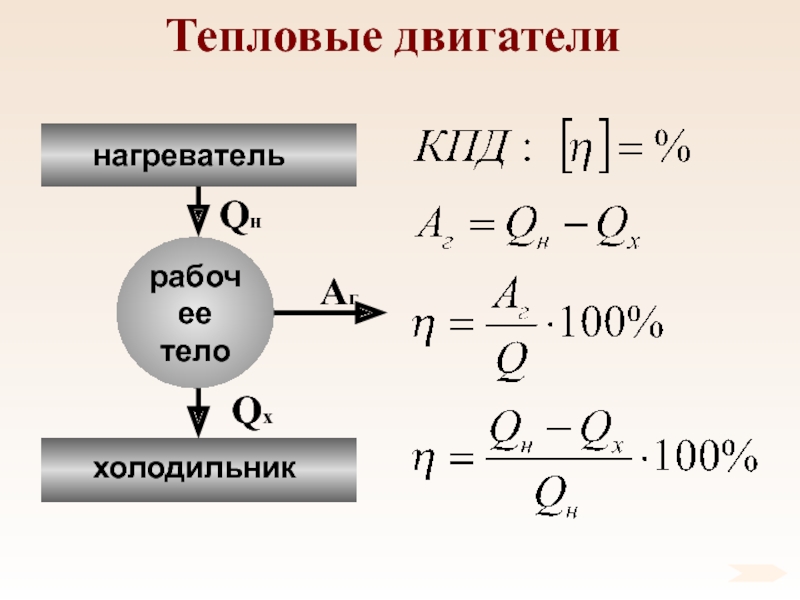
- 93. Тепловые двигателиТепловые двигатели – механизмы, преобразующие внутреннюю
- 94. Тепловые двигатели
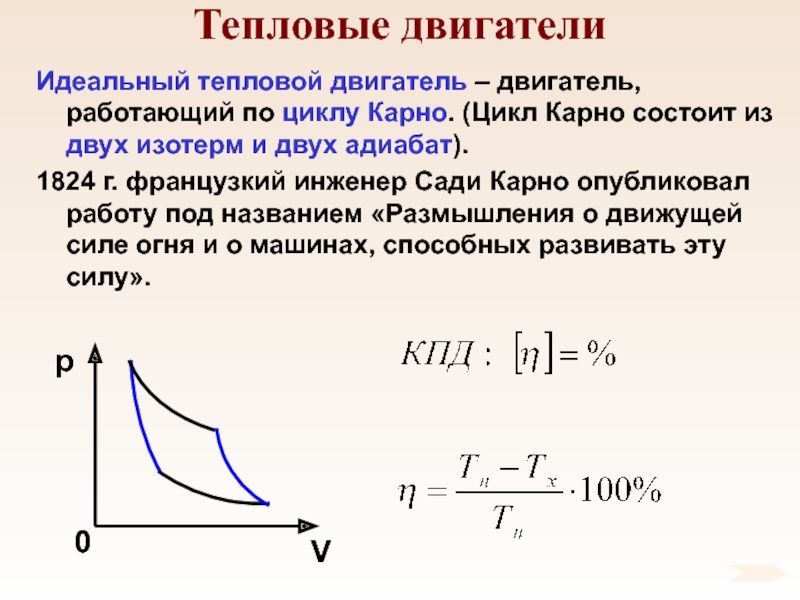
- 95. Тепловые двигателиИдеальный тепловой двигатель – двигатель, работающий
- 96. Скачать презентанцию
Слайды и текст этой презентации
Слайд 4Молекулярно-кинетическая теория
МКТ объясняет свойства макроскопических тел и тепловых процессов, на
основе представлений о том, что все тела состоят из отдельных,
беспорядочно движущихся частиц.Макроскопические тела – тела, состоящие из большого количества частиц.
Микроскопические тела – тела, состоящие из малого количества частиц.
Слайд 5Основные положения мкт
Вещество состоит из частиц
Частицы непрерывно и хаотически движутся
Частицы
взаимодействуют друг с другом
Слайд 9Масса и размеры молекул
Относительной молекулярной (или атомной) массой вещества (Мr)
называют отношение массы молекулы (или атома) m0 данного вещества к
1/12 массы атома углерода m0C.1961 год
Слайд 10Количество вещества
Количество вещества наиболее естественно было бы измерять числом молекул
или атомов в теле. Но число частиц в любом макроскопическом
теле так велико, что в расчетах используют не абсолютное число частиц, а относительное.Один моль – это количество вещества, в котором содержится столько же молекул или атомов, сколько содержится в углероде массой 12 г.
Слайд 11Количество вещества
В 1 моле любого вещества содержится одно и то
же число атомов или молекул.
Количество вещества равно отношению числа молекул
в данном теле к постоянной Авогадро.Слайд 12Количество вещества
Молярной массой вещества называют массу вещества, взятого в количестве
1 моль.
m0 - масса одной молекулы или атома
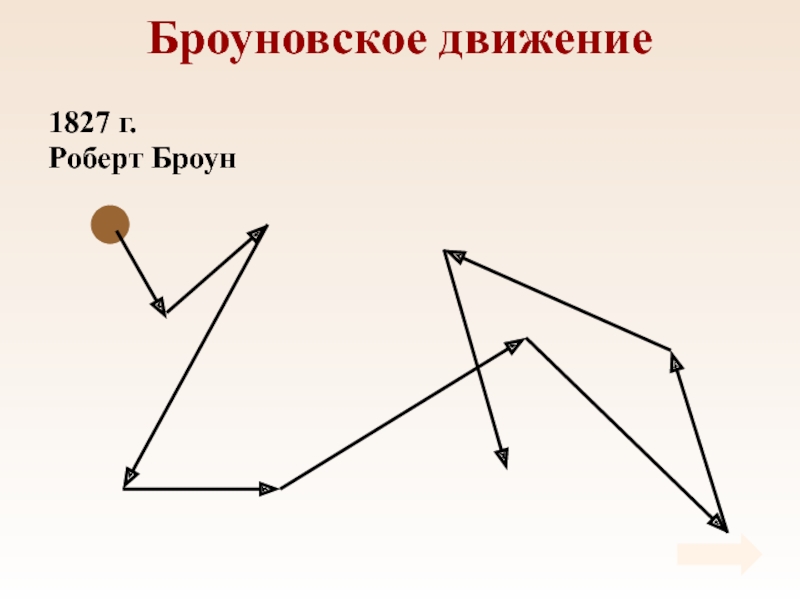
Слайд 15Броуновское движение
Причина броуновского движения состоит в том, что удары молекул
жидкости о частицу не компенсируют друг друга.
1905 г. Альберт Эйнштейн.
Слайд 21Расположение частиц
Частицы расположены в строгом порядке вплотную друг к другу.
Кристаллическая
решетка.
Слайд 22Расположение частиц
Частицы расположены вплотную друг к другу, образуют только ближний
порядок.
Слайд 23Расположение частиц
Частицы расположены на значительных расстояниях (расстояния между частицами во
много раз больше размеров самих частиц).
Слайд 24Движение и взаимодействие частиц
Частицы совершают колебательные движения около положения равновесия
Силы
притяжения и отталкивания значительны
Слайд 25Движение и взаимодействие частиц
Частицы совершают колебательные движения около положения равновесия,
изредка совершая скачки на новое место
Силы притяжения и отталкивания значительны
Слайд 26Движение и взаимодействие частиц
Частицы свободно перемещаются по всему объему, двигаясь
поступательно
Силы притяжения почти отсутствуют, силы отталкивания проявляются при соударениях
Слайд 28Идеальный газ
Идеальный газ – это газ, в котором
Частицы – материальные
точки
Частицы взаимодействуют только при соударениях
Удары абсолютно упругие
Слайд 29Среднее значение квадрата скорости молекул
Скорость – величина векторная, поэтому средняя
скорость движения частиц в газе равна нулю.
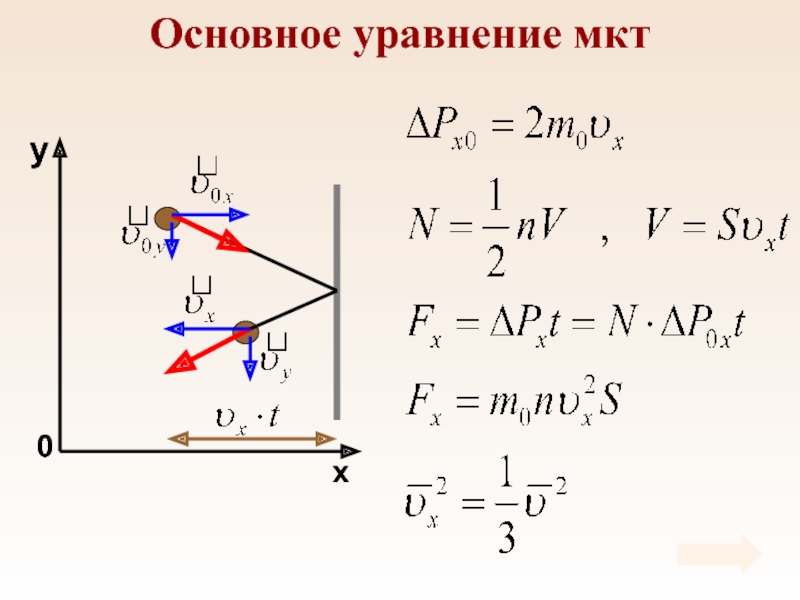
Слайд 31Основное уравнение мкт
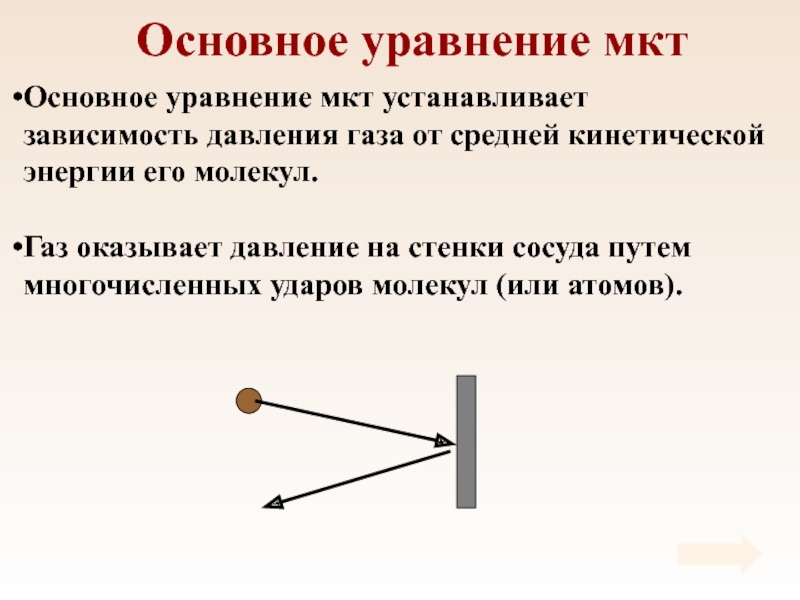
Основное уравнение мкт устанавливает зависимость давления газа от
средней кинетической энергии его молекул.
Газ оказывает давление на стенки сосуда
путем многочисленных ударов молекул (или атомов).Слайд 35Температура и тепловое равновесие
Макроскопические параметры (макропараметры) – величины, характеризующие состояние
макроскопических тел без учета молекулярного строения. (V, p, t ).
Тепловым
равновесием называют такое состояние, при котором все макроскопические параметры всех тел системы остаются неизменными сколь угодно долго.Слайд 36Температура и тепловое равновесие
Любое макроскопическое тело или группа макроскопических тел
при неизменных внешних условиях самопроизвольно переходит в состояние теплового равновесия.
Все
тела системы, находящиеся друг с другом в тепловом равновесии имеют одну и ту же температуру.Слайд 37Температура и тепловое равновесие
Термометр – прибор для измерения температуры тела.
Термометр
входит в состояние теплового равновесия с исследуемым телом и показывает
свою температуру.Слайд 38Температура и тепловое равновесие
Основная деталь термометра – термометрическое тело, то
есть тело, макропараметры которого изменяются при изменении температуры. (Например, в
ртутных термометрах термометрическим телом является ртуть – при изменении температуры изменяется ее объем.)Слайд 39Температура и тепловое равновесие
Изобретателем термометра является Галилео Галилей (ок. 1600
г.)
Термометрическим телом в его термометре являлся газ – при повышении
температуры его объем увеличивался, вытесняя жидкость.Недостатком термометра Галилея являлось отсутствие температурной шкалы.
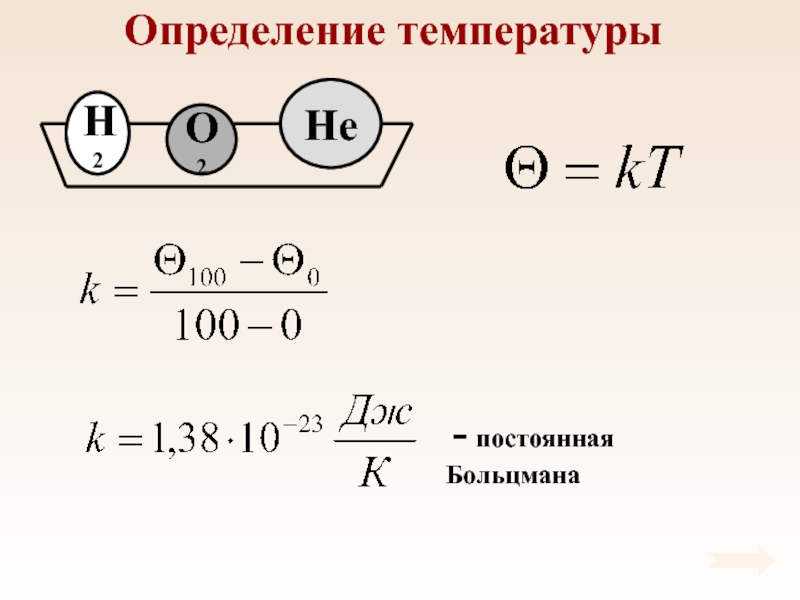
Слайд 41Определение температуры
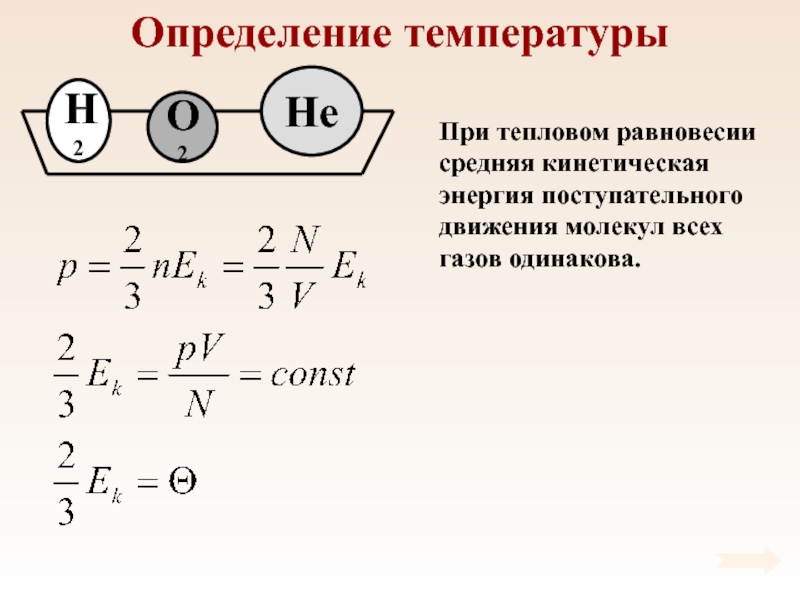
При тепловом равновесии средняя кинетическая энергия поступательного движения молекул
всех газов одинакова.
Слайд 47Уравнение состояния идеального газа
(ур-е Менделеева – Клапейрона)
- универсальная газовая постоянная
Слайд 48Уравнение состояния идеального газа
(ур-е Менделеева – Клапейрона)
Если в ходе процесса
масса газа остается неизменной, то
Слайд 51Изотермический процесс
Процесс, происходящий с газом неизменной массы при постоянной температуре
называется изотермическим.
Изотермический процесс описывается законом Бойля – Мариотта (конец 17
века):Слайд 52Изобарный процесс
Процесс, происходящий с газом неизменной массы при постоянном давлении
называется изобарным.
Изобарный процесс описывается законом Гей-Люссака (1802 г.):
Слайд 53Изохорный процесс
Процесс, происходящий с газом неизменной массы при постоянном объеме
называется изохорным.
Изохорный процесс описывается законом Шарля (1787 г.):
Слайд 55Тема 6. Термодинамика.
П. 21 Агрегатные состояния вещества и их фазовые
переходы. Аморфные тела.
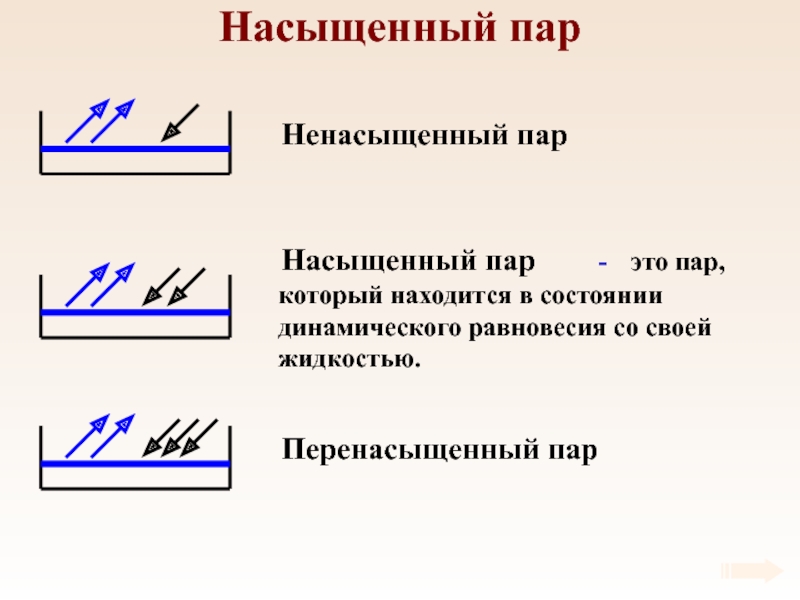
Слайд 56Насыщенный пар
Ненасыщенный пар
Насыщенный пар
Перенасыщенный пар
- это пар, который находится в состоянии динамического равновесия со своей жидкостью.
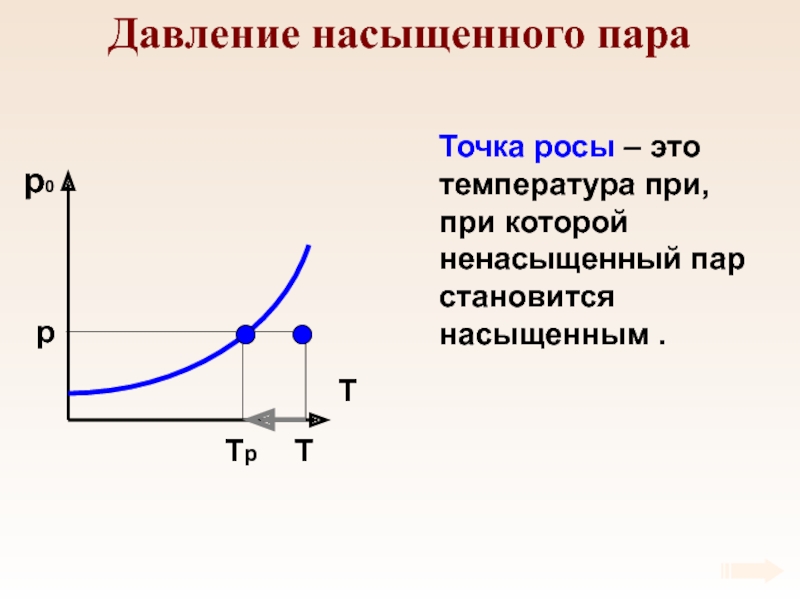
Слайд 59Давление насыщенного пара
p
T
Tр
Точка росы – это температура при, при которой
ненасыщенный пар становится насыщенным .
Слайд 60Испарение и кипение
Процесс парообразования с поверхности жидкости.
Процесс парообразования по всему
объему жидкости.
Происходит при любой температуре.
Происходит при температуре кипения.
Скорость испарения зависит
от:Вида жидкости
Температуры
Площади поверхности
Наличие ветра
Чем ниже давление, тем ниже температура кипения.
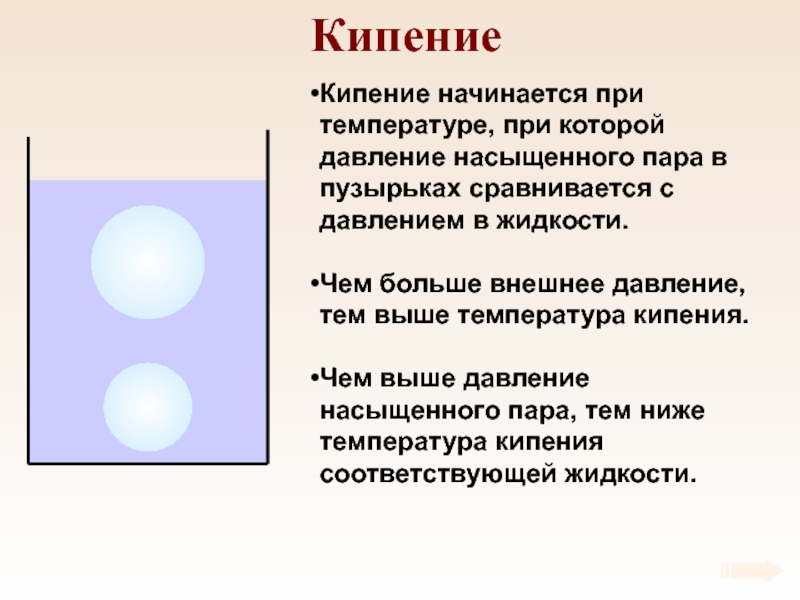
Слайд 61Кипение
Кипение начинается при температуре, при которой давление насыщенного пара в
пузырьках сравнивается с давлением в жидкости.
Чем больше внешнее давление, тем
выше температура кипения.Чем выше давление насыщенного пара, тем ниже температура кипения соответствующей жидкости.
Слайд 62Влажность
абсолютная
относительная
Плотность водяных паров в воздухе.
Отношение парциального давления водяного пара, содержащегося
в воздухе, к давлению насыщенного пара при данной температуре.
Слайд 69Кристаллические тела
монокристаллы
поликристаллы
Анизотропия – зависимость физических свойств от направления внутри кристалла.
Слайд 70Аморфные тела
Нет строгого порядка в расположении атомов.
Все аморфные тела изотропны,
т.е их физические свойства одинаковы по всем направлениям.
Аморфные тела не
имеют определенной температуры плавления.При внешних воздействиях аморфные тела обнаруживают одновременно упругие свойства, подобно твердым телам, и текучесть, подобно жидкости.
Слайд 72Внутренняя энергия
Внутренняя энергия макроскопического тела равна сумме кинетических энергий беспорядочного
движения всех молекул (или атомов) тела и потенциальных энергий взаимодействий
всех молекул друг с другом (но не с молекулами других тел).Слайд 73Внутренняя энергия
В идеальном газе частицы не взаимодействуют между собой, следовательно
их потенциальные энергии равны нулю.
Слайд 74Внутренняя энергия
Одноатомный газ (неон, аргон, гелий) – i =
3.
Двухатомный газ (водород, азот) – i = 5.
Трехатомный газ
(углекислый газ, озон) – i = 6.Слайд 76Работа в термодинамике
Данные выражения подходят только для расчета работы газа
в ходе изобарного процесса.
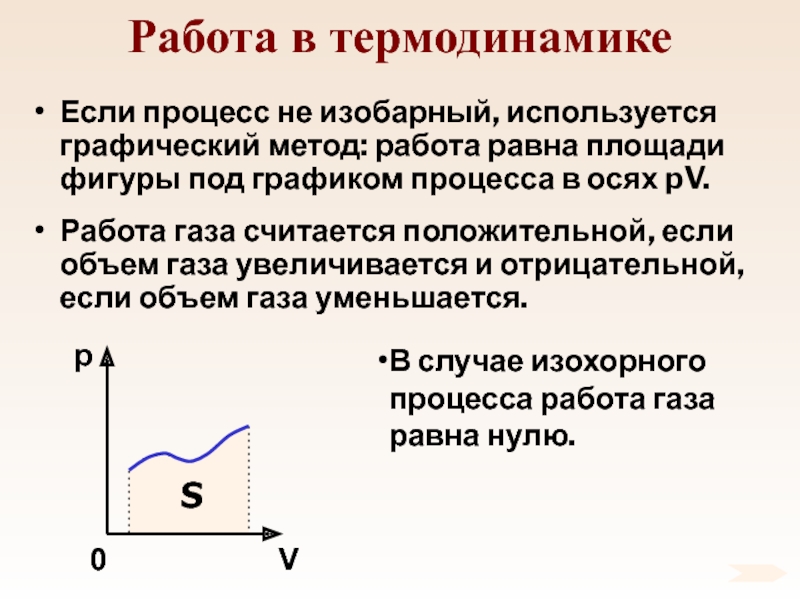
Слайд 77Работа в термодинамике
Если процесс не изобарный, используется графический метод: работа
равна площади фигуры под графиком процесса в осях pV.
Работа газа
считается положительной, если объем газа увеличивается и отрицательной, если объем газа уменьшается.В случае изохорного процесса работа газа равна нулю.
p
Слайд 78Количество теплоты
Количество теплоты – это энергия полученная или отданная телом
в процессе теплопередачи.
Виды теплопередачи:
Теплопроводность
Конвекция
излучение
Слайд 79Количество теплоты
потребляется
выделяется
нагревание
охлаждение
с – удельная теплоемкость вещества – величина равная энергии,
необходимой для нагревания тела массой 1 кг на 1 К.
Слайд 81Количество теплоты
потребляется
выделяется
парообразование
конденсация
L - удельная теплота парообразования вещества – величина равная
энергии, необходимой для того, чтобы жидкость массой 1 кг, взятая
при температуре кипения полностью перешла в газообразное состояние.Слайд 82Количество теплоты
потребляется
выделяется
Сгорание топлива
q – удельная теплота сгорания топлива – величина
равная энергии, которая выделяется при сгорании данного вида топлива массой
1 кг.Слайд 84Первый закон термодинамики
Изменение внутренней энергии системы при переходе ее из
одного состояния в другое равно сумме работы внешних сил и
количества теплоты, переданного системе.Количество теплоты, переданное системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами.