Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
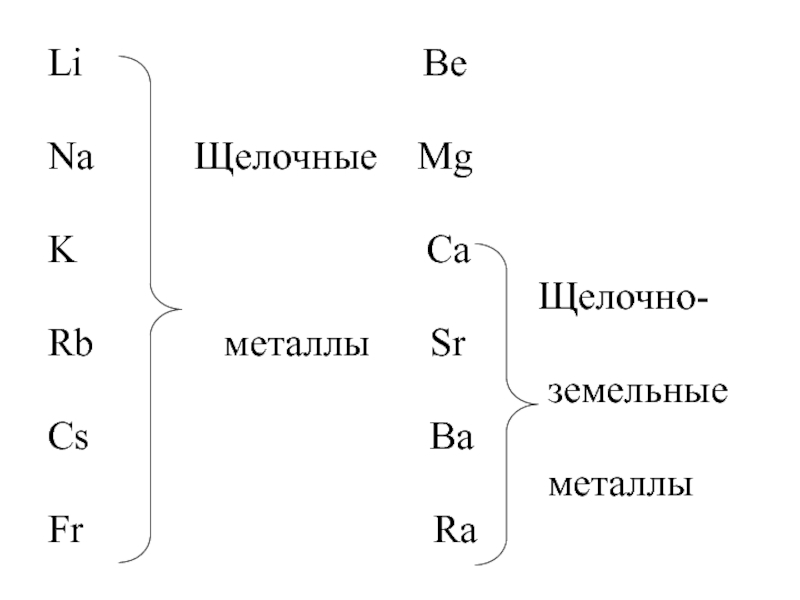
СВОЙСТВА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ I И II А ПОДГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ Д.И
Содержание
- 1. СВОЙСТВА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ I И II А ПОДГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ Д.И
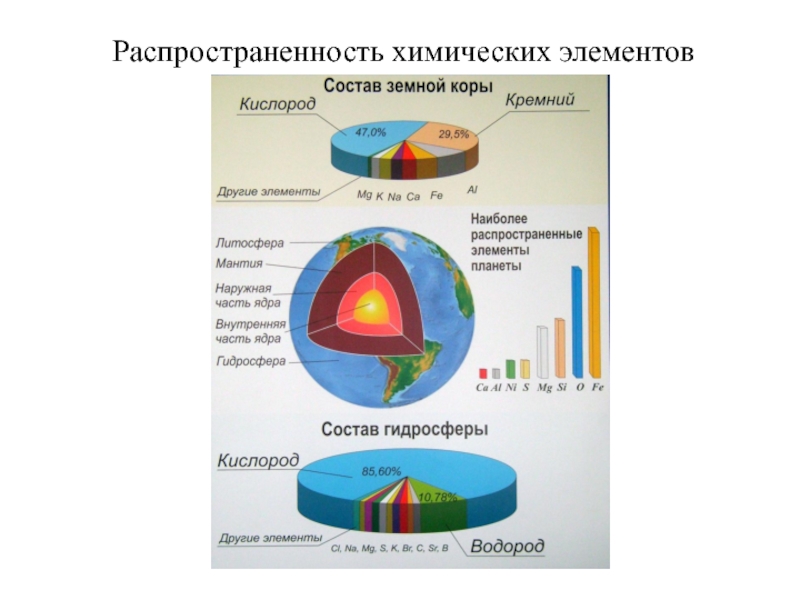
- 2. Распространенность химических элементов
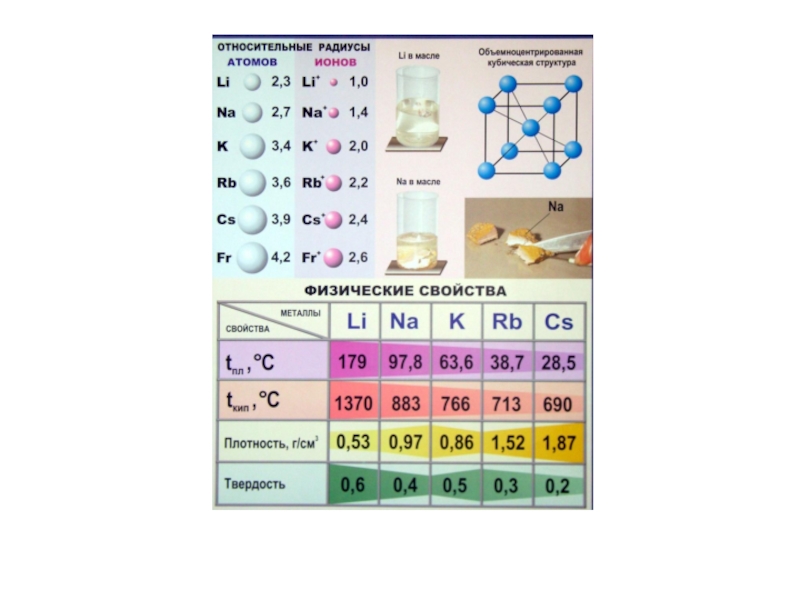
- 3. Li
- 4. Общая характеристика s-элементов
- 5. Слайд 5
- 6. Слайд 6
- 7. Распространённость в природеЛитийСподумен Li2O · Al2O3 · 4SiO2Амблигонит LiAlPO4FЛепидолит
- 8. НатрийГалит NaClМирабилит Na2SO4 · 10 H2OТенардит Na2SO4 Чилийская селитра NaNO3
- 9. КалийКарналлитСильвинит NaCl · KClЛангбейнит K2Mg2(SO4)3Рубидий, цезийСопутствуют калию
- 10. БериллийБерилл
- 11. МагнийОсадочные породы магнезит
- 12. КальцийОсадочные породы кальцит (известняк,
- 13. Стронций, барийИзоморфны кальцию встречаются в виде сульфатов,
- 14. Слайд 14
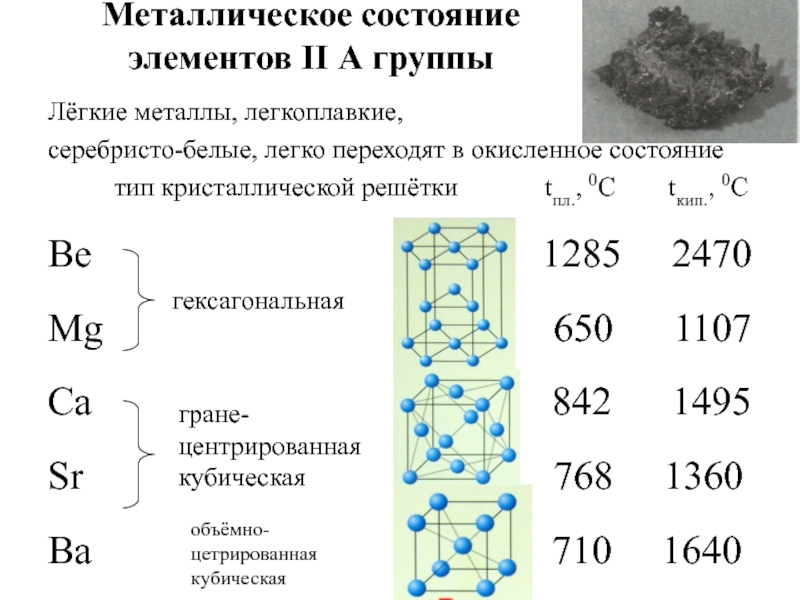
- 15. Металлическое состояние элементов II А группыЛёгкие
- 16. Слайд 16
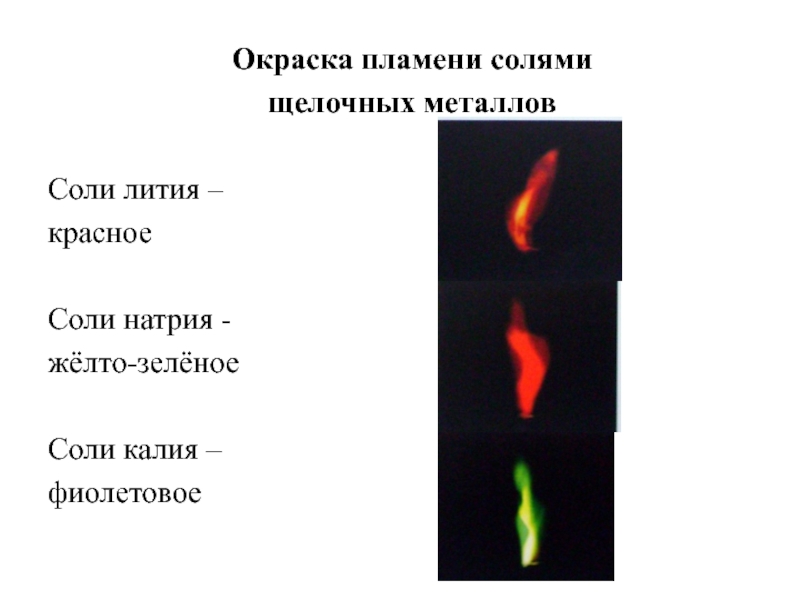
- 17. Окраска пламени солями щелочных металловСоли лития – красноеСоли натрия - жёлто-зелёноеСоли калия – фиолетовое
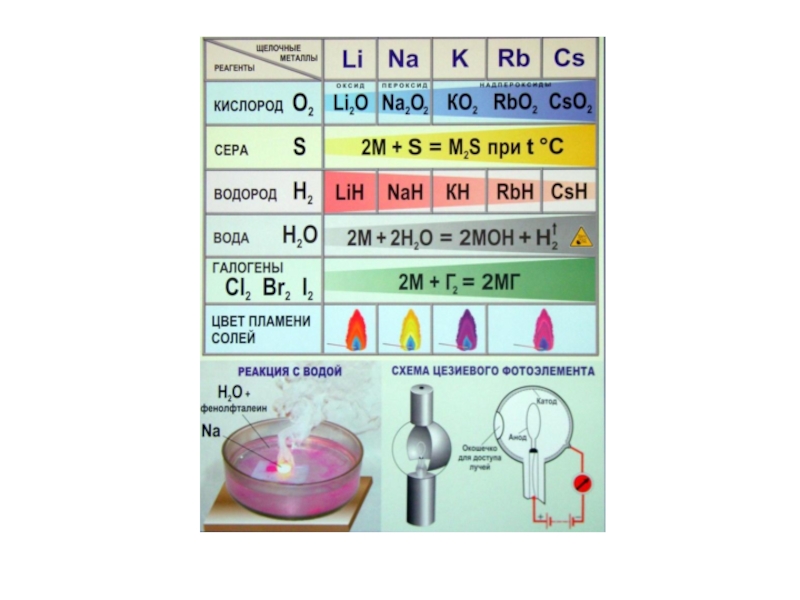
- 18. Химические свойства 2Bе + О2
- 19. 2M + Г2 → 2MГ2 3М +
- 20. Be + 2NaOH + 2H2O → Na2[Ве(ОН)4]
- 21. Получение Металлы нельзя получить из водных растворовЩелочные
- 22. Получение Бериллий получают:магнийтермически: ВеF2 + Мg
- 23. Магний получают: карботермически: MgO + C
- 24. Кальций, стронций и барий получают: 1) электролизом
- 25. Оксиды MOТугоплавки, бесцветны, гигроскопичныMO + Н2О =
- 26. Получение оксидовBe(OH)2 = BeO + Н2ОВеSО4 =
- 27. ГидроксидыM(OH)2Ca(OH)2 – известковое молоко Ba(OH)2 – баритовая
- 28. Получение гидроксидовВеСl2 + 2КОН = Ве(ОН)2↓ +
- 29. Соли КарбонатыBeCO3·4H2O xBe(OH)2·yBeCO3(NH4)2[Be(CO3)2]3MgCO3·Mg(OH)2·3H2OСа, Sr, Ba: МСО3, М(НСО3)2
- 30. СульфатыBeSO4·4H2O [Be(H2O)4]SO4MgSO4·7H2OCaSO4·2H2O, CaSO4·0,5H2O, CaSO4
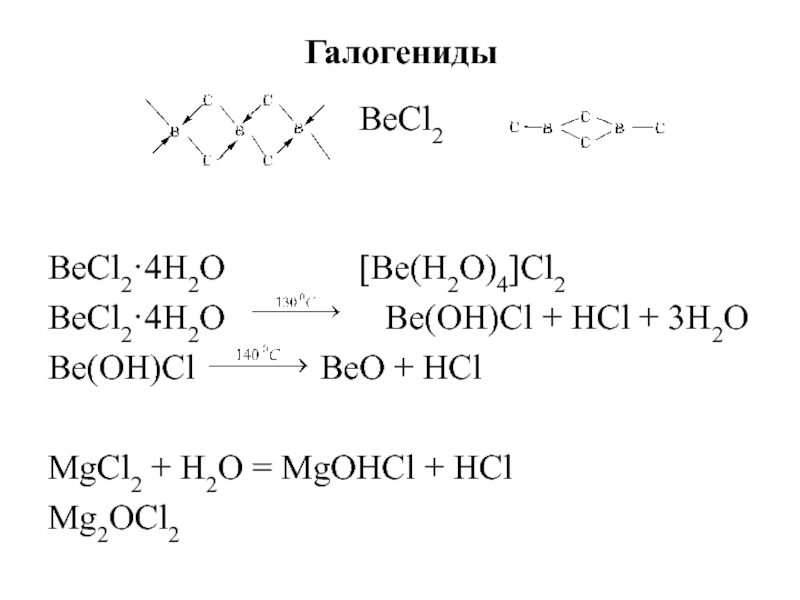
- 31. Галогениды
- 32. Бинарные соединенияMSMSeM3N2, M2N4, BaN2M3P2, M3As2, M3Sb2 Be2C
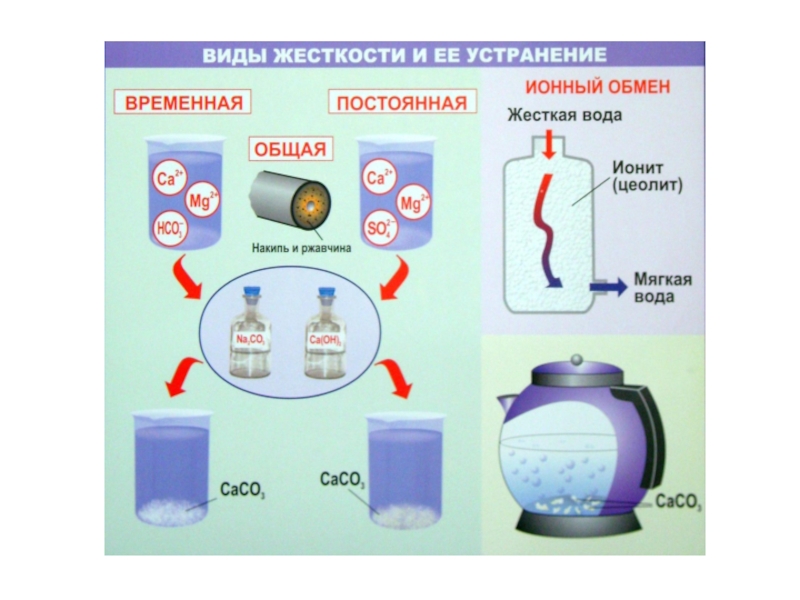
- 33. Жёсткость воды
- 34. Слайд 34
- 35. Совокупность временной и постоянной жёсткости называется общей
- 36. Устранение жёсткости водыВременная жёсткость устраняется кипячением:M(HCO3)2
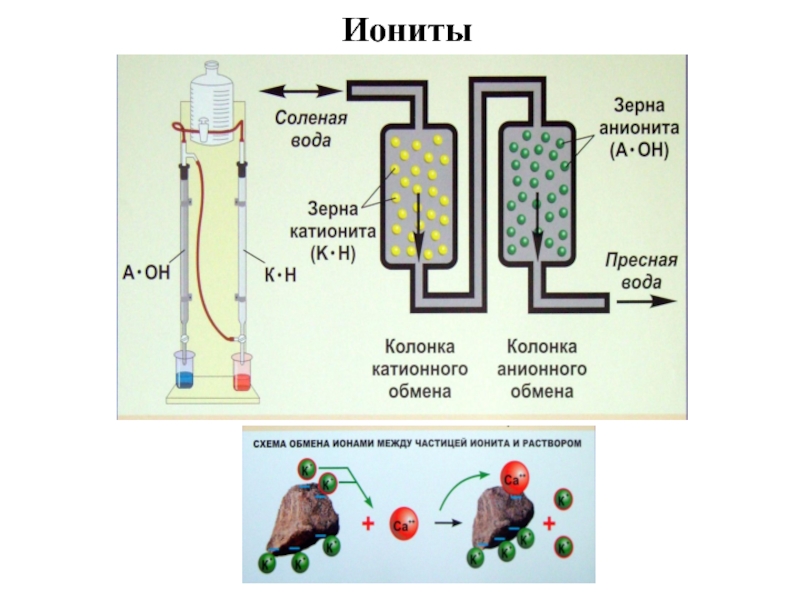
- 37. Иониты
- 38. Применение, влияние на живой организм
- 39. Скачать презентанцию
Распространенность химических элементов
Слайды и текст этой презентации
Слайд 4Общая характеристика s-элементов
M0 ns1
M0 ns2
M+ ns0 M2+ ns0
Проявляемая степень окисления в соединениях:
+1 +2
Слайд 11Магний
Осадочные породы
магнезит
доломит карналлит
MgCO3 CaCO3·MgCO3 KCl·MgCl2·6H2O Изверженные породы
оливин асбест тальк
(Mg,Fe)2[SiO4] Mg6[Si4O11](OH)·6H2O 3MgO · 4SiO2 · H2O
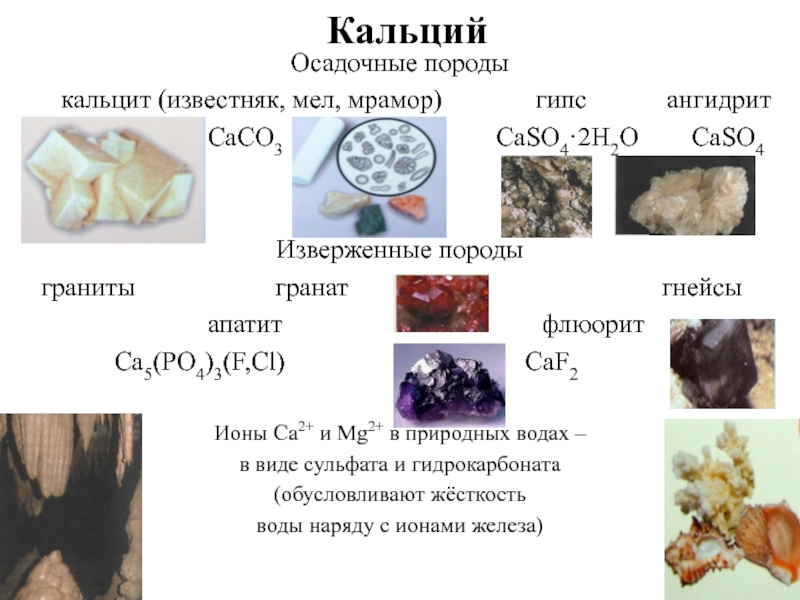
Слайд 12Кальций
Осадочные породы
кальцит (известняк, мел, мрамор)
гипс
ангидритCaCO3 СаSО4·2Н2О СаSО4
Изверженные породы
граниты гранат гнейсы
апатит флюорит
Са5(РО4)3(F,Сl) CaF2
Ионы Ca2+ и Mg2+ в природных водах –
в виде сульфата и гидрокарбоната
(обусловливают жёсткость
воды наряду с ионами железа)
Слайд 13Стронций, барий
Изоморфны кальцию
встречаются в виде сульфатов, карбонатов
целестин
стронцианит SrSО4 SrСО3барит (тяжёлый шпат) витерит
ВаSО4 ВаСО3
Слайд 15Металлическое состояние
элементов II А группы
Лёгкие металлы, легкоплавкие,
серебристо-белые, легко
переходят в окисленное состояние
тип кристаллической
решётки tпл., 0С tкип., 0СBe 1285 2470
Mg 650 1107
Ca 842 1495
Sr 768 1360
Ba 710 1640
гексагональная
гране-
центрированная кубическая
объёмно-цетрированная кубическая
Слайд 17Окраска пламени солями
щелочных металлов
Соли лития –
красное
Соли натрия -
жёлто-зелёное
Соли калия –
фиолетовое
Слайд 192M + Г2 → 2MГ2
3М + N2 → М3N2
М
+ S → МS
3М + 2Р → М3Р2
М + С → МС2 или 2М + 3С → М2С3
M + H2 → MH2 MH2 + 2H2O = M(OH)2 + H2
М + Н2О → М(ОН)2 + Н2
M + 2HA → МеA2 + Н2
Слайд 20
Be + 2NaOH + 2H2O → Na2[Ве(ОН)4] + Н2
(с концентрированными
- на холоде, с разбавленными - при нагревании)
Be + 2NaOH
Na2ВеО2 + Н2бериллат натрия
Слайд 21Получение
Металлы нельзя получить из водных растворов
Щелочные металлы получают:
1)
электролизом расплавов, например LiCl:
2LiCl
2Li + Cl22) кальцийтермически:
2CsCl + Ca Cs + CaCl2
Слайд 22Получение
Бериллий получают:
магнийтермически:
ВеF2 + Мg
Ве + МgF2
2) электролизом
расплава ВеCl2ВеCl2 Be + Cl2
Слайд 24Кальций, стронций и барий получают:
1) электролизом расплавов хлоридов кальция
и
стронция или оксида бария
2) алюмотермически в вакууме:
6CaO + 2Al
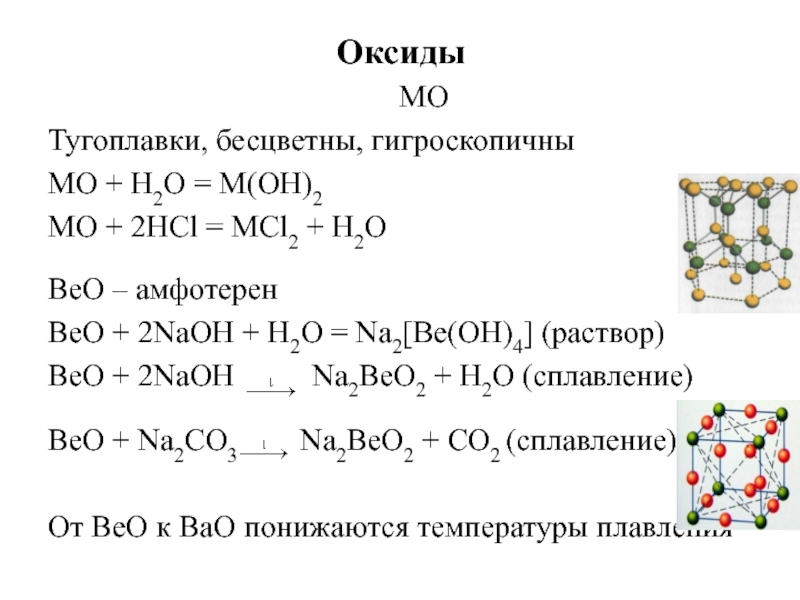
3Ca + 3CaO·Al2O3Слайд 25Оксиды
MO
Тугоплавки, бесцветны, гигроскопичны
MO + Н2О = M(OH)2
MO +
2НСl = МСl2 + Н2О
BeO – амфотерен
ВеО + 2NаОН +
Н2О = Nа2[Ве(ОН)4] (раствор)ВеО + 2NаОН Nа2ВеО2 + Н2О (сплавление)
ВеО + Nа2CО3 Nа2ВеО2 + CО2 (сплавление)
От BeO к BaO понижаются температуры плавления
Слайд 26Получение оксидов
Be(OH)2 = BeO + Н2О
ВеSО4 = ВеО + SО3
MСО3
= MО + СО2
2M(NО3)2 = 2MО + 4NО2 + О2
Слайд 27Гидроксиды
M(OH)2
Ca(OH)2 – известковое молоко
Ba(OH)2 – баритовая вода
M(ОН)2 +
2НСl = MСl2 + 2Н2О
Be(ОН)2 + 2НСl + 2H2O
= [Be(Н2О)4]Сl2 Ве(ОН)2 + 2NаОН = Nа2[Ве(ОH)]4
M(OH)2 MO + Н2О
Слайд 28Получение гидроксидов
ВеСl2 + 2КОН = Ве(ОН)2↓ + 2КСl
MgСl2 + 2КОН
= Mg(ОН)2↓ + 2КСl
ВеСl2 + 2NН3·Н2О = Ве(ОН)2↓ + 2NН4Сl
Особые
свойства:MgСl2 + 2NН3·Н2О = Mg(ОН)2 + 2NН4Сl
Слайд 29Соли
Карбонаты
BeCO3·4H2O
xBe(OH)2·yBeCO3
(NH4)2[Be(CO3)2]
3MgCO3·Mg(OH)2·3H2O
Са, Sr, Ba: МСО3, М(НСО3)2
СаСО3↓ + CO2
+ H2O = Са(НСО3)2
СаСО3 + 2HCl = CaCl2 +
CO2 + H2O Слайд 30Сульфаты
BeSO4·4H2O [Be(H2O)4]SO4
MgSO4·7H2O
CaSO4·2H2O, CaSO4·0,5H2O, CaSO4
SrSO4, BaSO4
CaSO4·2H2O
← CaSO4·0,5H2O
+ 1,5H2OCaSO4·2H2O CaSO4 + 2H2O
Слайд 31Галогениды
BeCl2
BeCl2·4H2O
[Be(H2O)4]Cl2BeCl2·4H2O Be(OH)Cl + HCl + 3H2O
Be(OH)Cl BeO + HCl
MgCl2 + H2O = MgOHCl + HCl
Mg2OCl2
Слайд 32Бинарные соединения
MS
MSe
M3N2, M2N4, BaN2
M3P2, M3As2, M3Sb2
Be2C и BeC2, MgC2
и Mg2C3, MC2
Mg2Si и Mg2Ge,
MSi, MSi2
Слайд 35Совокупность временной и постоянной жёсткости называется общей жёсткостью воды: ЖО
= ЖК + ЖНК.
Ж =
, где m – масса растворённого вещества, г;
МЭ – эквивалентная масса растворённого вещества, г/моль;
V – объём воды, л.
По значению жёсткости воду условно подразделяют на:
очень мягкую < 1,5 ммоль/л
мягкую 1,5–4 ммоль/л
средней жёсткости 4–8 ммоль/л
жёсткую 8–12 ммоль/л
очень жёсткую > 12 ммоль/л
Слайд 36Устранение жёсткости воды
Временная жёсткость устраняется кипячением:
M(HCO3)2
MCO3 + CO2 + H2O
Постоянная жёсткость устраняется
физическими или химическими способамиCaSO4 + Na2CO3 → CaCO3 + Na2SO4
Са(НСО3)2 + Са(ОН)2 = 2СаСО3↓ + 2Н2О










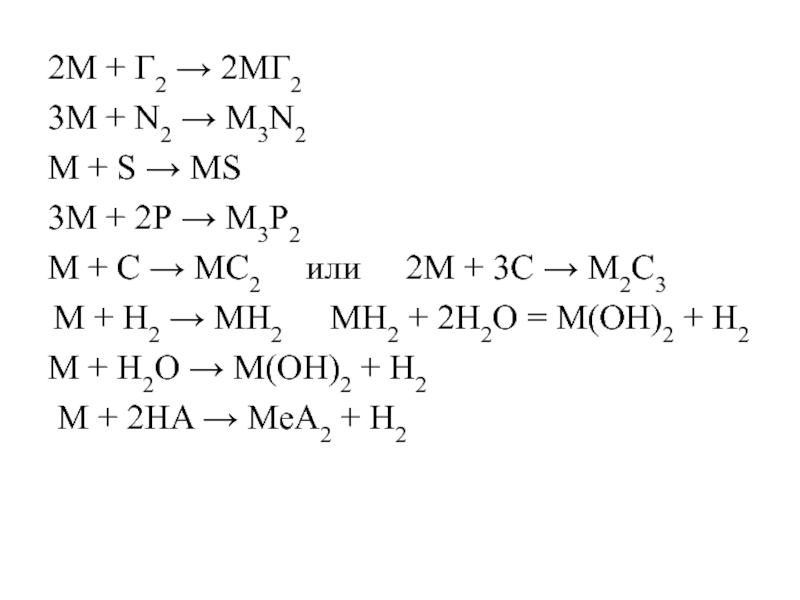
![СВОЙСТВА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ I И II А ПОДГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ Д.И Be + 2NaOH + 2H2O → Na2[Ве(ОН)4] + Н2(с концентрированными - Be + 2NaOH + 2H2O → Na2[Ве(ОН)4] + Н2(с концентрированными - на холоде, с разбавленными - при](/img/thumbs/4b26b5c18616a4e27680eabbfe50b208-800x.jpg)







![СВОЙСТВА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ I И II А ПОДГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ Д.И Соли КарбонатыBeCO3·4H2O xBe(OH)2·yBeCO3(NH4)2[Be(CO3)2]3MgCO3·Mg(OH)2·3H2OСа, Sr, Ba: МСО3, М(НСО3)2 СаСО3↓ + CO2 + Соли КарбонатыBeCO3·4H2O xBe(OH)2·yBeCO3(NH4)2[Be(CO3)2]3MgCO3·Mg(OH)2·3H2OСа, Sr, Ba: МСО3, М(НСО3)2 СаСО3↓ + CO2 + H2O = Са(НСО3)2 СаСО3 + 2HCl](/img/thumbs/69c73c909e9d0ca0f32ffd03076526a0-800x.jpg)
![СВОЙСТВА ХИМИЧЕСКИХ ЭЛЕМЕНТОВ I И II А ПОДГРУПП ПЕРИОДИЧЕСКОЙ СИСТЕМЫ Д.И СульфатыBeSO4·4H2O [Be(H2O)4]SO4MgSO4·7H2OCaSO4·2H2O, CaSO4·0,5H2O, CaSO4 SrSO4, BaSO4 CaSO4·2H2O ← СульфатыBeSO4·4H2O [Be(H2O)4]SO4MgSO4·7H2OCaSO4·2H2O, CaSO4·0,5H2O, CaSO4 SrSO4, BaSO4 CaSO4·2H2O ←](/img/thumbs/89a77b3b602ed7c9898da8353b31a99f-800x.jpg)