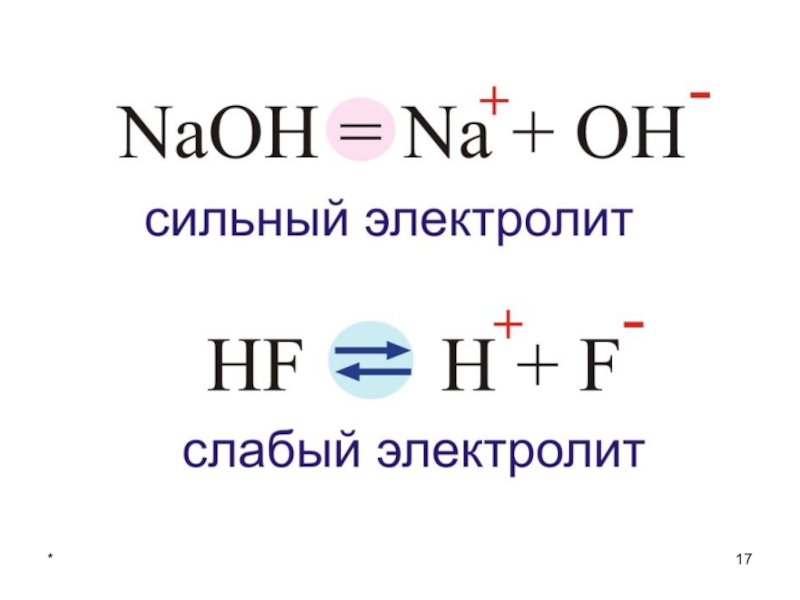Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Электролитическая диссоциация
Содержание
- 1. Электролитическая диссоциация
- 2. *Прибор для определения электропроводности
- 3. *Электролиты – это вещества, водные растворы которых
- 4. *Электропроводность веществ
- 5. *Вещества Электролиты(проводят электрический ток) Кислоты (HCl; H2SO4);Основания
- 6. *Вещества
- 7. *Задание. Из предложенного списка выбери вещества, которые
- 8. * Электролитическая диссоциация - процесс распада электролита на
- 9. * При растворении электролита происходит химическое взаимодействие растворенного
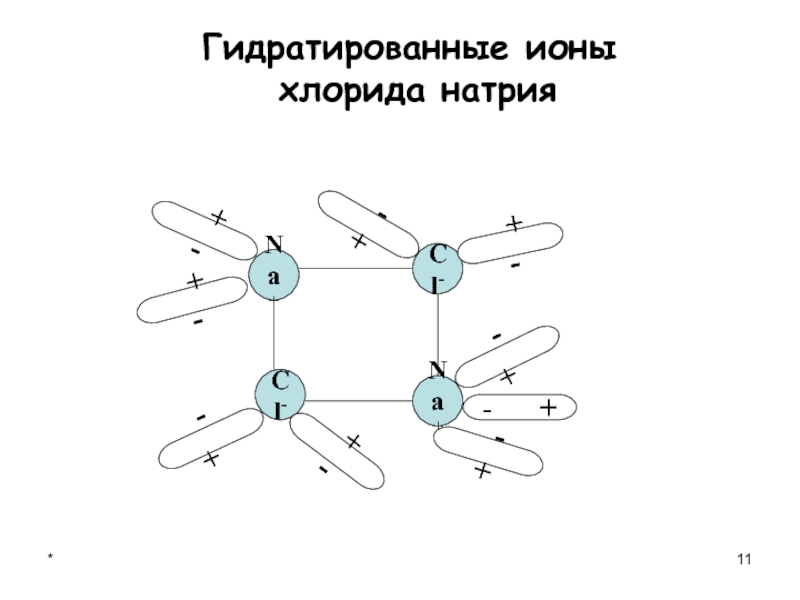
- 10. *Диссоциация веществ с ионной связью:Na+Cl-Cl-Na+ +
- 11. *Na+Cl-Cl-Na+ + - +
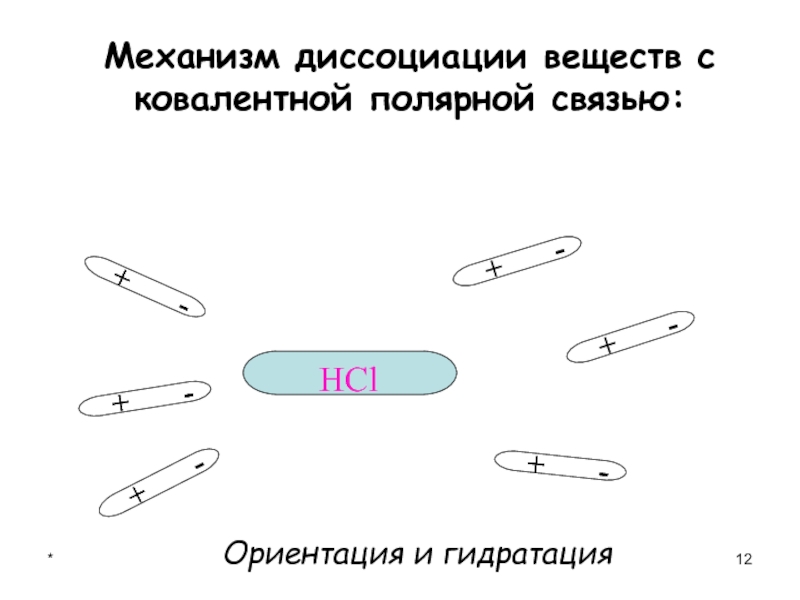
- 12. *Механизм диссоциации веществ с ковалентной полярной связью:
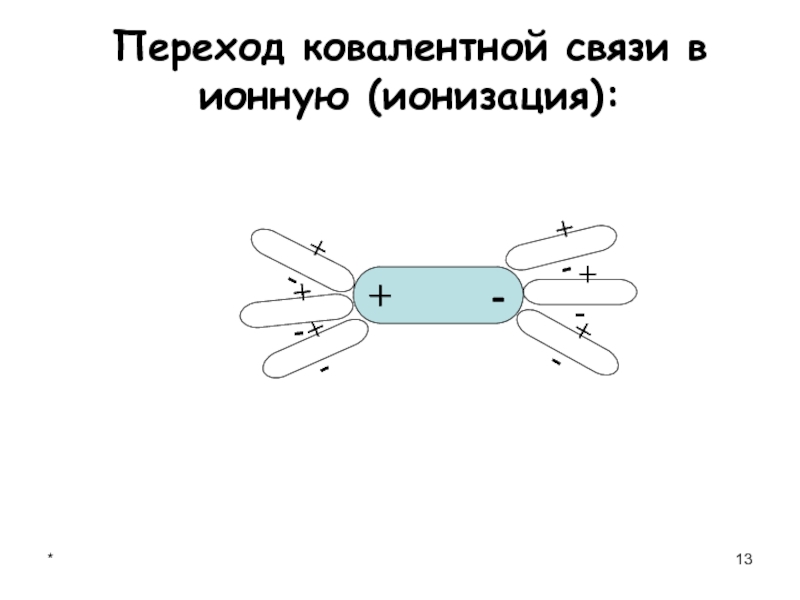
- 13. *Переход ковалентной связи в ионную (ионизация): +
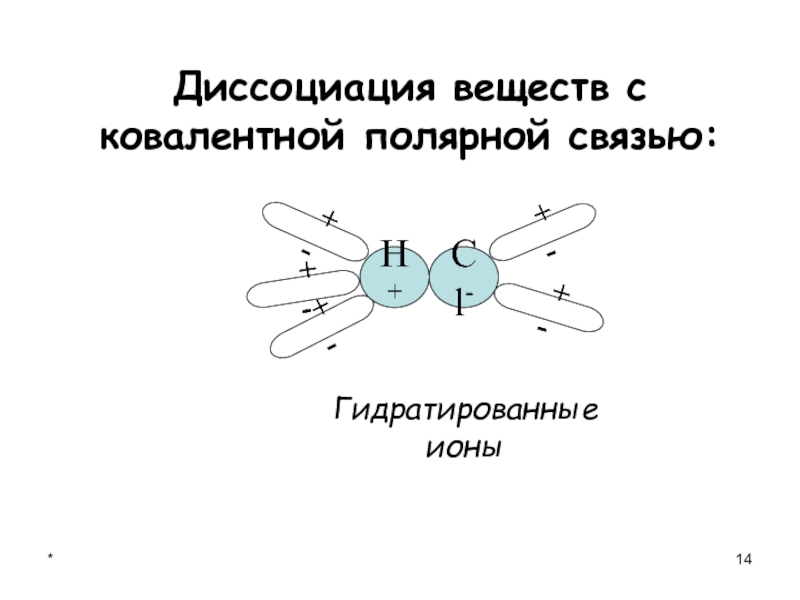
- 14. *Диссоциация веществ с ковалентной полярной связью:
- 15. *Степень электролитической диссоциации α Количественная характеристика процесса
- 16. * ЭлектролитыСильныеα>30%Средние30%>α>3%Слабыеα
- 17. *
- 18. *Задание. Напиши уравнение диссоциации веществ. 1. KNO3
- 19. *Что называют электролитической диссоциацией?Какие вещества называют электролитами?
- 20. *Задание. Пользуясь таблицей растворимости, определите, водные растворы
- 21. Домашнее задание:§*
- 22. Скачать презентанцию
Слайды и текст этой презентации
Слайд 3*
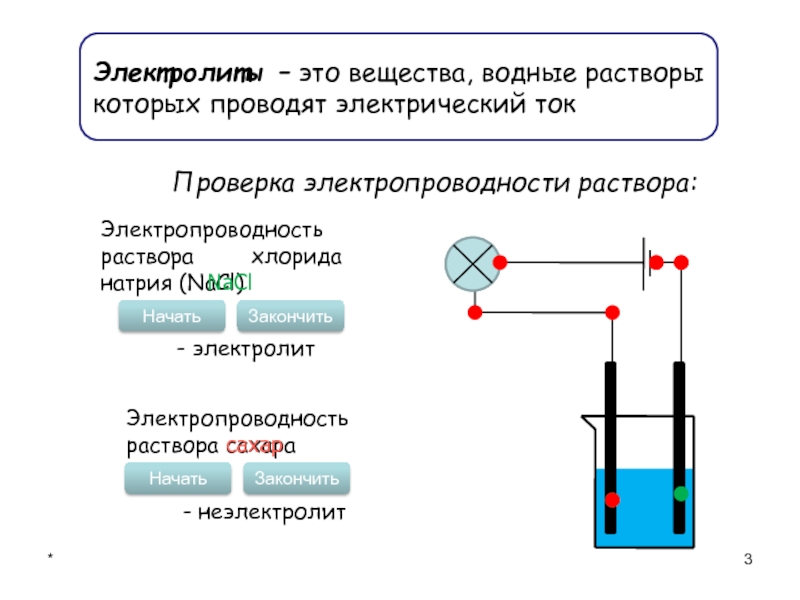
Электролиты – это вещества, водные растворы которых проводят электрический ток
Проверка
электропроводности раствора:
Электропроводность раствора хлорида натрия (NaCl)
Начать
Закончить
NaCl
- электролит
Электропроводность раствора сахара
Начать
Закончить
сахар
-
неэлектролит
Слайд 5*
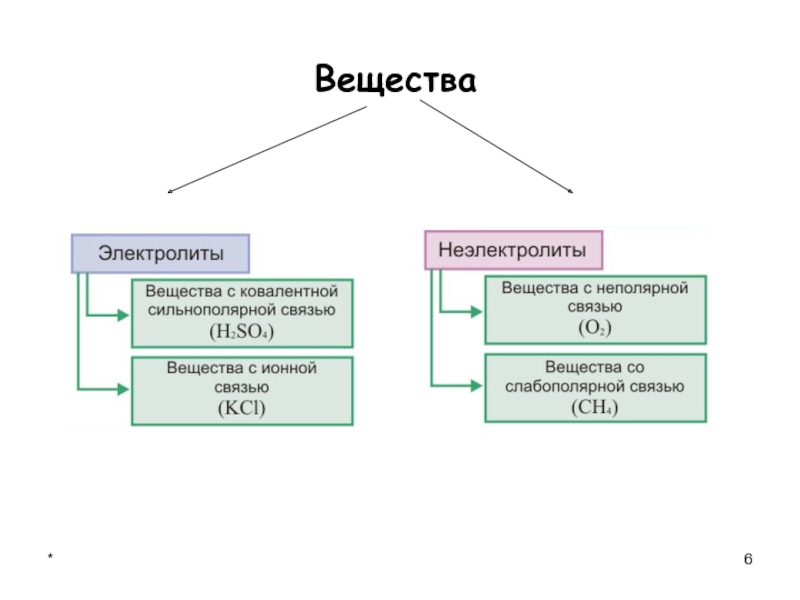
Вещества
Электролиты
(проводят электрический ток)
Кислоты (HCl; H2SO4);
Основания (NaOH; Ba(OH)2);
Соли (NaCl;
CuSO4).
Неэлектролиты
(не проводят электрический ток)
Органические вещества;
Газы (O2; H2; CO2);
Оксиды (CuO;
Fe2O3).Слайд 7*
Задание. Из предложенного списка выбери вещества, которые относятся к электролитам.
1) HCl;
6) H2SO4;2) N2; 7) CaCO3;
3) KOH; 8) Br2;
4) C6H12O6; 9) CH4;
5) NaCl; 10) C12H22O11.
Слайд 8*
Электролитическая диссоциация - процесс распада электролита на ионы при растворении
в воде или расплавлении.
Сванте Август
Аррениус
1859-1927гг.
Шведский физико-химик,
создатель теории
электролитической
диссоциации.
Слайд 9*
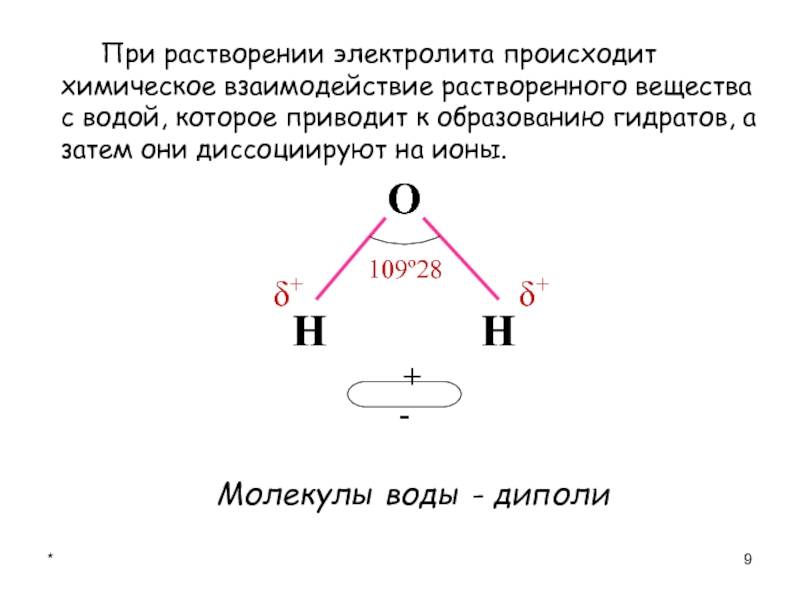
При растворении электролита происходит химическое взаимодействие растворенного вещества с водой,
которое приводит к образованию гидратов, а затем они диссоциируют на
ионы. Молекулы воды - диполи
О
Н
Н
109º28
+ -
δ+
δ+
Слайд 10*
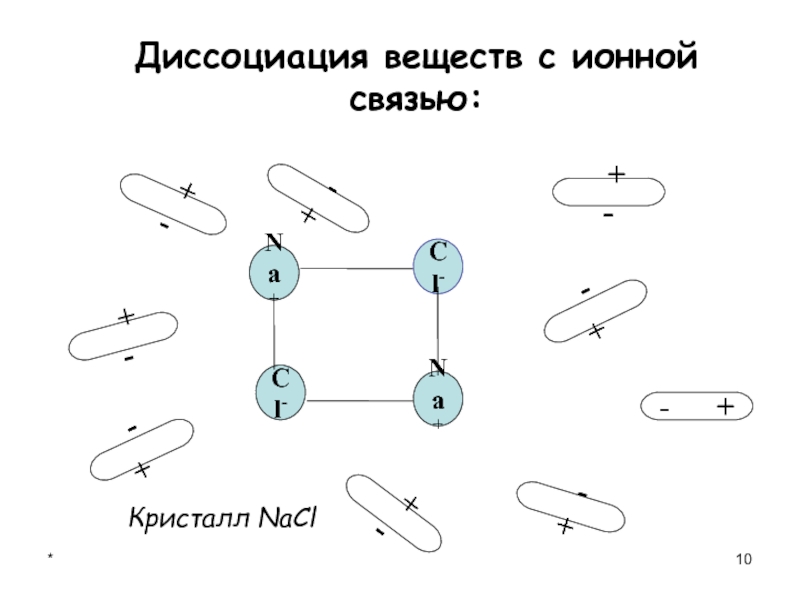
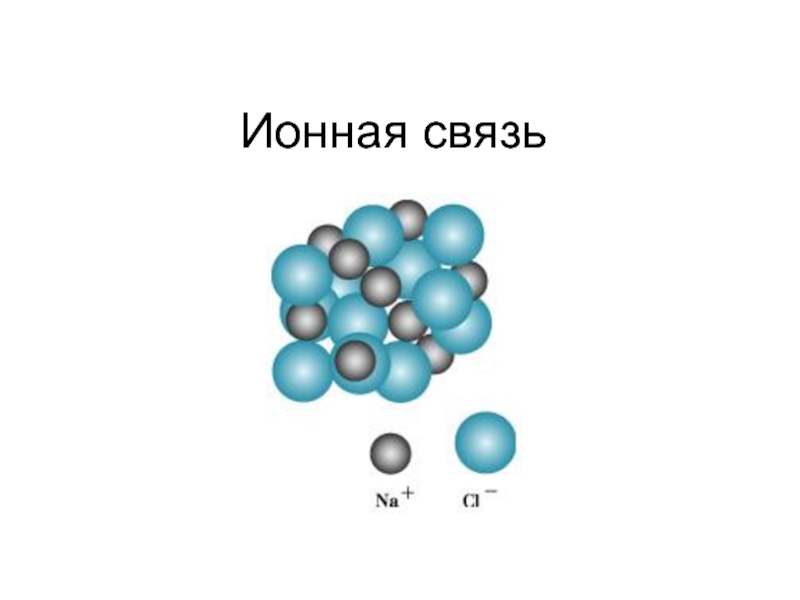
Диссоциация веществ с ионной связью:
Na+
Cl-
Cl-
Na+
+ -
+ -
+ -
- +- +
- +
+ -
+ -
+ -
Кристалл NaCl
Слайд 12*
Механизм диссоциации веществ с ковалентной полярной связью:
+ -
+
- + -
+ -
+ -
+ -
HCl
Ориентация и гидратация
Слайд 14*
Диссоциация веществ с ковалентной полярной связью:
+
-
+ -
+
- + -
Гидратированные ионы
+ -
H+
Cl-
Слайд 15*
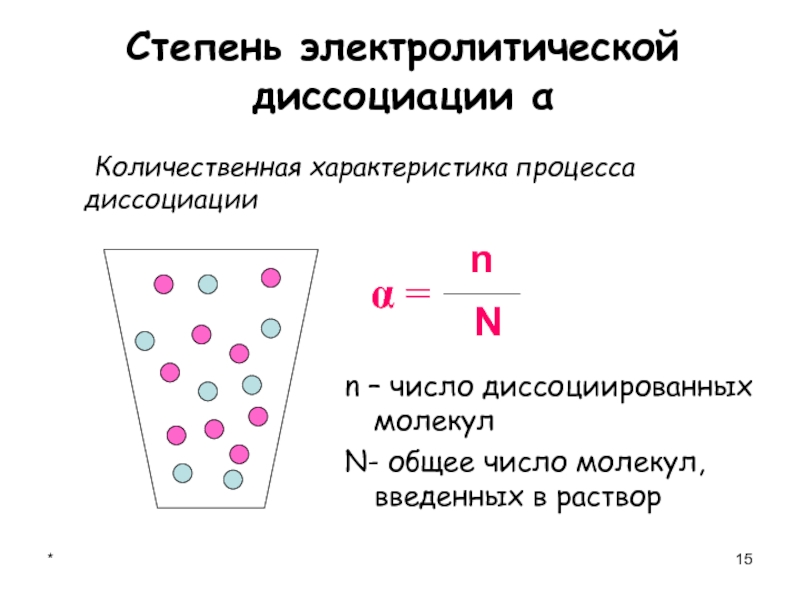
Степень электролитической диссоциации α
Количественная характеристика процесса диссоциации
n
– число диссоциированных молекул
N- общее число молекул, введенных в
раствор α =
Слайд 16*
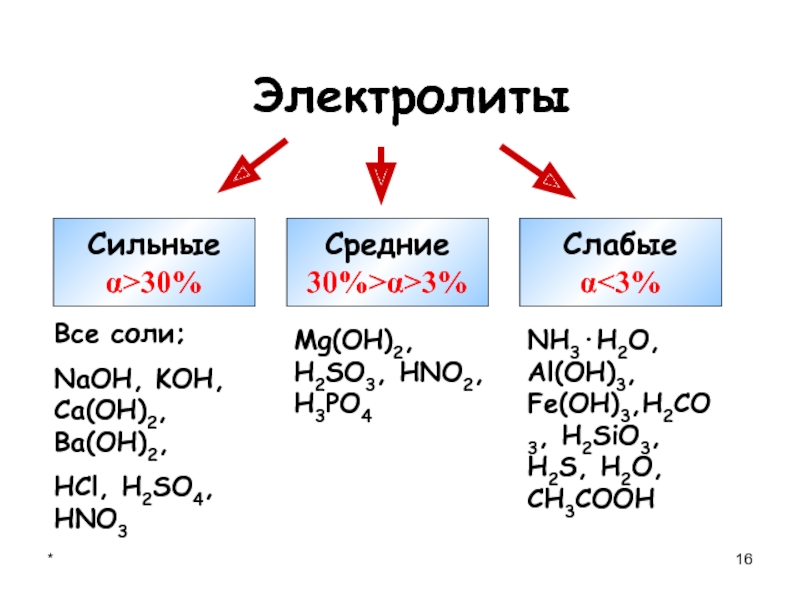
Электролиты
Сильные
α>30%
Средние
30%>α>3%
Слабые
α
HCl, H2SO4, HNO3
Mg(OH)2, H2SO3, HNO2, H3PO4
NH3·H2O, Al(OH)3, Fe(OH)3,H2CO3, H2SiO3, H2S,
H2O, CH3COOHСлайд 18*
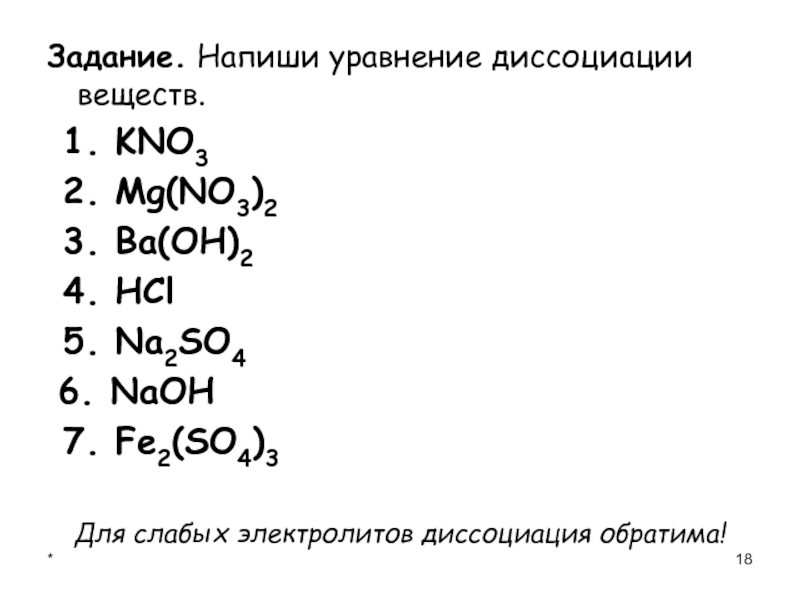
Задание. Напиши уравнение диссоциации веществ.
1. KNO3
2. Mg(NO3)2
3. Ba(OH)2
4. HCl
5. Na2SO4
6. NaOH
7.
Fe2(SO4)3Для слабых электролитов диссоциация обратима!
Слайд 19*
Что называют электролитической диссоциацией?
Какие вещества называют электролитами? Какие вещества к
ним относятся? Какой тип химической связи для них характерен?
Какие
вещества называют неэлектролитами? Какие вещества к ним относятся? Какой тип химической связи для них характерен?Каков механизм ЭД при растворении в воде веществ с ионной и ковалентной полярной связями?