Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Характеристика химического элемента – неметалла на основании его положения в Периодической системе химических элементов
Содержание
- 1. Характеристика химического элемента – неметалла на основании его положения в Периодической системе химических элементов
- 2. 1. Характеристика неметалла на примере азотаПоложение N
- 3. 1. Характеристика неметалла на примере азотаб) Состав
- 4. 1. Характеристика неметалла на примере азотав) строение
- 5. 1. Характеристика неметалла на примере азотаУ атома
- 6. 1. Характеристика неметалла на примере азотаЭлектроотрицательность –
- 7. 1. Характеристика неметалла на примере азота
- 8. 2. Сравнение свойств атома азота со свойствами
- 9. 3. Простое вещество азот – N2 –
- 10. 4. Высший оксид – N2O5Кислотный.Взаимодействует с ОснованиямиОсновными оксидамиводой
- 11. 4. Высший оксид – N2O5N2O5 + 2NaOH
- 12. 5. Высший гидроксид - HNO3 - кислотаВзаимодействует с ОснованиямиОсновными оксидамиСолямиметаллами
- 13. 5. Высший гидроксид - HNO3 - кислота2HNO3+Cu(OH)2
- 14. 6. NH3 - летучее водородное соединениеАммиак
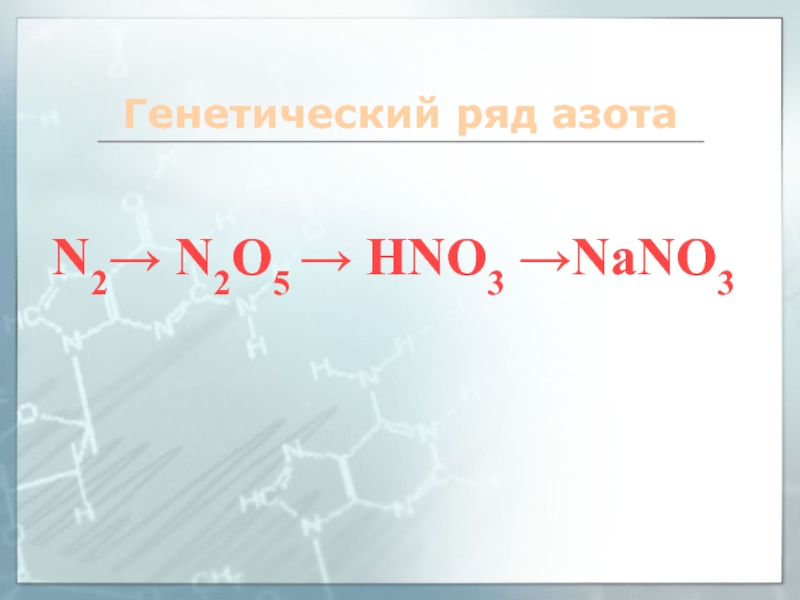
- 15. Генетический ряд азотаN2→ N2O5 → HNO3 →NaNO3
- 16. Закрепление знаний . Тестирование1. Заряд ядра атома
- 17. 2. В ряду химических элементов B→C→Nа)усиливаются металлические
- 18. 3. Значения высшей и низшей степеней окисления
- 19. 4. С образованием катионов водорода и анионов
- 20. 5. При взаимодействии с водой образует кислотуа)Na2O2б)N2O5в)NOг)NH3
- 21. Скачать презентанцию
1. Характеристика неметалла на примере азотаПоложение N в Периодической системе и строение его атомаа) Положение N в Периодической системе N порядковый номер – 7
Слайды и текст этой презентации
Слайд 1Урок 2. Характеристика химического элемента – неметалла на основании его
положения в Периодической системе химических элементов
Слайд 21. Характеристика неметалла на примере азота
Положение N в Периодической системе
и строение его атома
а) Положение N в Периодической системе
N
порядковый номер – 72 (малый) период, V группа, главная подгруппа
Слайд 31. Характеристика неметалла на примере азота
б) Состав атома
P+ = 7
(порядковый номер)
ē = P+ = 7
n0 = Ar - №
= 14-7=7Слайд 41. Характеристика неметалла на примере азота
в) строение атома N:
Число энергетических
уровней = номеру периода = 2
Число ē на последнем уровне
= номеру группы, в котором находится элемент, т.е. 5.N+7 )) 1s2 2s2 2p3
2 5
2
2
3
Слайд 51. Характеристика неметалла на примере азота
У атома азота на внешнем
электронном слое
находится 5 электронов, до завершения не хватает
3 электрона (8-5),
атом азота может и принимать, и отдавать электроны в химических реакциях, проявляя как окислительные, так и восстановительные свойства.
N0 + 3 ē → N-3 (восстановление, окисилитель)
N0 - 5ē→N+5 (окисление, восстановитель)
Слайд 61. Характеристика неметалла на примере азота
Электроотрицательность – способность атомов химических
элементов оттягивать к себе электроны атомов.
Самый электроотрицательный элемент- F, затем
O, затем N. Азот – третий по электроотрицательности элемент.
Слайд 82. Сравнение свойств атома азота со свойствами атомов – соседей
по группе и периоду
R АТ (N) < R АТ (P)
Азот
– самый сильный окислитель в V группе.R АТ (С) > R АТ (N) > R АТ (O)
Атомы азота проявляют более сильные окислительные свойства, т.к. обладают:
а) меньшим R ат , чем атомы С
б) и большим числом ē
Но азот менее сильный окислитель, чем кислород.
Слайд 93. Простое вещество азот – N2 – неметалл
N2 - к.н.п,
газ.
Неметаллические свойства простого вещества азота выражены сильнее, чем у фосфора.
Неметаллические
свойства простого вещества азота выражены сильнее, чем у углерода, но слабее, чем у простого вещества укислорода.Слайд 114. Высший оксид – N2O5
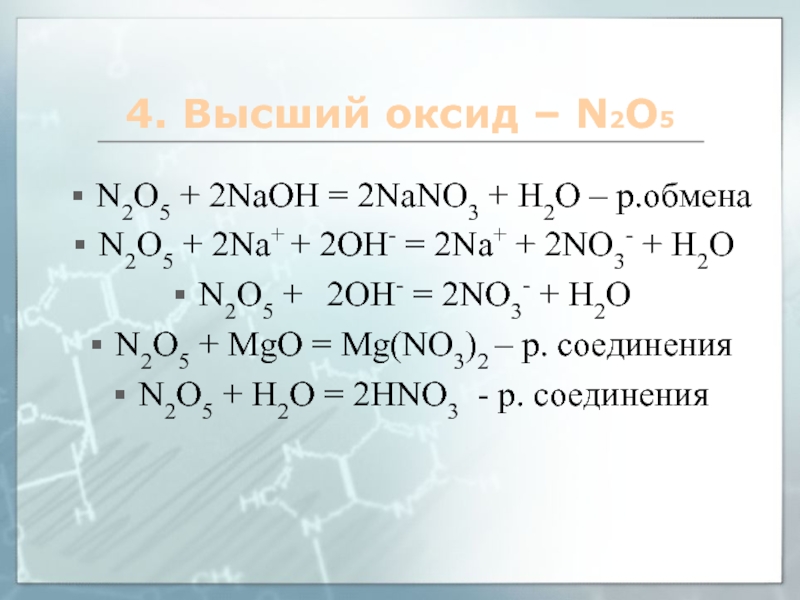
N2O5 + 2NaOH = 2NaNO3 +
H2O – р.обмена
N2O5 + 2Na+ + 2OH- = 2Na+ +
2NO3- + H2O N2O5 + 2OH- = 2NO3- + H2O
N2O5 + MgO = Mg(NO3)2 – р. соединения
N2O5 + Н2О = 2HNO3 - р. соединения
Слайд 125. Высший гидроксид - HNO3 - кислота
Взаимодействует с
Основаниями
Основными оксидами
Солями
металлами
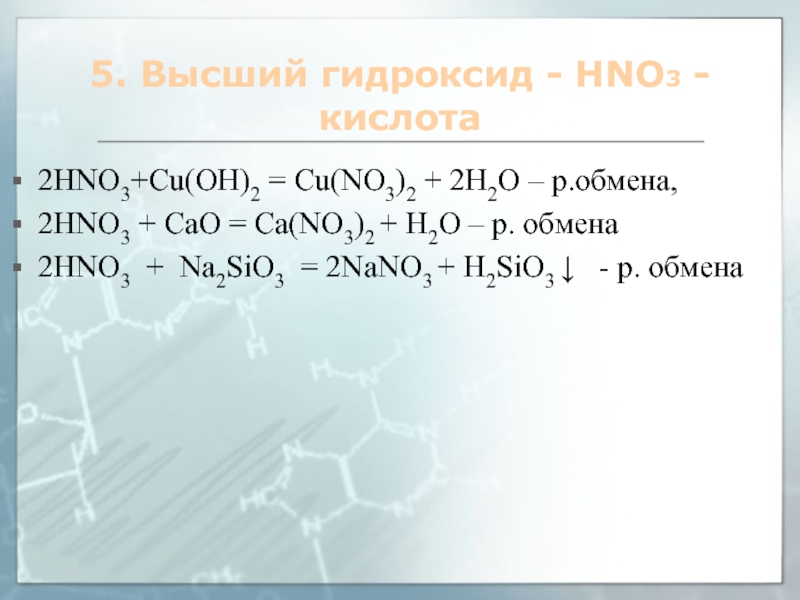
Слайд 135. Высший гидроксид - HNO3 - кислота
2HNO3+Cu(OH)2 = Cu(NO3)2 +
2H2O – р.обмена,
2HNO3 + СaO = Ca(NO3)2 + H2O –
р. обмена2HNO3 + Na2SiO3 = 2NaNO3 + H2SiO3 ↓ - р. обмена
Слайд 16Закрепление знаний . Тестирование
1. Заряд ядра атома азота равен числу
а)
протонов
б)электронов во внешнем электронном слое
в) нейтронов
г)энергетических уровней
Слайд 17
2. В ряду химических элементов B→C→N
а)усиливаются металлические свойства
б)ослабевают восстановительные свойства
в)уменьшается
электроотрицательность атомов
г)уменьшается высшая степень окисления в оксидах
Слайд 18
3. Значения высшей и низшей степеней окисления азота соответственно равны
а)
+5 и -3
б) +4 и +1
в)+5 и 0
г)+4 и 0
Слайд 19
4. С образованием катионов водорода и анионов кислотного остатка диссоциирует
а)оксид
кремния (IV)
б) оксид меди (II)
в)гидроксид натрия
г)азотная кислота
Теги