Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Бактерии в геохимических круговоротах
Содержание
- 1. Бактерии в геохимических круговоротах
- 2. Химический элемент + электроны восстановление. Химический
- 3. Схема трансформации серных соединений
- 4. Описания новых официально утвержденных (валидных) видов и
- 5. «…количество валидных родов (Genera) и видов (Species).»А.С.
- 6. Скорость восстанов-ления сульфатов, мкг S/г ила-сутки, в
- 7. Скорость восстановления сульфатов, мкг S/г ила-сутки, в
- 8. Зависимость интенсивности сульфатредукции в поверхностных илах Азовского
- 9. Расчетное распределение органического углерода в Черном море
- 10. Слайд 10
- 11. Сульфатредукция: восстановление сульфатной серы до сероводорода, сопряженное
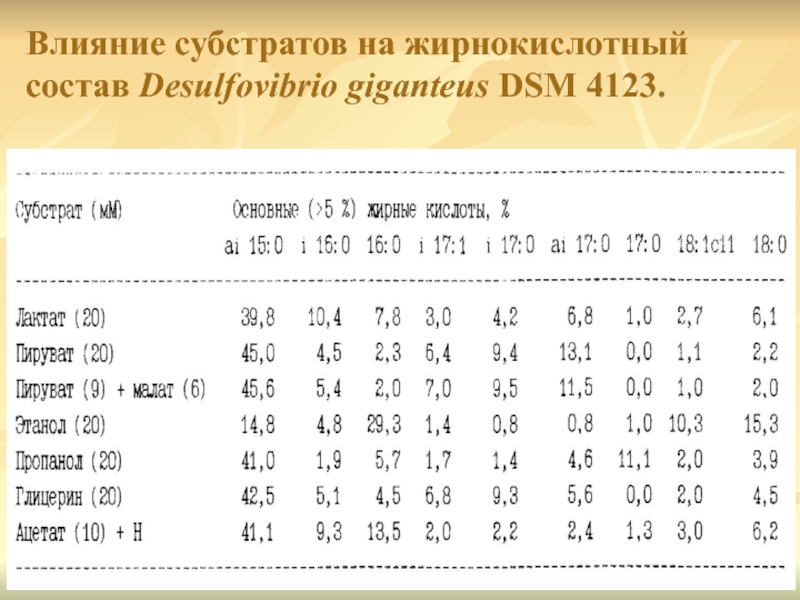
- 12. Влияние субстратов на жирнокислотный состав Desulfovibrio giganteus DSM 4123.
- 13. Первая культура сульфатредуцирующих бактерий была выделена в
- 14. Почему на сульфатредукторов обратили внимание в Нидерландах?
- 15. Слайд 15
- 16. Слайд 16
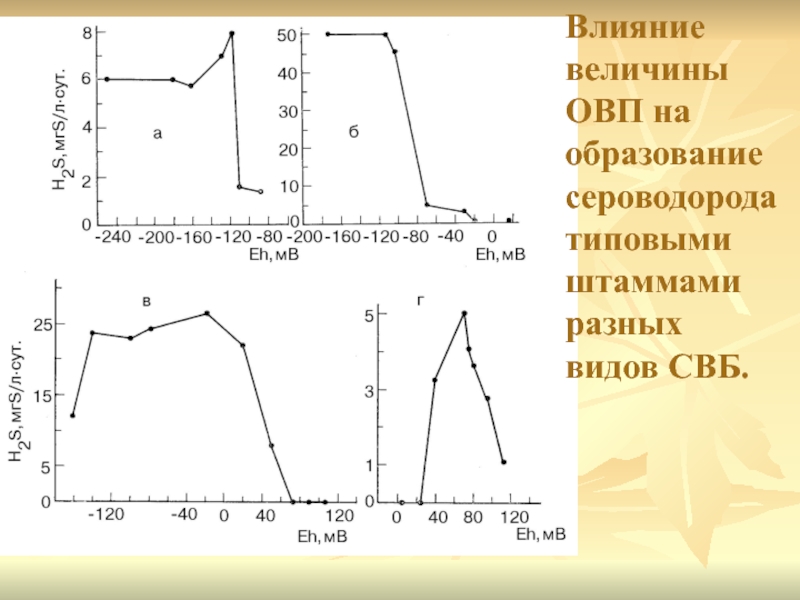
- 17. Влияние величины ОВП на образование сероводорода типовыми штаммами разных видов СВБ.
- 18. Схема трансформации серных соединений
- 19. Интенсивность сульфатредукции в водной толще озера Черный Кичиер и Черного моря
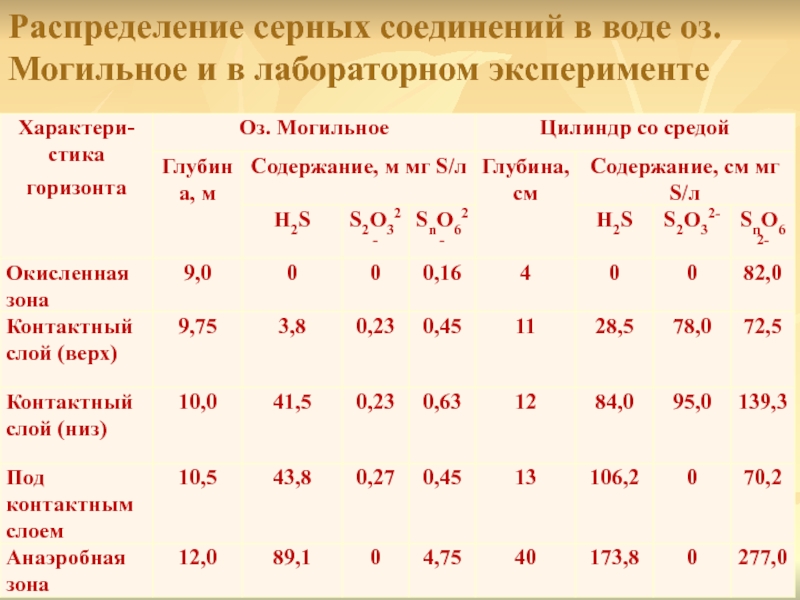
- 20. Распределение серных соединений в воде оз. Могильное и в лабораторном эксперименте
- 21. Лет 20 назад была попытка разведения мидий
- 22. Происхождение Черноморского сероводорода1-я гипотеза: гнилостный. 2-я: сульфатредукционный.
- 23. Слайд 23
- 24. Образование метана культурой Desulfosarcina variabilis ВКМ В-1167 при росте на различных субстратах
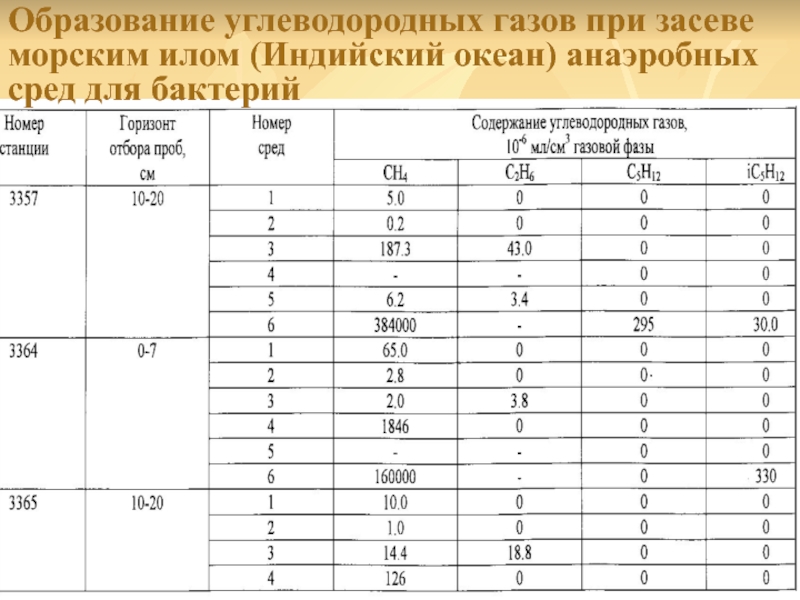
- 25. Образование углеводородных газов при засеве морским илом (Индийский океан) анаэробных сред для бактерий
- 26. Образование нанноклетки и нанноформ у СВБ. Desulfomicrobium
- 27. Бактерии в геохимических круговоротах Биовыщелачивание тионовыми бактериямии участие микроорганизмов в круговороте серы
- 28. Классический метод добычи ценных металлов из руд
- 29. Проблемы биовыщелачивания ацидофилами: внесение серной кислотыОсновные добавки
- 30. Мы исследовали 16S рДНК бактерий из образцов
- 31. Доминирующие группы бактерий в отвалах канадских руд
- 32. Бактериальные сообщества из рудных отвалов в накопительных
- 33. Филогенетический анализ 16S рДНК накопительных культур привел
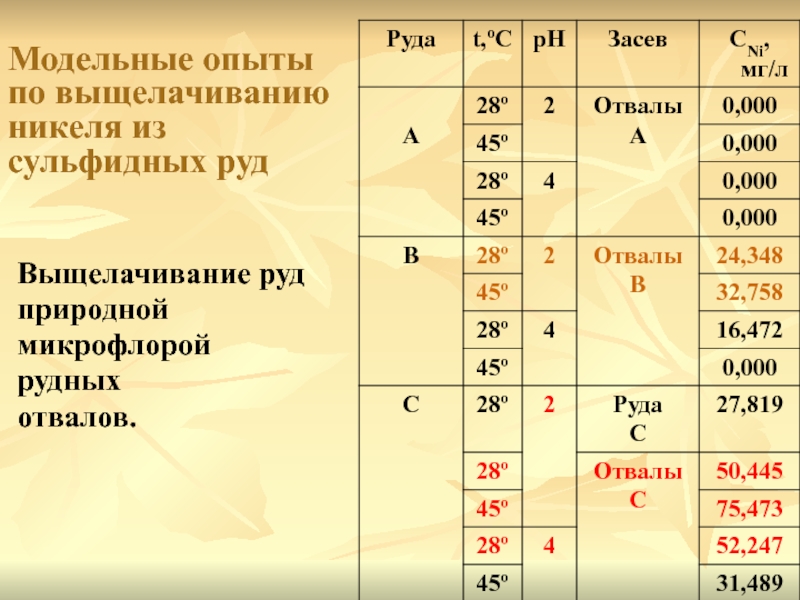
- 34. Модельные опыты по выщелачиванию никеля из сульфидных рудВыщелачивание рудприродной микрофлорой рудных отвалов.
- 35. BioHeap Ltd - австралийская компания, специализируется в
- 36. Сравнительное выщелачивание никеля из образцов сульфидных руд
- 37. Сравнительное выщелачивание никеля культурой бактерий Halothiobacillus halophilus DSM 6132 и природной микрофлорой
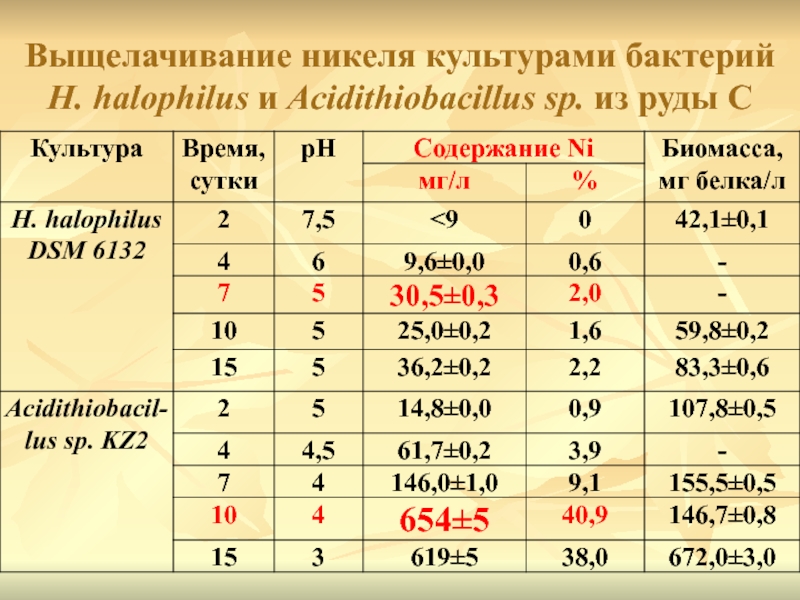
- 38. Выщелачивание никеля культурами бактерий H. halophilus и Acidithiobacillus sp. из руды C
- 39. Основной итог завершенного проекта МНТЦЗамена кислотолюбивых штаммов
- 40. J. T. Pronk, W. M. Meijer, W.
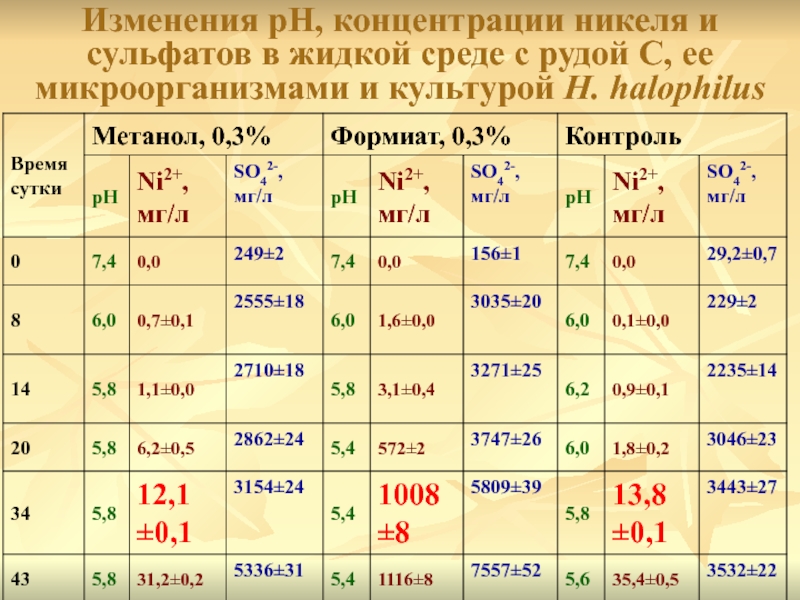
- 41. Изменения рН, концентрации никеля и сульфатов в
- 42. Тионовые бактерии способны не только окислять
- 43. Коррозия бетона за счет образования сульфата
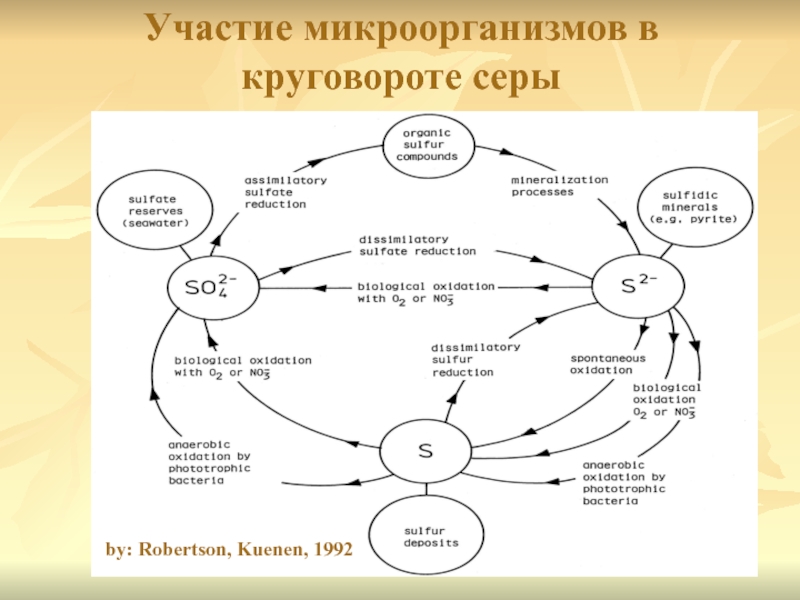
- 44. Участие микроорганизмов в круговороте серыby: Robertson, Kuenen, 1992
- 45. Осаждение тяжелых металлов сульфатвосстанавливающими бактериями
- 46. rH2 = Eh / 0,029 + 2 рН
- 47. Слайд 47
- 48. Слайд 48
- 49. Скачать презентанцию
Слайды и текст этой презентации
Слайд 1
Бактерии в геохимических круговоротах
ПущГЕНИ
М.Б. Вайнштейн
30 сентября 2019
Круговорот серы. Ассимиляторное и
Слайд 2Химический элемент + электроны восстановление.
Химический элемент - электроны
окисление.
Сульфат (S 6+) + 8 электронов
сульфид
(S 2-). Слайд 4Описания новых официально утвержденных (валидных) видов и родов сульфатвосстанавли-вающих бактерий.
По оси абцисс - годы, по оси ординат количество валидных
родов (Genera) и видов (Species).Слайд 5«…количество валидных родов (Genera) и видов (Species).»
А.С. Пушкин «Капитанская дочка»
– капитан Миронов и его инвалиды.
Кто такие инвалиды?
Вопрос
1. Что означает «валидный род / вид»?
Вопрос 2.
Где в природе много доступных бактериям сульфатов?
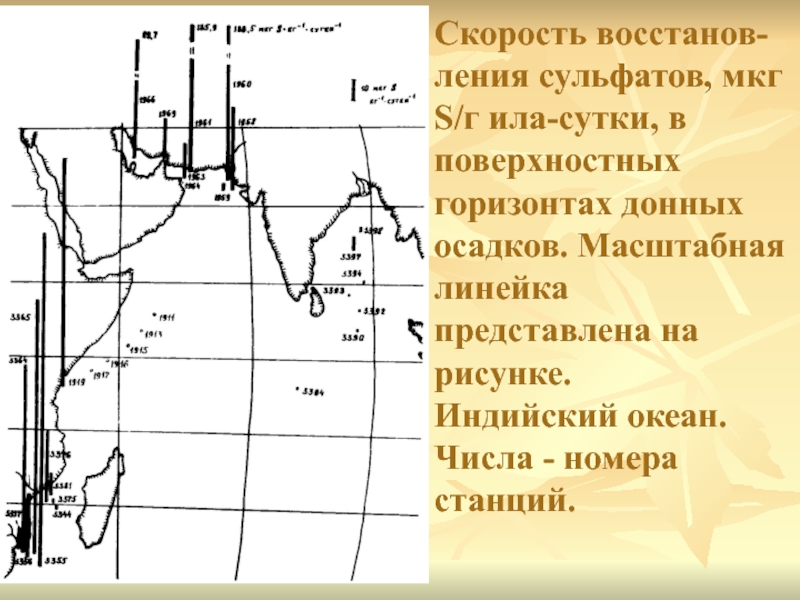
Слайд 6Скорость восстанов-ления сульфатов, мкг S/г ила-сутки, в поверхностных горизонтах донных
осадков. Масштабная линейка представлена на рисунке.
Индийский океан. Числа -
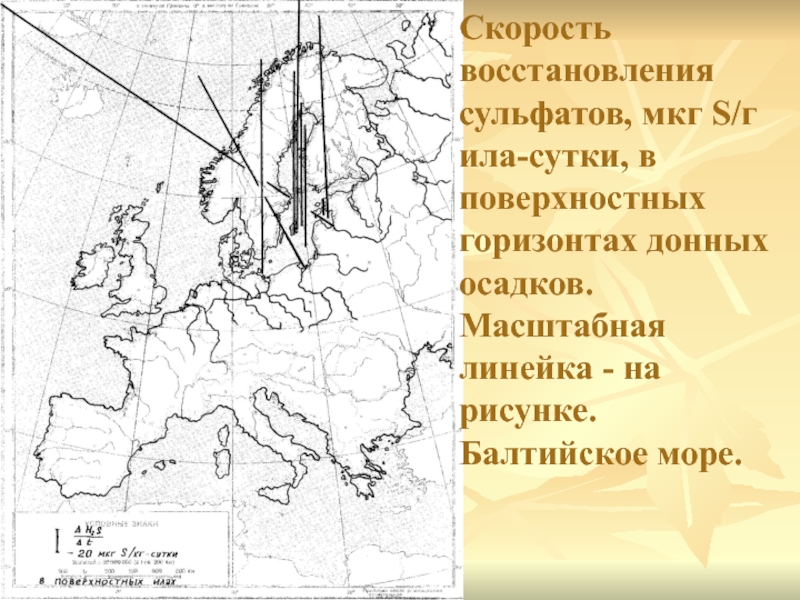
номера станций. Слайд 7Скорость восстановления сульфатов, мкг S/г ила-сутки, в поверхностных горизонтах донных
осадков. Масштабная линейка - на рисунке. Балтийское море.
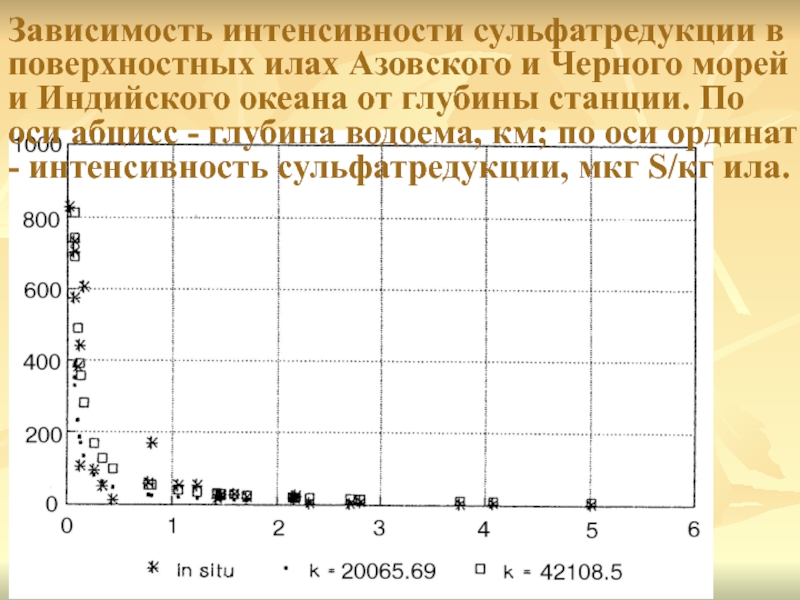
Слайд 8Зависимость интенсивности сульфатредукции в поверхностных илах Азовского и Черного морей
и Индийского океана от глубины станции. По оси абцисс -
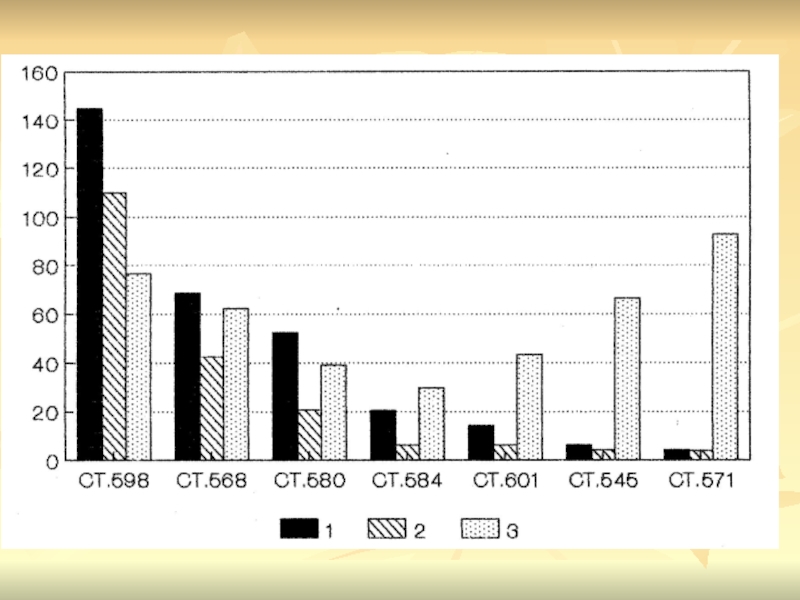
глубина водоема, км; по оси ординат - интенсивность сульфатредукции, мкг S/кг ила.Слайд 9Расчетное распределение органического углерода в Черном море по разрезу "берег-батиаль".
На оси абцисс указаны номера станций, приведенные в порядке увеличения
глубины.1 – исходное содержание органического вещества, кг с/м2;
2 – расчетное потребление органического вещества на сульфатредукцию, кг с/м2;
3 – расчетное потребление органического вещества на сульфатредукцию, %.
Слайд 11Сульфатредукция: восстановление
сульфатной серы до сероводорода,
сопряженное с
окислением
углеводов
до карбонатов
(«полное
окисление»).
Вайнштейн М.Б.
Вопрос:
Что такое «полное» и
«неполное» окисления? И почему Джон Постгейт обиделся, когда Фридрих Виддель назвал бактерию в его честь?
Слайд 21Лет 20 назад была попытка разведения мидий под Одессой –
вроде устричных плантаций, - однако, случился сероводородный замор, и всё
хозяйство погибло. Тогда это трактовалось как подъем глубинных сероводородных вод Черного моря и вызвало ряд журналистских статей о том, что сероводород начал подниматься из глубин Черного моря и скоро достигнет поверхности и отравит все живое!Вопрос:
Каковы основные причины этого замора?
Слайд 22Происхождение Черноморского сероводорода
1-я гипотеза: гнилостный.
2-я: сульфатредукционный.
3-я: древний, поступающий
по разломам.
Методы проверки:
расчетный химический по балансу,
расчетный химический по соотношению «сульфат : хлорид», изотопный,
подтверждение современного процесса,
подтверждение присутствия бактерий.
Слайд 24Образование метана культурой Desulfosarcina variabilis ВКМ В-1167 при росте на
различных субстратах
Слайд 25Образование углеводородных газов при засеве морским илом (Индийский океан) анаэробных
сред для бактерий
Слайд 26Образование нанноклетки и нанноформ у СВБ. Desulfomicrobium baculatum ВКМ В-1378
после обработки ВЧ (600 МГц, 10 мин): нанноклетка имеет сферическую
форму.Слайд 27Бактерии в геохимических круговоротах
Биовыщелачивание тионовыми бактериями
и участие микроорганизмов в
круговороте серы
Слайд 28Классический метод добычи ценных металлов из руд – пирометаллургия –
выплавка при высокой температуре. Этот метод непригоден, если содержание металла
не более 1%.При низких содержаниях металлов их добывают растворением из руд – гидрометаллургия. Минеральное сырье практически нерастворимо в воде, поэтому требуется разрушение основной структуры минералов или хелатирование металлов.
Первый в мире патент на биовыщелачивание (выщелачивание растворами с использованием бактерий) был выдан в США в 1958 г.
Наиболее востребованными оказались тионовые бактерии, используемые для добычи ценных металлов из сульфидных руд.
Классические виды тионовых бактерий автотрофны, то есть не нуждаются в добавлении дополнительных ростовых субстратов в руду, и используют энергию окисления сульфидов – компонентов минерального сырья руды.
Слайд 29Проблемы биовыщелачивания ацидофилами: внесение серной кислоты
Основные добавки для химического выщелачивания
- минеральные кислоты, из которых предпочтение обычно отдается серной как
сильной и нелетучей даже при разогреве. Например, по патенту США 4,098,870 (1978) для выщелачивания железо-никелевой руды вносят серную кислоту из расчета 0,8 на 1 часть сухой руды.Внесение кислоты
разрушает/растворяет некоторые минералы,
способствует окислению минеральных сульфидов,
создает благоприятные условия для строгих ацидофилов.
Вместе с этим внесение серной кислоты экономически невыгодно:
увеличивает себестоимость металла за счет цены кислоты,
требует затрат на последующую ремедиацию закисленного участка.
По заказу CANMET-Mining and Mineral Sciences Laboratories, Канада, мы получили грант МНТЦ на выполнение проекта «Выщелачивание никелевых руд умеренными ацидофилами».
Слайд 30Мы исследовали 16S рДНК бактерий из образцов трех видов отвалов
(хвостов) канадской никелевой руды c нейтральными значениями рН. Все варианты
схожи по составу бактериальных сообществ: в них преобладали неизвестные и некультивируемые на стандартных средах виды Acidithiobacillus.Слайд 31Доминирующие группы бактерий в отвалах канадских руд
В соответствии
с определенной величиной сходства ≥97% найденных бактериальных последовательностей с известными
в базе данных GenBank 39 полученных нами клонов были идентифицированы как представители Acidithiobacillus, Leptospirillum, Halothiobacillus и Pseudomonas. Наиболее широко был представлен род Aciditiobacillus.В целом доминирование в бактериальном разнообразии микробиот может быть представлено по следующей схеме в порядке убывания: Acidithiobacillus > Leptospirillum > Halothiobacillus > Thiomonas > Pseudomonas > Delftia.
Слайд 32Бактериальные сообщества из рудных отвалов в накопительных культурах
В экспериментах по
выщелачиванию накопительные культуры, засеянные образцами инкубировали при различных условиях: A1
– pH 2, 28 оC; A2 – pH 4, 28 оC; A3 – pH 2, 45 оC; A4 – pH 4, 45 оC; B1 – рH 2, 28 оC; B2 – pH 4, 28 оC; B3 – pH 2, 45 оC; B4 – pH 4, 45 оC; C1 – pH 2, 28 оC; C2 – pH 4, 28 оC; C3 – pH 2, 45 оC; C4 – pH 4, 45 оC. A0 A1 A2 A3 A4 B0 B1 B2 B3 B4 C0 C1 C2 C3 C4
Буквами А, В и С обозначены образцы отвалов, A0, B0 и С0 – исходный состав микрофлоры образцов.
Слайд 33Филогенетический анализ 16S рДНК накопительных культур привел к тем же
результатам, что и анализ исходных отвалов руд: в культурах были
обнаружены многочисленные «некультивируемые» штаммы бактерий родов Acidithiobacillus, Leptospirillum и Halothiobacillus.Слайд 34Модельные опыты
по выщелачиванию
никеля из
сульфидных руд
Выщелачивание руд
природной
микрофлорой
рудных
отвалов.
Слайд 35BioHeap Ltd - австралийская компания, специализируется в бактериальном кучном выщелачивании
на протяжении 10 лет (более 10 миллион дол. США)
Слайд 36Сравнительное выщелачивание никеля из образцов сульфидных руд культурами тионовых бактерий:
-
Acidithiobacillus thiooxidans NCIMB 8342,
Thiobacillus concretivorus (A. thiooxidans) NCIMB
8345, Acidithiobacillus albertensis DSM 14366,
Thiobacillus denitrificans DSM 12475,
Halothiobacillus halophilus DSM 6132
Слайд 37Сравнительное выщелачивание никеля культурой бактерий Halothiobacillus halophilus DSM 6132 и
природной микрофлорой
Слайд 39Основной итог завершенного проекта МНТЦ
Замена кислотолюбивых штаммов микроорганизмов на умеренные
позволит отказаться от применения серной кислоты, уменьшить себестоимость и расходы
на восстановление закисленного грунта.Применение умеренно кислотолюбивых штаммов на первом этапе позволяет использовать более кислотолюбивые на втором без дополнительного внесения серной кислоты и без образования мешающих выходу ценных металлов окислов железа.
Слайд 40J. T. Pronk, W. M. Meijer, W. Hazeu, J. P.
Van Dijken, P. Bos, and J. G. Kuenen Growth of
Thiobacillus ferrooxidans on Formic Acid Applied аnd Environmental Microbiology 1991, V. 57, № 7, pр. 2057-2062«… Thiobacillus ferrooxidans ATCC 21834, which, however, could not grow on formate in normal batch cultures. However, the organism could be grown on formate when the substrate supply was growth limiting, e.g., in formate-limited chemostat cultures. The cell densities achieved by the use of the latter cultivation method were higher than cell densities reported for growth of T. ferrooxidans on ferrous iron or reduced sulfur compounds. Inhibition of formate oxidation by cell suspensions, but not cell extracts, of formate-grown T. ferrooxidans occurred at formate concentrations above 100 mM. This observation explains the inability of the organism to grow on formate in batch cultures. Cells grown in formate-limited chemostat cultures retained the ability to oxidize ferrous iron at high rates. Ribulose 1,5-bisphosphate carboxylase activities in cell extracts indicated that T. ferrooxidans employs the Calvin cycle for carbon assimilation during growth on formate. Oxidation of formate by cell extracts was NAD(P) independent.»