Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Химические компоненты клетки. Неорганические компоненты
Содержание
- 1. Химические компоненты клетки. Неорганические компоненты
- 2. «Химия» - в основе живого
- 3. Слайд 3
- 4. Биоэлементами обычно называют элементы, необходимые живым организмам
- 5. Это деление относительно условно, количественные критерии
- 6. Слайд 6
- 7. Слайд 7
- 8. Молекула воды состоит из атома О, связанного
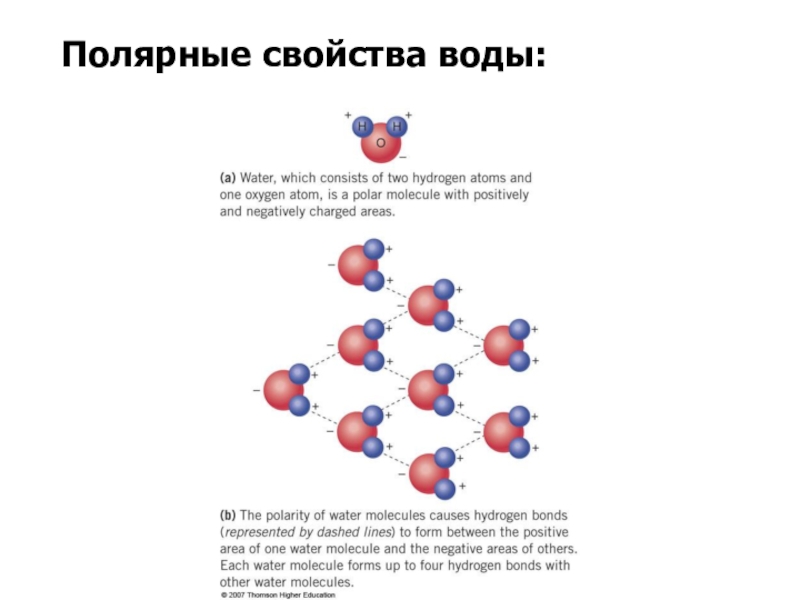
- 9. Полярные свойства воды:
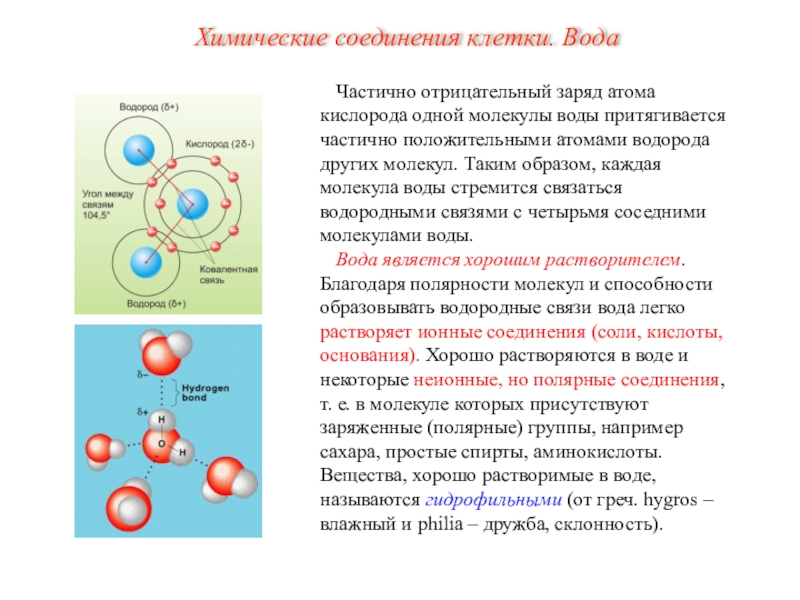
- 10. Частично отрицательный заряд атома кислорода одной молекулы
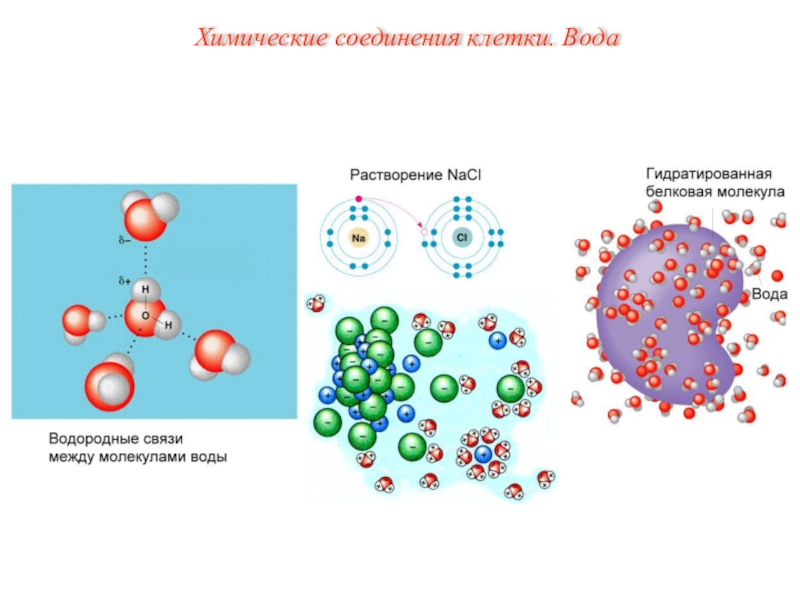
- 11. Химические соединения клетки. Вода
- 12. Вещества, плохо или вовсе нерастворимые в воде,
- 13. Вода обладает высокой теплоемкостью, т. е. способностью
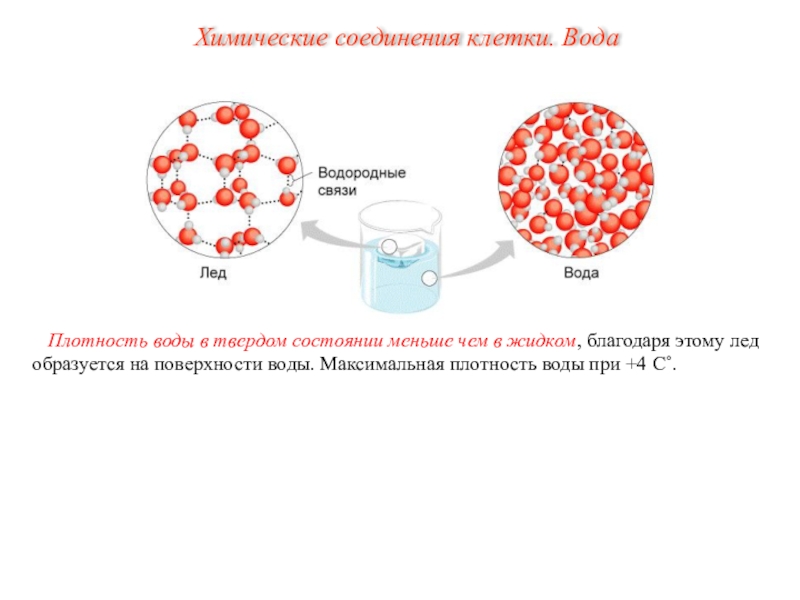
- 14. Плотность воды в твердом состоянии меньше чем
- 15. Важнейшие катионыК+, Na+, Ca2+ и др.Данные катионы
- 16. Важнейшие анионы: Н2РО4-, НРО42-, НСО3-, Сl-Буферность –
- 17. Буферность клетки: способность поддерживать стабильный уровень рН
- 18. Скачать презентанцию
Слайды и текст этой презентации
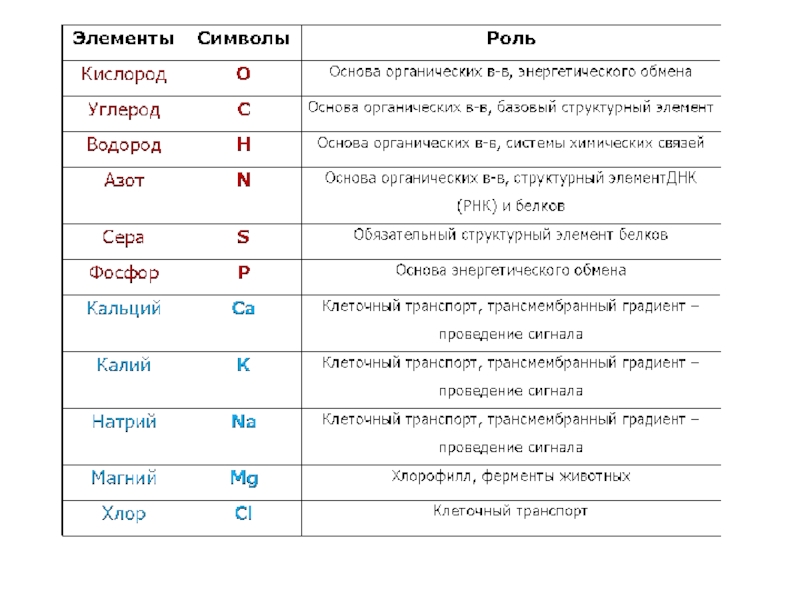
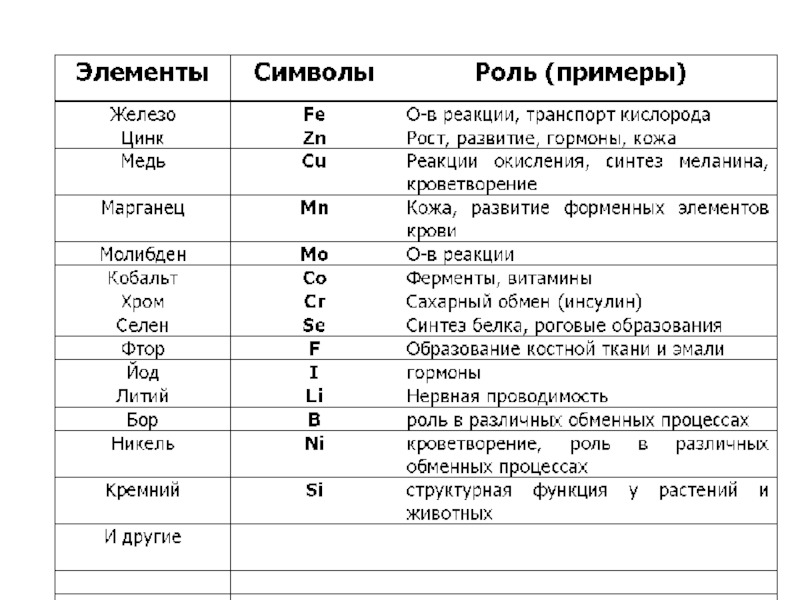
Слайд 4Биоэлементами обычно называют элементы, необходимые живым организмам для обеспечения нормальной
жизнедеятельности.
Часто их подразделяют на макроэлементы и микроэлементы.
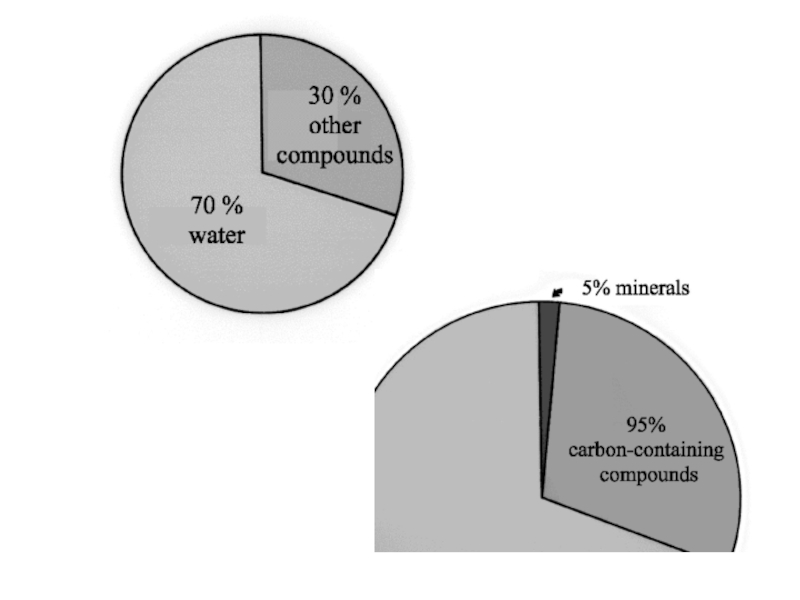
Слайд 5 Это деление относительно условно, количественные критерии можно определять по-разному. Например,
существует такая градация: макроэлементы – элементы, содержание которых в живых
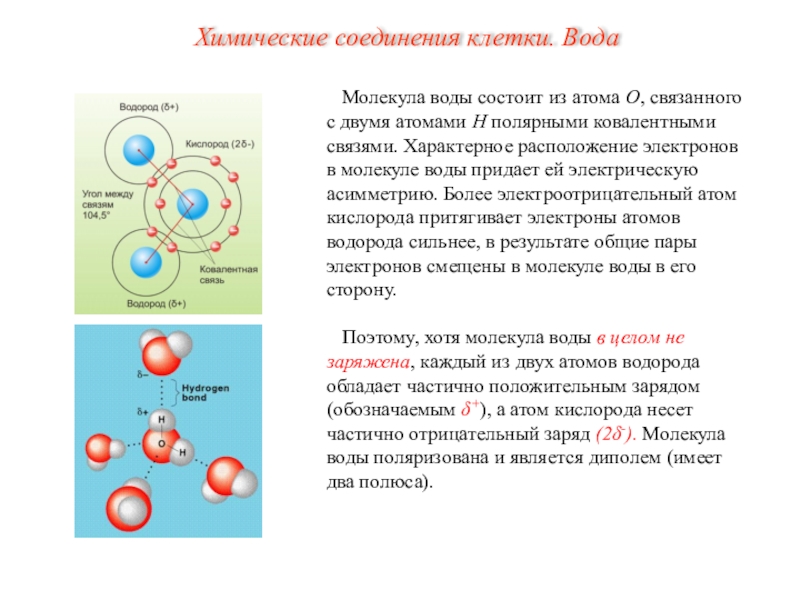
организмах составляет больше 0,001 %, микроэлементы - содержание которых менее 0,001 %. С учетом разных подходов к термину всегда точно макроэлементами окажутся О, С, N, Н (хотя в отечественной медицине принято их вообще не рассматривать, а макроэлементами считают Ca, K, P, Mg). Вместе с P и S они представляют группу из 6 базовых биоэлементов, присущих ВСЕМ организмам в относительно большом количестве в качестве структурной основы. Ca, K, Na, Mg, Cl являются также необходимыми элементами для большинства процессов жизнедеятельности. Множество других микроэлементов может присутствовать в очень маленьком количестве и играть важную роль в отдельно взятых процессах у определенных групп организмов.Слайд 8Молекула воды состоит из атома О, связанного с двумя атомами
Н полярными ковалентными связями. Характерное расположение электронов в молекуле воды
придает ей электрическую асимметрию. Более электроотрицательный атом кислорода притягивает электроны атомов водорода сильнее, в результате общие пары электронов смещены в молекуле воды в его сторону.Поэтому, хотя молекула воды в целом не заряжена, каждый из двух атомов водорода обладает частично положительным зарядом (обозначаемым δ+), а атом кислорода несет частично отрицательный заряд (2δ-). Молекула воды поляризована и является диполем (имеет два полюса).
Химические соединения клетки. Вода
Слайд 10Частично отрицательный заряд атома кислорода одной молекулы воды притягивается частично
положительными атомами водорода других молекул. Таким образом, каждая молекула воды
стремится связаться водородными связями с четырьмя соседними молекулами воды.Вода является хорошим растворителем. Благодаря полярности молекул и способности образовывать водородные связи вода легко растворяет ионные соединения (соли, кислоты, основания). Хорошо растворяются в воде и некоторые неионные, но полярные соединения, т. е. в молекуле которых присутствуют заряженные (полярные) группы, например сахара, простые спирты, аминокислоты. Вещества, хорошо растворимые в воде, называются гидрофильными (от греч. hygros – влажный и philia – дружба, склонность).
Химические соединения клетки. Вода
Слайд 12Вещества, плохо или вовсе нерастворимые в воде, называются гидрофобными (от
греч. phobos – страх). К ним относятся жиры, некоторые белки.
Такие вещества могут образовывать с водой поверхности раздела, на которых протекают многие химические реакции.Следовательно, тот факт, что вода не растворяет неполярные вещества, для живых организмов также очень важен. К числу важных в физиологическом отношении свойств воды относится ее способность растворять газы (О2, СО2 и др.).
Химические соединения клетки. Вода
Слайд 13Вода обладает высокой теплоемкостью, т. е. способностью поглощать тепловую энергию
при минимальном повышении собственной температуры. Большая теплоемкость воды защищает ткани
организма от быстрого и сильного повышения температуры.Вода обладает также высокой теплопроводностью, обеспечивая равномерное распределение тепла по всему организму. Следовательно, высокая удельная теплоемкость и высокая теплопроводность делают воду идеальной жидкостью для поддержания теплового равновесия клетки и организма.
Вода практически не сжимается, создавая тургорное давление, определяя объем и упругость клеток и тканей. Так, именно гидростатический скелет поддерживает форму у круглых червей, медуз и других организмов.
Химические соединения клетки. Вода
Слайд 14Плотность воды в твердом состоянии меньше чем в жидком, благодаря
этому лед образуется на поверхности воды. Максимальная плотность воды при
+4 С˚.Химические соединения клетки. Вода
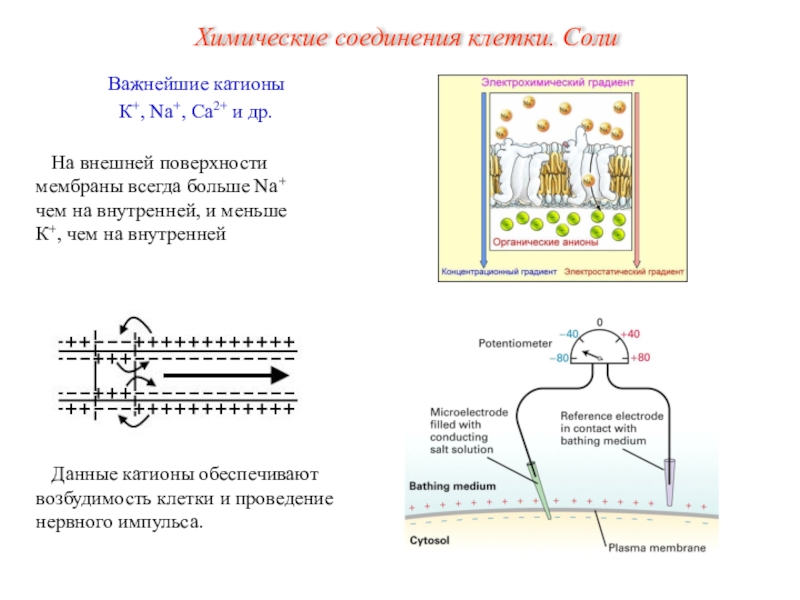
Слайд 15Важнейшие катионы
К+, Na+, Ca2+ и др.
Данные катионы обеспечивают возбудимость клетки
и проведение нервного импульса.
На внешней поверхности мембраны всегда больше Na+
чем на внутренней, и меньше К+, чем на внутреннейХимические соединения клетки. Соли
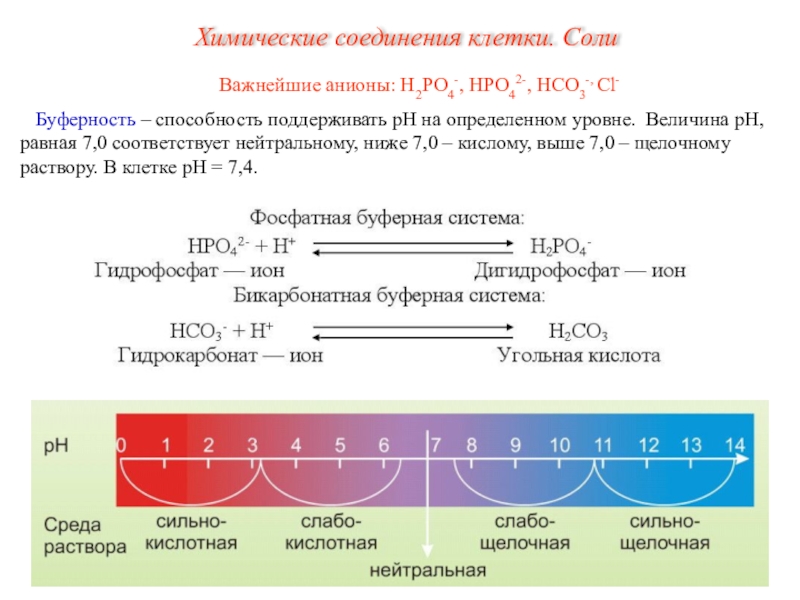
Слайд 16Важнейшие анионы: Н2РО4-, НРО42-, НСО3-, Сl-
Буферность – способность поддерживать рН
на определенном уровне. Величина рН, равная 7,0 соответствует нейтральному, ниже
7,0 – кислому, выше 7,0 – щелочному раствору. В клетке рН = 7,4.Химические соединения клетки. Соли
Слайд 17Буферность клетки:
способность поддерживать стабильный уровень рН несмотря на привнесение
небольшого количества кислот или щелочей. Обычно в клетке поддерживается слабощелочная
среда.Обеспечивается в основном анионами слабых кислот.