Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
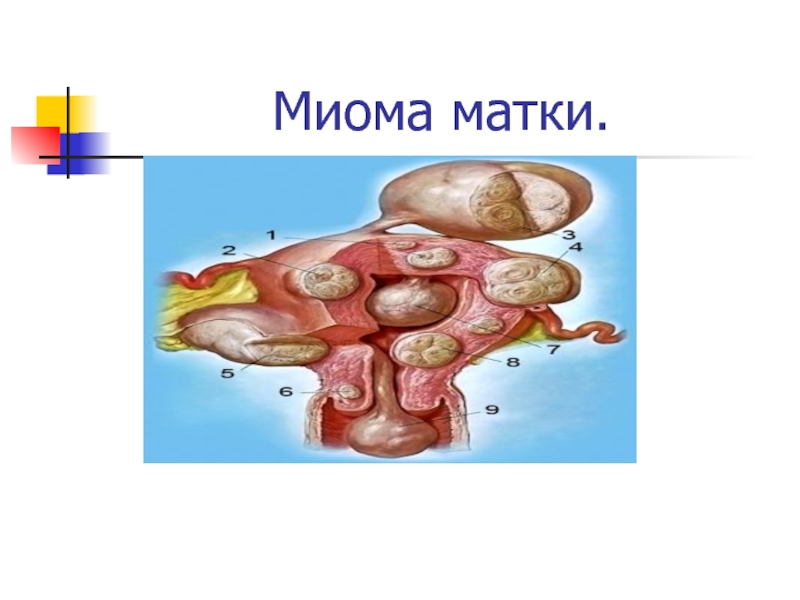
Миома матки
Содержание
- 1. Миома матки
- 2. Определение Миома матки (ММ) — моноклональный гормоночувствительный пролиферат, состоящий из фенотипически изменённых гладкомышечных клеток миометрия.
- 3. ПроисхождениеРастет из одной первичной клетки, которая в
- 4. Эпидемиология Миома
- 5. К основным факторам риска, способствующим возникновению миомы
- 6. Патогенез миомы маткиОпухолевый рост является следствием нарушения
- 7. Патогенез миомы маткиКлючевыми факторами патогенеза миомы матки
- 8. Патогенез миомы маткиВ последние годы основопологающее значение
- 9. Классификация По соотношению форменных элементов опухоли:
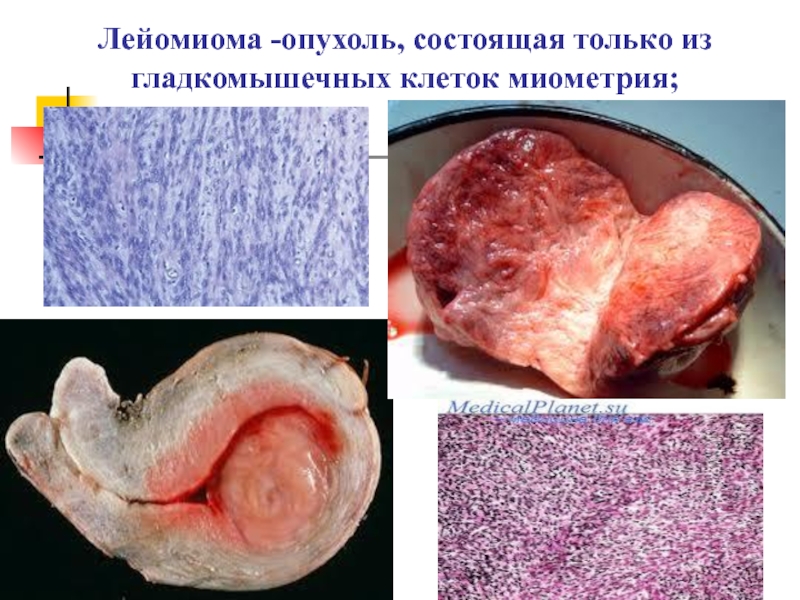
- 10. Лейомиома -опухоль, состоящая только из гладкомышечных клеток миометрия;
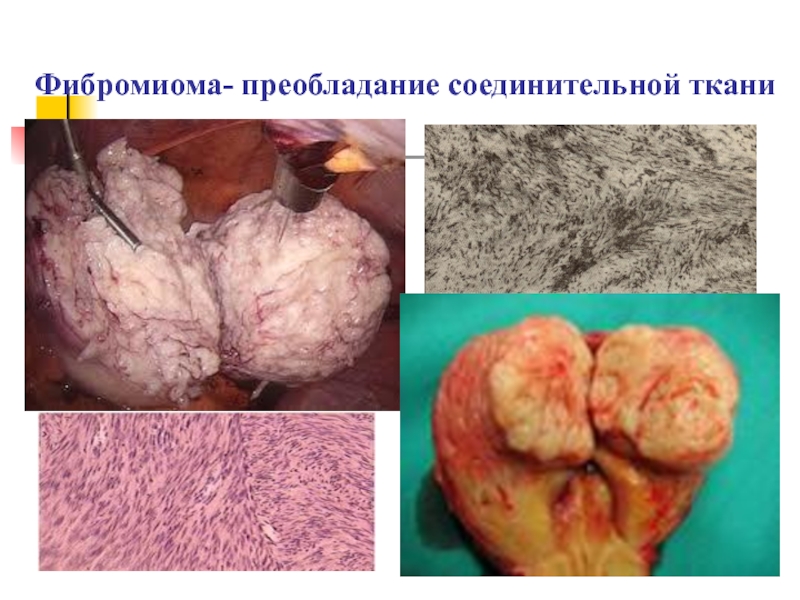
- 11. Фибромиома- преобладание соединительной ткани
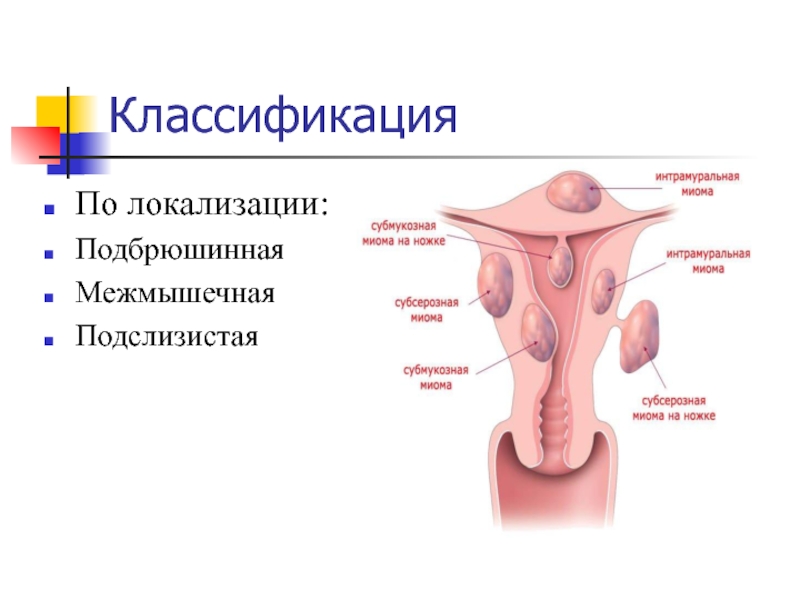
- 12. КлассификацияПо локализации:ПодбрюшиннаяМежмышечнаяПодслизистая
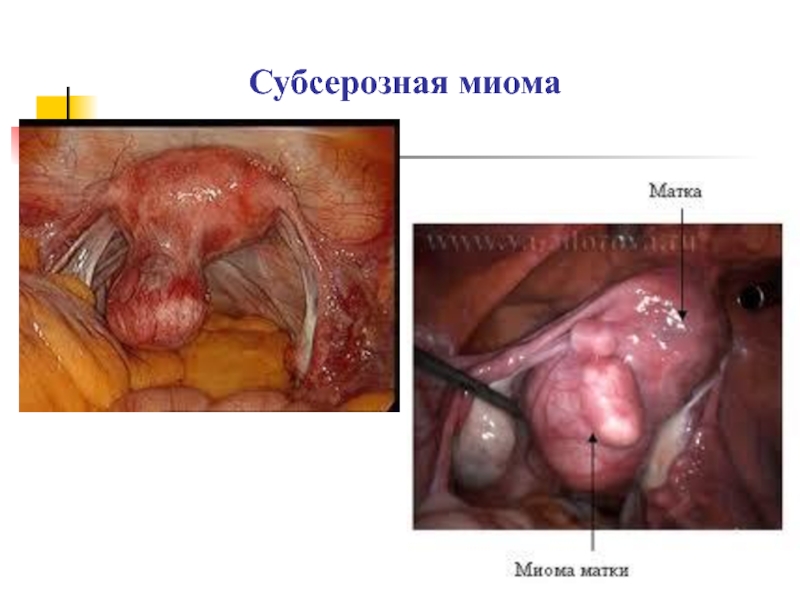
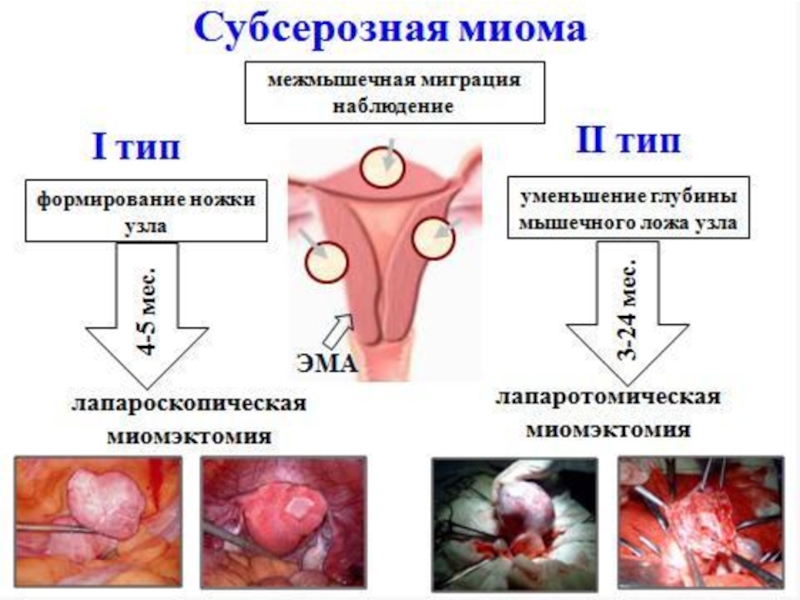
- 13. Субсерозная миома
- 14. По гистологическим особенностям: ПростаяВстречается в 75% случаевСтрома
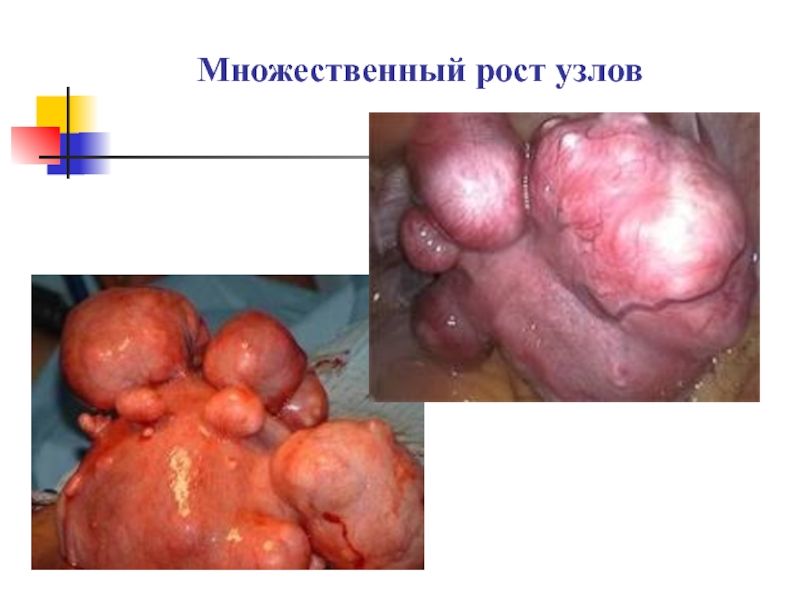
- 15. Множественный рост узлов
- 16. По клиническим проявлениям:симптомная миома матки (20-50% случаев)
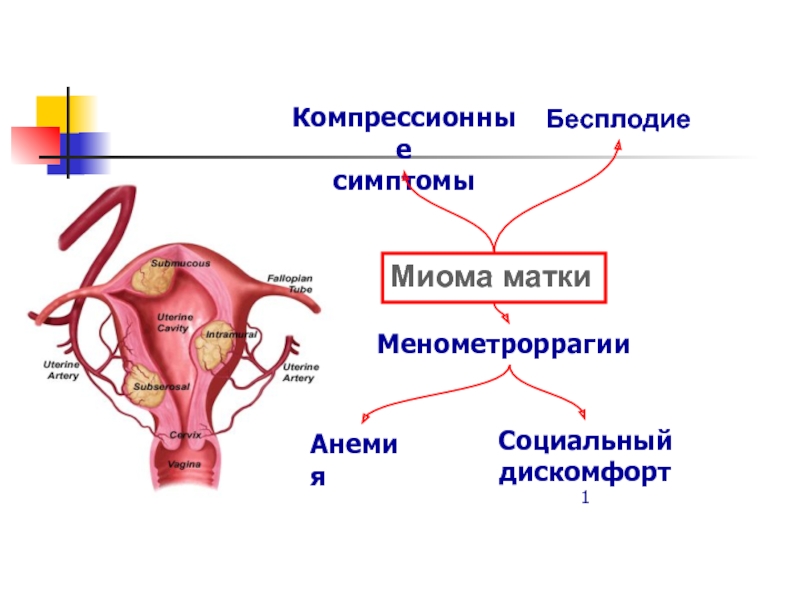
- 17. Миома матки, клиникаМиома маткиМенометроррагииАнемияСоциальный дискомфорт1Компрессионные симптомыБесплодие
- 18. ДиагностикаЖалобы: аномальные маточные кровотечения;тазовая боль;тяжесть внизу живота;увеличение живота;нарушение функции мочевого пузыря (дизурия);нарушение функции кишечника (дисхезия)бесплодие.
- 19. ДиагностикаАнамнез: отсутствие беременности и родов; раннее менархе,
- 20. Диагностика миомы маткиГинекологический осмотр позволяет обнаружить:-
- 21. Ультразвуковая диагностика подбрюшинной миомы матки. На эхограмме
- 22. Трансвагинальное ультразвуковое сканирование. Подбрюшинной миомы матки.
- 23. Допплерография и ангиографияПозволяют определить особенности кровообращения в
- 24. МРТ- признаки миомы маткиЧетко отчерченные образования, резко
- 25. Лапароскопическая картина миомы маткиУвеличенная в размерах матка
- 26. Лечение миомы матки
- 27. Лечение миомы маткиБ. радикальные операции:- гистерэктомия, применяемая
- 28. Показания к медикаментозному лечению миомы:величина опухоли, увеличивающая
- 29. ГонадотропиныДаназол, гестринонОбладают антиэстрогенным и антипрогестероновым эффектом, вызывая
- 30. Агонисты гонадотропин-рилизинг гормона (аГнРГ)Бусерелин, трипторелин, лейпрорелинБлокируют секрецию
- 31. АнтипрогестиныМифепристон Связывается с прогестероновыми рецепторами, блокируя их функциюГлавное
- 32. Показания к оперативному лечению: Большие размеры матки (более
- 33. Радикальное (ампутация матки) Включает гистерэктомию лапароскопическим и лапаротомическим
- 34. Лапароскопическая гистерэктомияОграничениями являются размер матки, превышающий 16-18
- 35. Постгистерэктомический синдромОбусловлен недостаточностью эстрогенов из-за снижения овариального
- 36. Слайд 36
- 37. Миомэктомия лапароскопическим доступомОсновным критерием эффективности миомэктомии следует
- 38. Эмболизация маточных артерийЭмболизация маточных артерий (ЭМА, эндоваскулярная эмболизация
- 39. Слайд 39
- 40. ЭМАЭмболизация маточных артерий выполняется :в специально оборудованной
- 41. ЭМАПервым этапом вмешательства является:пункция правой общей бедренной
- 42. ЭМА
- 43. ЭМАВ течение 12-18 мес происходит прогрессивное уменьшение
- 44. Фокусированная ультразвуковая абляция под контролем МРТСравнительно новый
- 45. ФУЗ-МРТПроводится базовое сканирование, врач намечает план операции.
- 46. ФУЗ-МРТ
- 47. ФУЗ-МРТ
- 48. ФУЗ-МРТ
- 49. Спасибо за внимание!
- 50. Скачать презентанцию
Определение Миома матки (ММ) — моноклональный гормоночувствительный пролиферат, состоящий из фенотипически изменённых гладкомышечных клеток миометрия.
Слайды и текст этой презентации
Слайд 2Определение
Миома матки (ММ) — моноклональный гормоночувствительный пролиферат, состоящий из фенотипически
изменённых гладкомышечных клеток миометрия.
Слайд 3Происхождение
Растет из одной первичной клетки, которая в результате произошедшей в
ней мутации приобрела способность нерегулируемого роста. Множественные узлы клонально не
связаны, что и объясняет различный темп роста.Слайд 4Эпидемиология
Миома матки встречается у
15 – 17% женщин старше 30 лет – до постменопаузы.
В постменопаузе, как правило, происходит обратное развитие опухоли.Среди гинекологических больных миома матки наблюдается у 10 – 27%, а при профилактических осмотрах эту опухоль впервые выявляют у 1 – 2,5% женщин. В гинекологических хирургических стационарах оперативное вмешательство по поводу миомы матки производят более чем у 50% больных.
Слайд 5
К основным факторам риска, способствующим возникновению миомы матки, относят:
поздняя менструация;
обильные
менструации;
высокую частоту медицинских абортов;
наличие экстрагенитальной патологии (особенно сердечно-сосудистой);
воспалительные процессы внутренних
половых органов;нарушение гемодинамики малого таза;
метаболические нарушения в организме женщины (ожирение);
вторичные иммунодефицитные состояния;
отягощенный семейный анамнез онкологическими заболеваниями половой системы и других органов (рак эндометрия, шейки матки, яичников, молочной железы, желудка, пищевода, печени).
Слайд 6Патогенез миомы матки
Опухолевый рост является следствием нарушения тканевого гомеостаза, поддерживаемого
балансом между двумя процессами:
-клеточной пролиферацией;
- апоптозом;
Клетки
миомы матки обладают значительно более высокой миотической активностью в обе фазы менструального цикла, чем клетки неизмененного миометрия. Слайд 7Патогенез миомы матки
Ключевыми факторами патогенеза миомы матки считаются:
половые стероидные
гормоны- физиологические регуляторы клеточной пролиферации миометрия.
В отличие от нормального
миометрия миома содержит гораздо больше эстрогеновых рецепторов на единицу объема ткани, число которых особенно возрастает в фолликулиновую фазу, и поэтому ткань миомы матки чрезвучайно чувствительно к эстрогенам. Слайд 8Патогенез миомы матки
В последние годы основопологающее значение приобретает:
« прогестероновая
» гипотеза, в соответствии с которой, не только эстродиол 17-в,
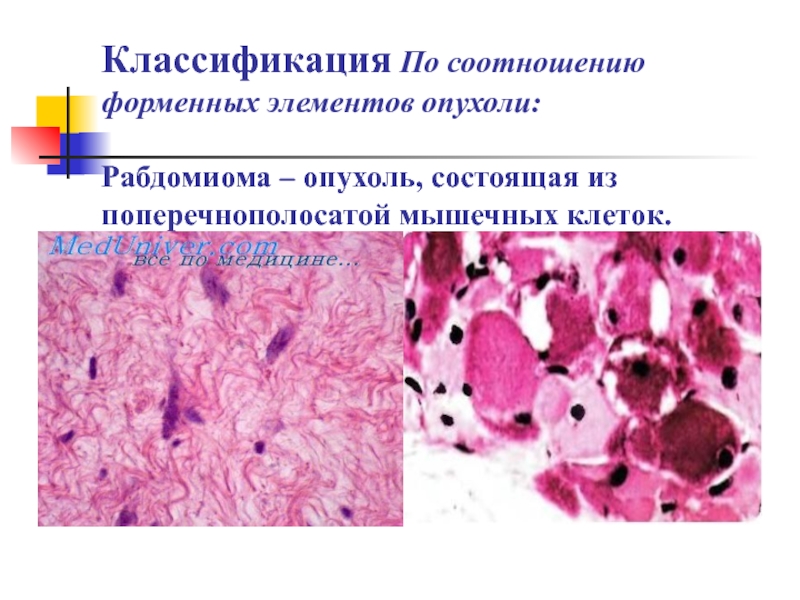
но и, в большей степени , прогестерон играет ключевую роль в инициировании каскада малекулярно- генетических нарушений, возникающих в процессе роста опухоли.Слайд 9Классификация По соотношению форменных элементов опухоли: Рабдомиома – опухоль, состоящая
из поперечнополосатой мышечных клеток.
Слайд 14По гистологическим особенностям:
Простая
Встречается в 75% случаев
Строма преобладает над паренхимой
Растет медленно
Митотическая
активность миоцитов практически отсутствует
Пролиферирующая
Встречается в 25% случаев
Преобладают миогенные элементы
Множественная
Растет быстро
Митотическая
активность повышенаСлайд 16По клиническим проявлениям:
симптомная миома матки (20-50% случаев) – с клиническими
проявлениями
-боли,
-кровотечение,
-нарушение функции соседних органов.
бессимптомная миома матки (50-80% случаев)
– без клинических проявлений; -отсутствует жалобы
-нарушения менструальной функции;
Слайд 17Миома матки, клиника
Миома матки
Менометроррагии
Анемия
Социальный
дискомфорт1
Компрессионные
симптомы
Бесплодие
Слайд 18Диагностика
Жалобы:
аномальные маточные кровотечения;
тазовая боль;
тяжесть внизу живота;
увеличение живота;
нарушение функции мочевого
пузыря (дизурия);
нарушение функции кишечника (дисхезия)
бесплодие.
Слайд 19Диагностика
Анамнез:
отсутствие беременности и родов;
раннее менархе,
увеличение частоты менструации;
длительность дисменореи;
отягощенная наследственность;
повышенная масса тела;
артериальная гипертензия;
сахарный
диабет;возраст (пик заболеваемости 40-50 лет).
Слайд 20 Диагностика миомы матки
Гинекологический осмотр позволяет обнаружить:
- увеличенную матку(
размеры ее оцениваются в неделя беременности),
с бугристой ( узловатой) поверхностью,
плотной
консистенцией.Среди методов инструментальной диагностики миомы матки применяется:
- ультразвуковое сканирование ( трансвагинальное ультрозвуковое сканирование)
- МРТ матки (для уточнение локализации и размеров).
- Гистероскопия ( при субмукозной форме у женщин репродуктивного возраста )
- Лапароскопия ( у женщин репродуктивного возраста для проведения более точной диагностики и хирургического лечения
- лапароскопическая миомэктомия- при субсерозной и субсерозной-интрамуральной формах ).
Слайд 21Ультразвуковая диагностика подбрюшинной миомы матки.
На эхограмме субсерозная миома матки идентифицируется
в виде:
- образования округлой конфигурации, сповышенным уровнем звукопроводимости
-
плотно спаянной маткой. Субсерозные узлы миомы на широком оснавании характеризуется определенными эхографическими признаками:
- акустическое отражение от поверхности опухоли, обращенной в брющную полость отличается повышенной звукопоглащаемостью.
Слайд 22
Трансвагинальное ультразвуковое сканирование. Подбрюшинной миомы матки.
-Угасание амплитуды волновых колебаний от
маточной поверхности опухоли к брюшной.
- Осутствие эффекта « врастания»
опухоли в миометрий, - Повышенная смещаемость опухоли по отношению матки
- Округлой формой,
- С гладкой блестящей поверхностью
- Бледно-розовым оттенком.
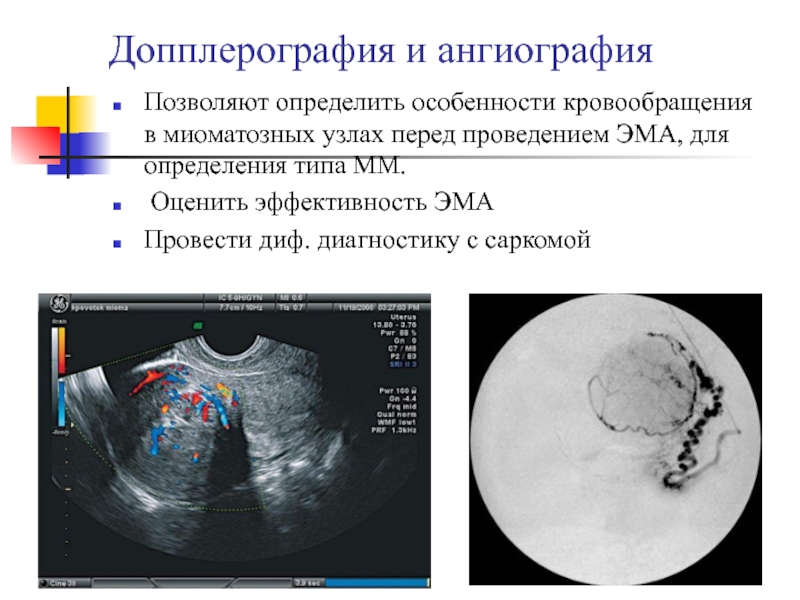
Слайд 23Допплерография и ангиография
Позволяют определить особенности кровообращения в миоматозных узлах перед
проведением ЭМА, для определения типа ММ.
Оценить эффективность ЭМА
Провести диф.
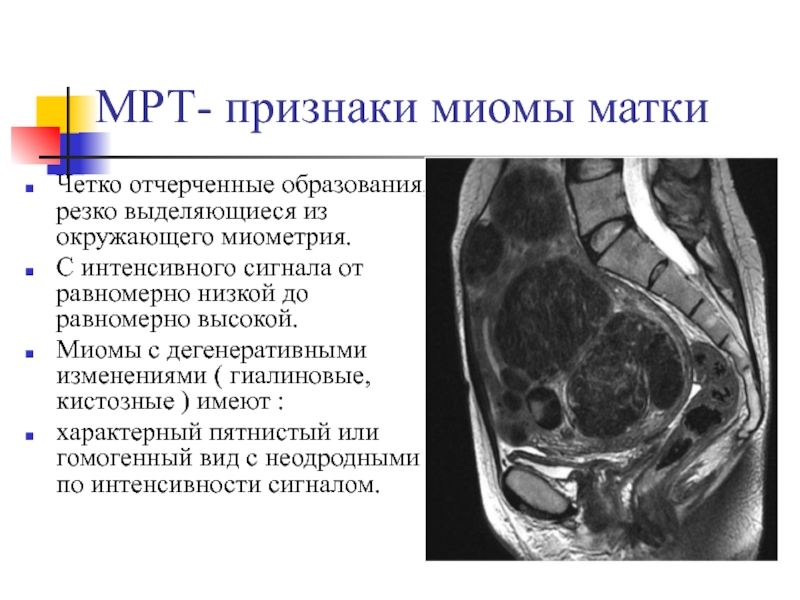
диагностику с саркомойСлайд 24МРТ- признаки миомы матки
Четко отчерченные образования, резко выделяющиеся из окружающего
миометрия.
С интенсивного сигнала от равномерно низкой до равномерно высокой.
Миомы с дегенеративными изменениями ( гиалиновые, кистозные ) имеют :
характерный пятнистый или гомогенный вид с неодродными по интенсивности сигналом.
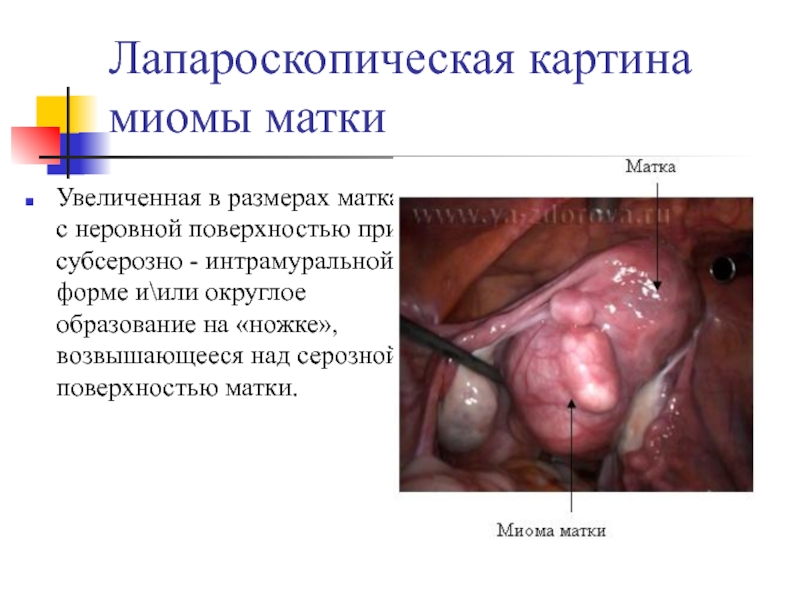
Слайд 25Лапароскопическая картина миомы матки
Увеличенная в размерах матка с неровной поверхностью
при субсерозно - интрамуральной форме и\или округлое образование на «ножке»,
возвышающееся над серозной поверхностью матки.Слайд 26Лечение миомы матки
Медикаментозное
лечение, направленное на контроль роста миомы и развития симптомов заболевания.
Хирургическое
лечение:А. органосохраняющие операции:
абдоминальная,
лапароскапическая
гистероскопическая миомэктомия,применяемые при нериализованной репродуктивной функции
Слайд 27Лечение миомы матки
Б. радикальные операции:
- гистерэктомия, применяемая при множественной миоме
матки больших размеров и у женщин с реализованной репродуктивной функцией.
Малоинвазивные органосохраняющие методы лечения:
- эмболизация маточных артерий(ЭМА),
-миолиз различными источниками энергии).
Слайд 28Показания к медикаментозному лечению миомы:
величина опухоли, увеличивающая размер матки менее
чем до 12-13 недель беременности;
интерстициальное и субсерозное расположение узлов (на
широком основании);наличие противопоказаний к оперативному лечению;
отсутствие маточных кровотечений, приводящих к анемии;
в качестве адъювантной терапии.
Основой консервативной терапии являются гормональные препараты.
Медикаментозное лечение целесообразно проводить при размерах миоматозных узлов до 3см.
Слайд 29Гонадотропины
Даназол, гестринон
Обладают антиэстрогенным и антипрогестероновым эффектом, вызывая временную аменорею.
Препараты
назначают 1 раз в день в течение 3-5 месяцев.
В ряде
случаев аменорея не наступает, а имеется гипоменструальный синдромРазмер матки уменьшается на 50-60%.
Побочные эффекты наблюдаются редко.
Слайд 30Агонисты гонадотропин-рилизинг гормона (аГнРГ)
Бусерелин, трипторелин, лейпрорелин
Блокируют секрецию гонадотропинов и, следовательно,
половых гормонов.
Блокада обратима, после отмены синтез гонадотропных гормонов восстанавливается
Высказано мнение
о прямом влиянии аГнРГ на ММ – в ней обнаружены рецепторы к ГнРГПобочные эффекты связаны с гипоэстрогенией, поэтому возможно сочетание с небольшими дозами эстрогенов.
Слайд 31Антипрогестины
Мифепристон
Связывается с прогестероновыми рецепторами, блокируя их функцию
Главное достоинство препарата –
отсутствие гипоэстрогении
После приема в течение 12 недель размеры ММ уменьшаются
на 50-60%Слайд 32Показания к оперативному лечению:
Большие размеры матки (более 13-14 недель);
Быстрый рост
(более 4 недель в год);
Резистентность к консервативной терапии;
Наличие болей, кровотечений,
нарушение функции соседних органов;Признаки нарушения трофики узла, некроз миоматозного узла;
Подслизистая миома, сопровождающаяся длительными и обильными менструациями. «Рождающийся» миоматозный узел;
Признаки перекрута субсерозного узла на «ножке»;
Миома шейки матки;
Миома матки в сочетании с опухолями половых органов другой локализации, аденомиозом, гиперплазией эндометрия.
Слайд 33Радикальное (ампутация матки)
Включает гистерэктомию лапароскопическим и лапаротомическим доступами.
Лечение по принципу
«нет органа – нет проблем»
Нужно помнить, что в организме лишних
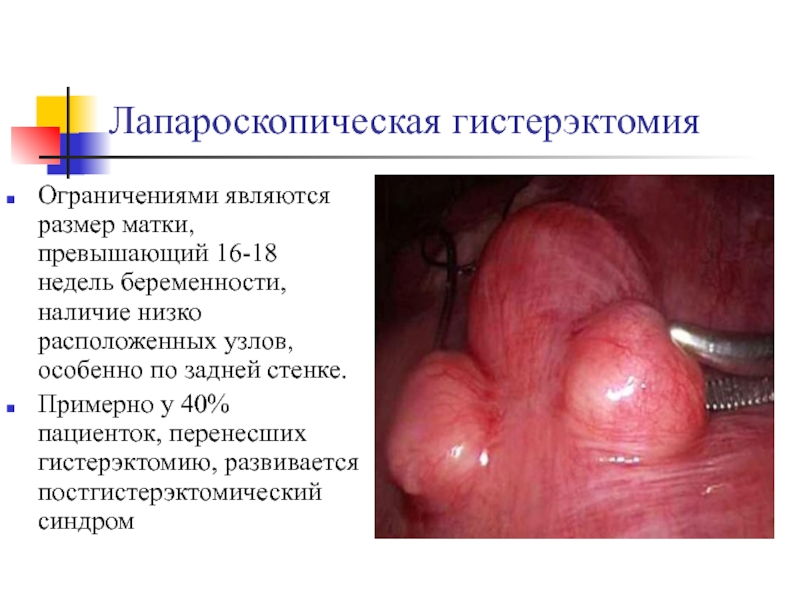
органов нет!Слайд 34Лапароскопическая гистерэктомия
Ограничениями являются размер матки, превышающий 16-18 недель беременности, наличие
низко расположенных узлов, особенно по задней стенке.
Примерно у 40% пациенток,
перенесших гистерэктомию, развивается постгистерэктомический синдромСлайд 35Постгистерэктомический синдром
Обусловлен недостаточностью эстрогенов из-за снижения овариального кровотока и нарушения
рецепторных взаимодействий в системе яичники-миометрий-эндометрий.
Для его коррекции необходима гормонзаместительная терапия(ГЗТ)
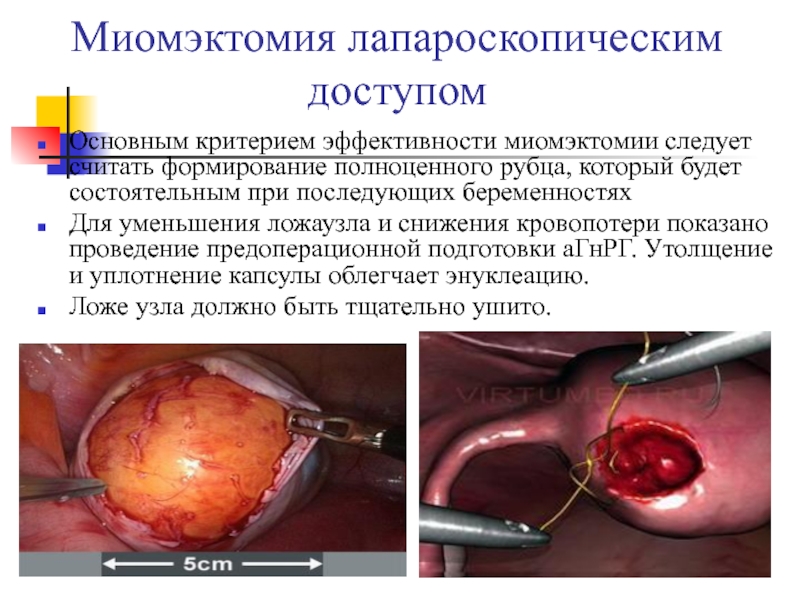
Слайд 37Миомэктомия лапароскопическим доступом
Основным критерием эффективности миомэктомии следует считать формирование полноценного
рубца, который будет состоятельным при последующих беременностях
Для уменьшения ложаузла и
снижения кровопотери показано проведение предоперационной подготовки аГнРГ. Утолщение и уплотнение капсулы облегчает энуклеацию.Ложе узла должно быть тщательно ушито.
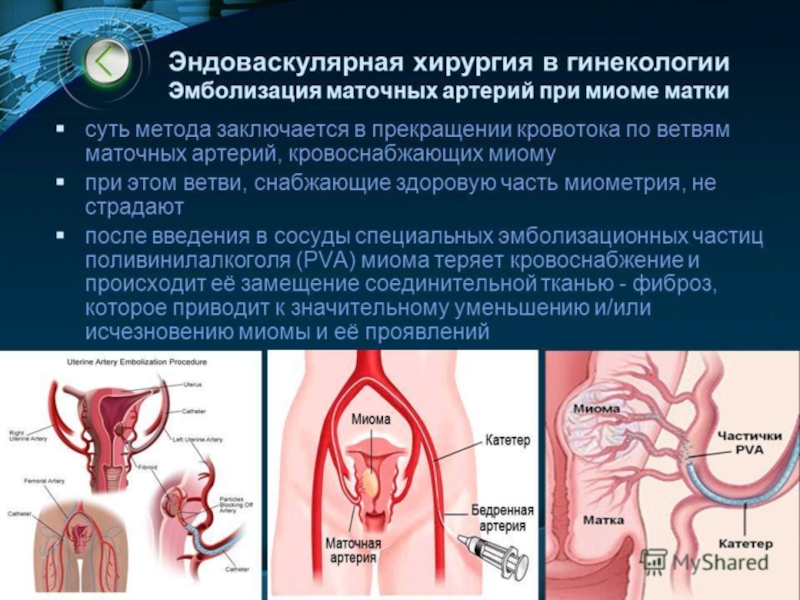
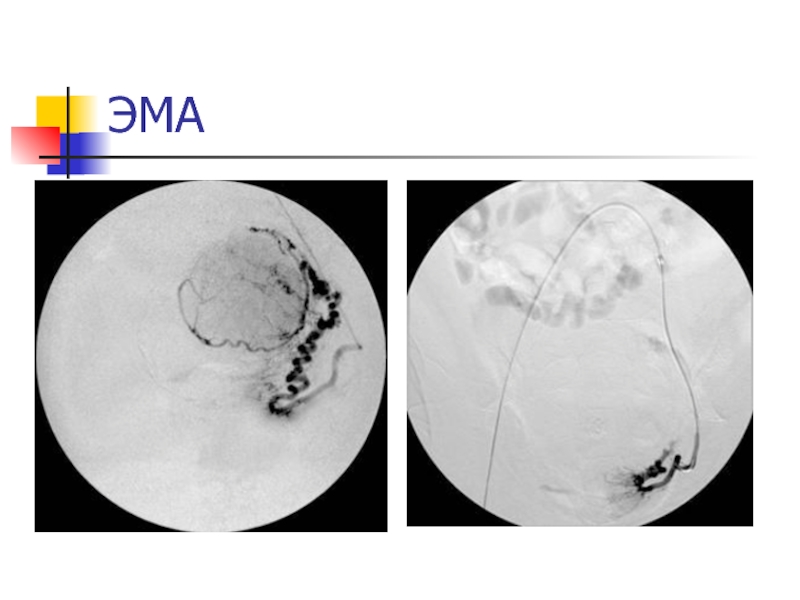
Слайд 38Эмболизация маточных артерий
Эмболизация маточных артерий (ЭМА, эндоваскулярная эмболизация маточных артерий) –
это малоинвазивное вмешательство, в ходе которого через прокол бедренной артерии
(пункцию), по внутрисосудистому катетеру в сосуды, питающие миому, вводятся частички специального эмболизационного препарата.Бессимптомная (3,8%) или симптомная миома матки;
Менометроррагия ( 51,9%)
Диспареуния (7%);
Сдавления соседних органов (20,5%);
Бесплодие(16,8%)
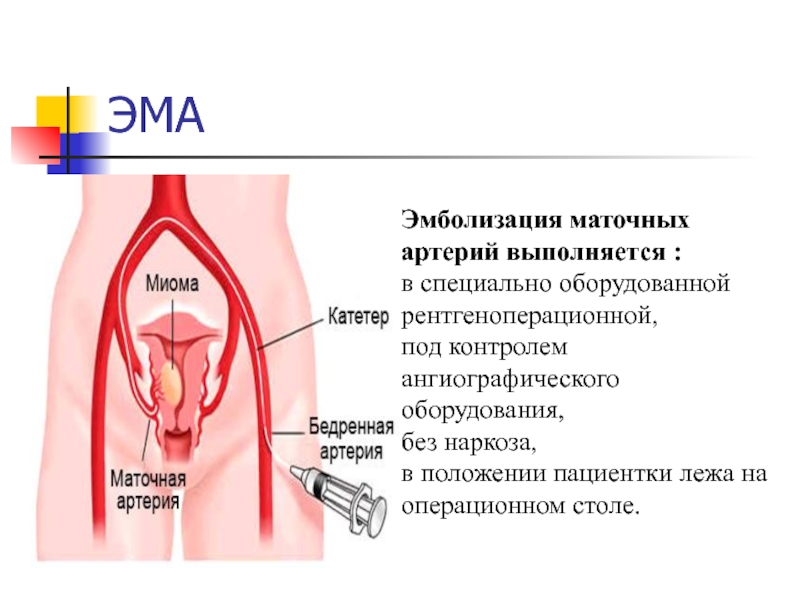
Слайд 40ЭМА
Эмболизация маточных артерий выполняется :
в специально оборудованной рентгеноперационной,
под контролем
ангиографического оборудования,
без наркоза,
в положении пациентки лежа на операционном
столе. Слайд 41ЭМА
Первым этапом вмешательства является:
пункция правой общей бедренной артерии.
местная анестезия
кожи (в зоне прокола в верхней части бедра)
пункция артерии полой
иглой (диаметр 1,5 мм), через которую вводится тонкий катетер (диаметр 1,2 мм). под контролем ангиографии :данные выводятся на монитор,
внутрисосудистый катетер проводится до маточных артерий.
через катетер вводится эмболизационный препарат
Слайд 43ЭМА
В течение 12-18 мес происходит прогрессивное уменьшение размеров миоматозных узлов
и матки в целом в среднем на 83% с восстановлением
архитектоники полости матки.Устранение симптомов менометроррагии (97,9%);
Исчезновение симптомов сдавления близлежащих органов (88,6%);
Исчезновение симптомов диспареуниии (99%);
Пиометра и эндометрит (2,6%) после 3-6 мес
Маточное кровотечения (1,2%);
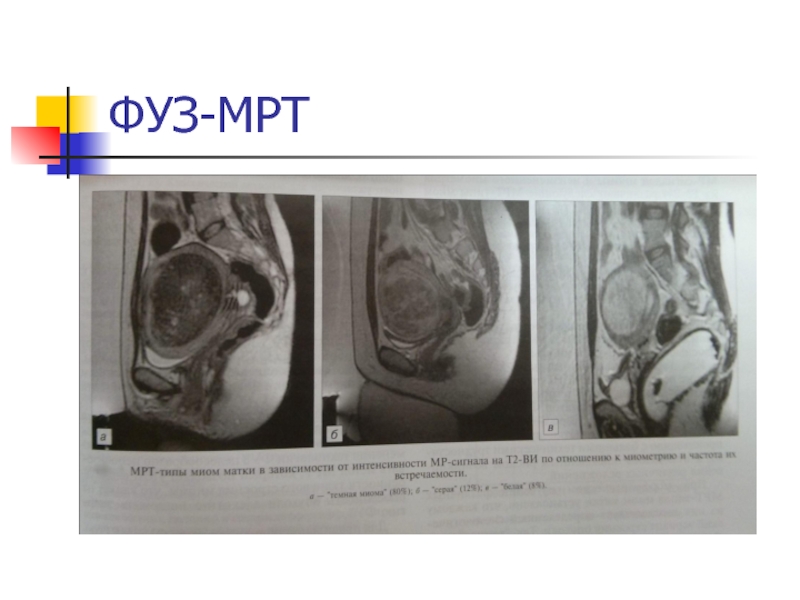
Слайд 44Фокусированная ультразвуковая абляция под контролем МРТ
Сравнительно новый метод лечения ММ,
применяется в России с 2006 года.
Сущность метода заключается в
воздействии на ткань ММ высокочастотного УЗ, под действием которого происходит нагрев и развивается коагуляционный некроз. Пациентка располагается в положении лежа на животе внутри магнитно-резонансного томографа.
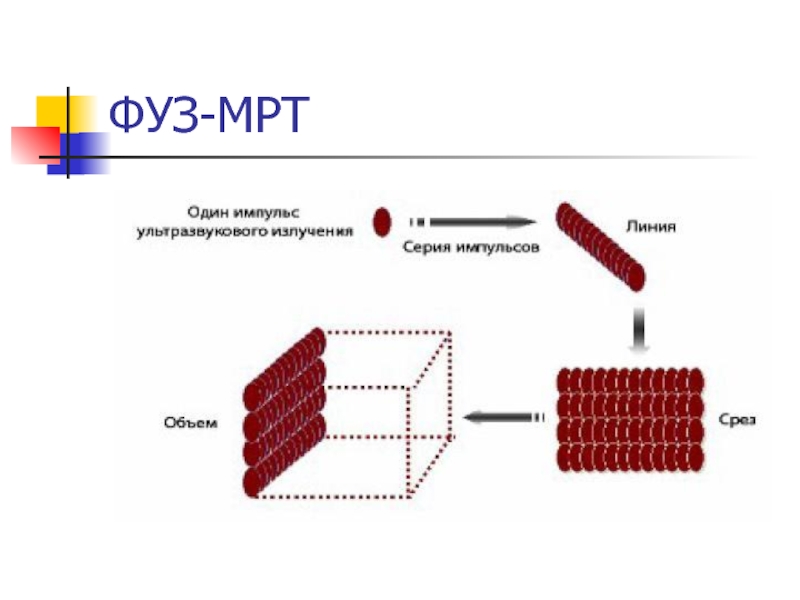
Слайд 45ФУЗ-МРТ
Проводится базовое сканирование, врач намечает план операции.
Затем выполняется сама
процедура, в ходе которой УЗ поочередно воздействуют на определенный объем
ткани.Продолжительность процедуры 3-5 часов.
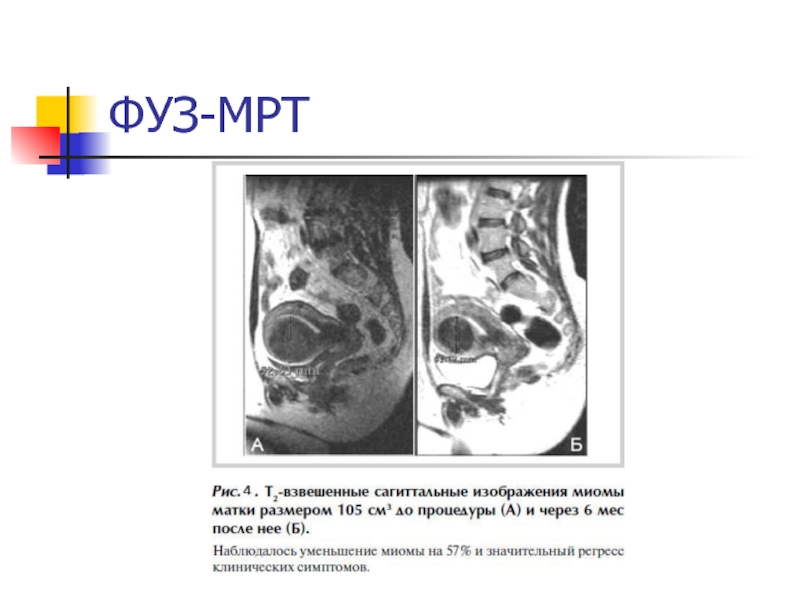
Так как ультразвук в большей степени поглощается соединительной тканью, этот метод практически неприменим для пролиферирующих миом. Наибольшая эффективность в отношении «темных» миом.
Через 6 месяцев после процедуры ММ уменьшается в среднем на 50%.