Слайд 1Спектрофотометрия в инфракрасной области спектра
Слайд 2Содержание
Краткие теоретические основы метода
Спектрофотометрия в инфракрасной области
2.1. Применение ИК-спектроскопии для идентификации веществ
2.2. Применение ИК-спектроскопии в количественном анализе
Способы подготовки образцов для ИК-спектроскопии
3.1. Прессование ксероформа в таблетку с калия бромидом
3.2. Подготовка образца ксероформа в суспензии с вазелиновым маслом
Слайд 31. Краткие теоретические основы метода
Слайд 4Спектроскопические методы анализа основаны на избирательном поглощении электромагнитного излучения анализируемым
веществом и служат для исследования строения, идентификации и количественного определения
светопоглощающих соединений.
Слайд 5В зависимости от используемой аппаратуры в фармацевтическом анализе различают следующие
методы анализа, основанные на поглощении электромагнитного излучения и испускании света:
Спектрофотометрия
в ультрафиолетовой (УФ) и видимой областях
Спектрофотометрия в инфракрасной (ИК) области
Атомно-эмиссионная и атомно-абсорбционная спектроскопия (АЭС и ААС)
Флуориметрия
Спектроскопия ядерного магнитного резонанса (ЯМР).
Слайд 6Ряд длин волн, для которых проводятся измерения методами абсорбционной спектрофотометрии,
охватывает спектральную область от коротких длин волн в УФ-области до
ИК-области.
Для удобства отнесений этот спектральный ряд делится на следующие диапазоны длин волн:
УФ (от 190 до 380 нм);
видимый (от 380 до 780 нм);
- ИК (от 0,78 до 400 мкм).
Слайд 72. Спектрофотометрия в инфракрасной области спектра
Слайд 8Спектрофотометрия в инфракрасной области спектра (ОФС 42-0043-07)
ИК-спектрофотометрия – метод исследования
веществ, основанный на поглощении ИК-излучения, в результате чего происходит усиление
колебательных и вращательных движений молекул.
Инфракрасные (ИК) спектры (колебательные спектры) возникают вследствие поглощения электромагнитной энергии при колебаниях ядер атомов в молекулах или ионах, которые сопровождаются изменением дипольных моментов, и представляют собой график зависимости процента пропускания от длины волны (λ, мкм) или частоты колебаний ИК-излучения.
Поскольку частота колебаний в ИК-спектрах имеет большие числовые значения, обычно используют не частоты (ν), а волновые числа ( ), которые измеряются в см-1. Волновое число ( ) связано с длиной волны (λ, в мкм) соотношением:
Слайд 9Спектрофотометрия в инфракрасной области (ОФС 42-0043-07)
Под ИК-областью подразумевают электромагнитное излучение
в области длин волн от 0,780 до 400 мкм.
Ближняя
ИК-область: от 780 до 2500 нм (от 0,780 до 2,5 мкм).
Средняя ИК-область: от 2,5 до 25 мкм (от 4000 до 400 см-1).
Дальняя ИК-область: от 25 до 400 мкм.
Наиболее часто используется средняя ИК-область.
Слайд 102.1. Применение ИК-спектроскопии для доказательства подлинности веществ
Лекарственные средства в основном
идентифицируются путем сопоставления спектра исследуемого вещества со спектром стандартного образца,
полученном на том же приборе и при тех же условиях, что и спектр исследуемого вещества.
Сопоставление ИК-спектров рекомендуется начинать с анализа характеристических полос, которые обычно хорошо проявляются на спектрах, и лишь при их совпадении сопоставляют низкочастотную область. Для низкочастотного интервала 1350-400 см-1 характерен специфический набор полос, который называют областью «отпечатков пальцев».
Слайд 11Для подтверждения соответствия лекарственного средства своему наименованию используют несколько подходов:
Сравнение ИК-спектра анализируемого вещества с ИК-спектром стандартного образца, снятых в
одинаковых условиях Рисунки спектров должны совпадать по числу полос поглощения, их частоте и форме контура. Полное совпадение полос поглощения в ИК-спектрах свидетельствует об идентичности вещества.
Сравнение ИК-спектра анализируемого вещества со спектром приведенным в фармакопейной статье Метод используется, если стандартный образец анализируемого вещества отсутствует.
Возможность снятия ИК-спектра определенного участка наиболее характерного фрагмента структуры вещества
Используется для лекарственных средств близких по структуре.
Слайд 122.2. Применение ИК-спектроскопии в количественном анализе
Количественный анализ по спектрам
поглощения основан на применение закона Бугера-Ламберта-Бера.
Существенной характеристикой веществ является интенсивность
полос поглощения, которая может быть охарактеризована в спектрах величиной интегральной интенсивности поглощения (А), равной площади огибаемой кривой поглощения.
Слайд 13ИК-спектрофотометрия включает следующие стадии:
Подготовка исследуемого образца
Регистрация (снятие) спектра с помощью
прибора
Интерпретация (анализ спектра, отнесение полос поглощения к определенным функциональным группам,
связям, фрагментам структур).
Слайд 15Спектрофотометрию в ИК-области можно использовать для исследования твердых тел, газов
и жидкостей.
Процедура отличается способом подготовки образца.
Слайд 163. Способы подготовки образцов для ИК-спектроскопии
Слайд 17Существуют три способа подготовки веществ к снятию спектра:
Для жидких
веществ
Готовят тонкую полимерную пленку веществ: для этого растворяют образцы
в легколетучих растворителях, и раствор наносят пипеткой на пластинки из NaCl или KBr, растворитель испаряется в вакууме, пластинку с тонким покрытием помещают в спектрофотометр и снимают спектр.
2. Для растворов
Раствор исследуемого образца в концентрации от 0,5 до 1,5% помещают в кювету с толщиной слоя 0,1-1 мм и снимают спектр относительно чистого растворителя.
Слайд 183. Для твердых веществ
а) Вещество растирают в агатовой ступке
с иммерсионной жидкостью (вазелиновое или парафиновое масло), т.е. готовят пасту,
и помещают между двумя пластинами натрия хлорида или калия бромида и прессуют (частицы вещества не должны быть более 2 мкм). В канал сравнения помещают пластинки с иммерсионной жидкостью.
б) Вещество запрессовывают в таблетку с калия бромидом. Таблетка должна быть прозрачной, а растирание и таблетирование должно производится в отсутствии влаги воздуха.
Слайд 193.1. Подготовка образца: прессование ксероформа в таблетку с калия бромидом
Слайд 20Порядок работы
Взвешивают навеску калия бромида
Слайд 21Порядок работы
Переносят навеску калия бромида в агатовую ступку
Слайд 22Порядок работы
Взвешивают навеску ксероформа на аналитических весах
Слайд 23Порядок работы
Переносят навеску ксероформа в агатовую ступку
Слайд 24Порядок работы
Навеску ксероформа тщательно перемешивают с порошком калия бромида
Слайд 25Полученную смесь насыпают в рамное кольцо около 3 мг
Слайд 26Порядок работы
Прессуют таблетку в специальной пресс-форме
Таблетка представляет собой прозрачную пластинку
диаметром от 3 до 30 мм, толщиной от 0,1 до
1 мм
Слайд 27Порядок работы
Рамное кольцо с полученной таблеткой помещают в держатель рамного
кольца
Слайд 28Порядок работы
Держатель рамного кольца вместе с таблеткой помещают в кюветное
отделение ИК-спектрофотометра
В канал сравнения помещают держатель рамного кольца без таблетки
Слайд 293.2. Подготовка образца ксероформа в суспензии с вазелиновым маслом
Слайд 30Порядок работы
Взвешивают навеску ксероформа на аналитических весах
Слайд 31Переносят навеску ксероформа в агатовую ступку
Слайд 32Добавляют 1 каплю вазелинового масла
Слайд 33Тщательно растирают до получения однородной кремообразной пасты
Слайд 34Полученную пасту помещают в виде тонкого слоя между пластинками калия
бромида
Слайд 35Порядок работы
Пластинки калия бромида с пастой помещают
в разборную кювету
Слайд 36Порядок работы
Разборную кювету вместе с пластинками калия бромида с пастой
помещают в кюветное отделение ИК-спектрофотометра
В канал сравнения помещают разборную кювету
вместе с пластинками калия бромида
Слайд 37Порядок работы
Снимают ИК-спектр на ИК-спектрофотометре
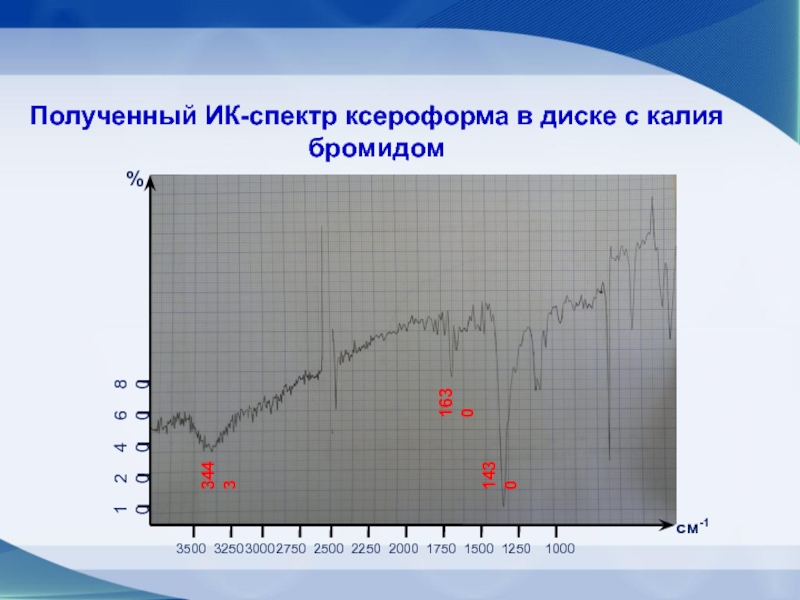
Слайд 38Полученный ИК-спектр ксероформа в диске с калия бромидом
1500
1250
1430
1750
1630
2000
2250
2500
2750
3000
3250
3500
1000
3443
см-1
%
60
40
20
80
10
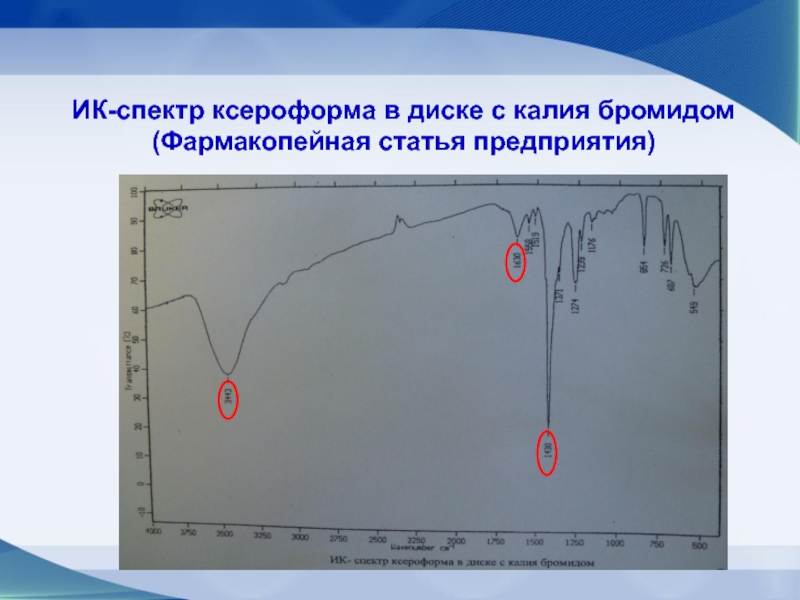
Слайд 39ИК-спектр ксероформа в диске с калия бромидом (Фармакопейная статья предприятия)
Слайд 40Рисунки спектров совпадают по числу полос поглощения, их частоте и
форме контура. Полное совпадение полос поглощения в ИК-спектрах свидетельствует об
идентичности вещества.
Заключение: субстанция ксероформа соответствует требованиям ФСП по показателю «Подлинность».
Слайд 41Список литературы:
Беликов, В.Г. Фармацевтическая химия / 4-е изд., перераб. и
доп. – М., МЕДпрессинформ", 2008. – 613 с.
Государственная фармакопея Российской
Федерации [Текст]. – 12-е изд. – М.: Науч. центр экспертизы средств мед. применения, 2007. – Ч. 1. – 696 с.
Практическое руководство к лабораторным занятиям по фармацевтической химии для студентов III курса / Т.И. Ярыгина, О.Л. Визгунова, В.А. Дубовик и др. / под ред. Л.М. Коркодиновой – Пермь, 2011. – 102 с.
Руководство к лабораторным занятиям по фармацевтической химии: учеб. пособие / Э.Н. Аксенова, О.П. Андрианова, А.П. Арзамасцев и др. / под. ред. А.П. Арзамасцева. – 3-е изд., перераб. и доп. – М., Медицина, 2001. – 384 с. : ил.1.
Слайд 42Иллюстративные материалы подготовили:
Хамидуллина Назиля Наилевна, студентка 55 группы ГБОУ ВПО
ПГФА
Саттарова Ольга Евгеньевна, доцент кафедры фармацевтической химии факультета очного обучения
ГБОУ ВПО ПГФА, кандидат фармацевтических наук, директор Центра дистанционных образовательных технологий
Люст Елена Николаевна, кандидат фармацевтических наук, старший преподаватель кафедры токсикологической химии
Консультант:
Ярыгина Татьяна Ивановна, профессор кафедры фармацевтической химии факультета очного обучения ГБОУ ВПО ПГФА, доктор фармацевтических наук