Слайд 1 Атомистическая теория
Закон постоянства состава – где бы
химическое соединение не было получено его состав и свойства одинаковы
Закон
кратных отношений- в химических соединениях массы образующих их элементов соотносятся между собой как простые целые числа
Закон эквивалентов – элементы соединяются между собой в определенных массовых количествах, всегда соответствующих их эквивалентам
Слайд 2 Термодинамическое обоснование нестехиометрии
Допустим, что кристалл стехиометрический.
Кристалл АВ
частично диссоциирует в твердой фазе
ABs=As+Bs KAB=XAXB/XAB
Так как диссоциация очень слабая,
то XAB≅1
Между компонентами твердого раствора и паровой фазой устанавливаются равновесия
As=Av KA=PA/XA ⇒ XA=(1/KA) PA
Bs=Bv KB=PB/XB ⇒ XB=(1/KB) PB
KA и KB – константы распределения нестехиометрических компонентов между паровой и твердой фазами
В общем случае KA ≠ KB , а в стехиометрическом кристалле при PA=PB
XA ≠ XB
Слайд 3 Стехиометрия
выполнение закона кратных отношений в кристаллических фазах
химических соединений
Na1,00000…Cl1,00000
Mg1,00000…Si1,00000…O4,00000……
Слайд 4Нестехиометрия
свойство несовпадения реального состава кристаллического химического соединения с идеальным
составом
явление, описывающее процесс нарушения стехиометрии
Слайд 5Способы выражения нестехиометрии
Для кристалла AkBm по результатам химического анализа нестехиометрию
выражают следующей записью
Слайд 6Способы выражения нестехиометрии
xAизб.- концентрация избыточного (относительно стехиометрии) компонента в соединении
AmBk
единица измерения – моль избыточного компонента А/ моль несетхиометрического соединения
AmBk
Учитывая, что nAизб.<
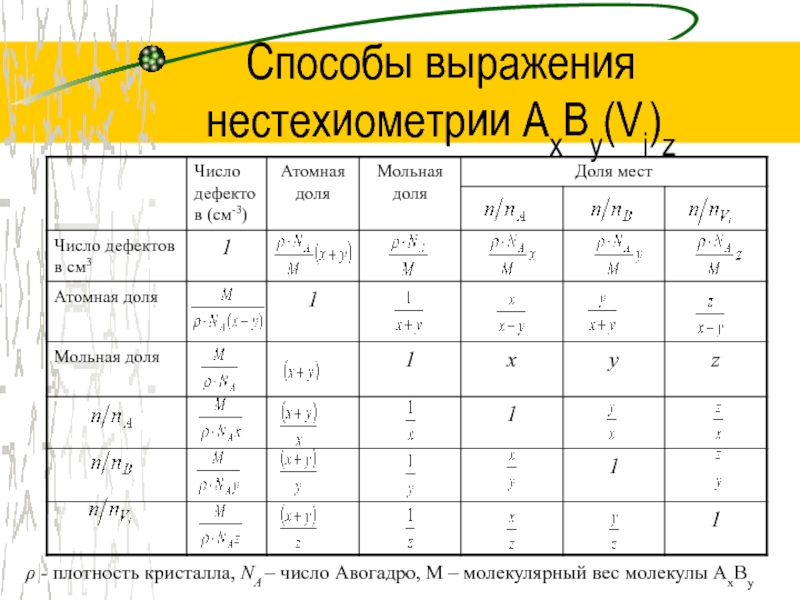
Слайд 7Способы выражения нестехиометрии AxBy(Vi)z
ρ - плотность кристалла, NA – число
Авогадро, М – молекулярный вес молекулы AxBy
Слайд 8Нестехиометрия
Молекулярные или немолекулярные кристаллы?
Нестехиометрическая фаза – твердый раствор избыточного компонента
А в идеальном кристалле АВ.
Величина нарушения стехиометрии зависит от
степени диссоциации молекул в сосуществующей с кристаллом фазе – «кристалл-пар», «кристалл-расплав»
Слайд 9Нестехиометрические фазы
Химические соединения
Твердые растворы внедрения
Соединения включения – клатраты, интеркалаты
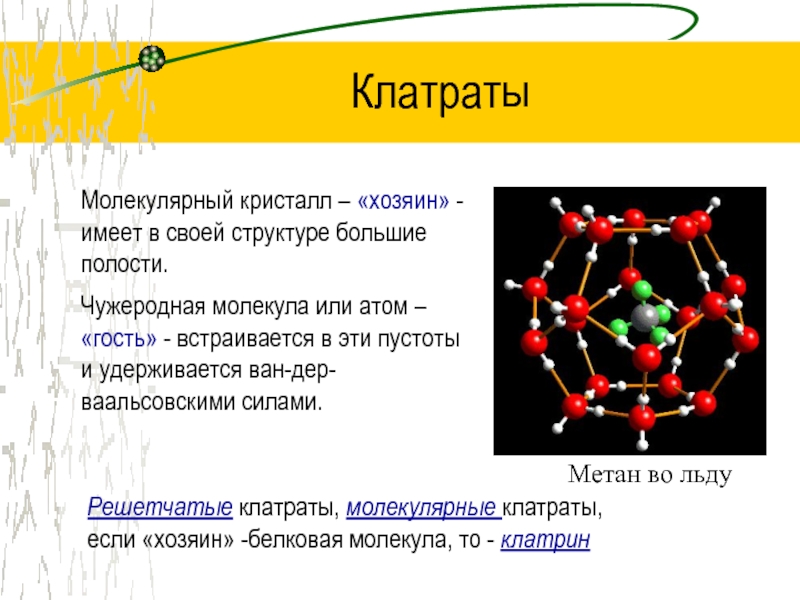
Слайд 10Клатраты
Молекулярный кристалл – «хозяин» - имеет в своей структуре большие
полости.
Чужеродная молекула или атом – «гость» - встраивается в эти
пустоты и удерживается ван-дер-ваальсовскими силами.
Решетчатые клатраты, молекулярные клатраты,
если «хозяин» -белковая молекула, то - клатрин
Метан во льду
Слайд 11Интеркалаты
Интеркалаты - -клатраты со слоистой структурой «хозяина», когда между слоями
встраиваются молекулы «гостя»
Слайд 12 Квазихимический метод описания
процессов образования
дефектов
Кристалл состоит из структурных элементов (частиц в узлах и междоузлиях
решетки, вакансий в узлах, ассоциатов частиц и т.п.)
В реакциях образования дефектов принимают участие квазичастицы – электроны и «дырки»
Реакции образования дефектов записываются по правилам написания химических реакций
Закон сохранения массы
Закон сохранения заряда
Принцип постоянства отношения числа разносортных узлов кристаллической решетки
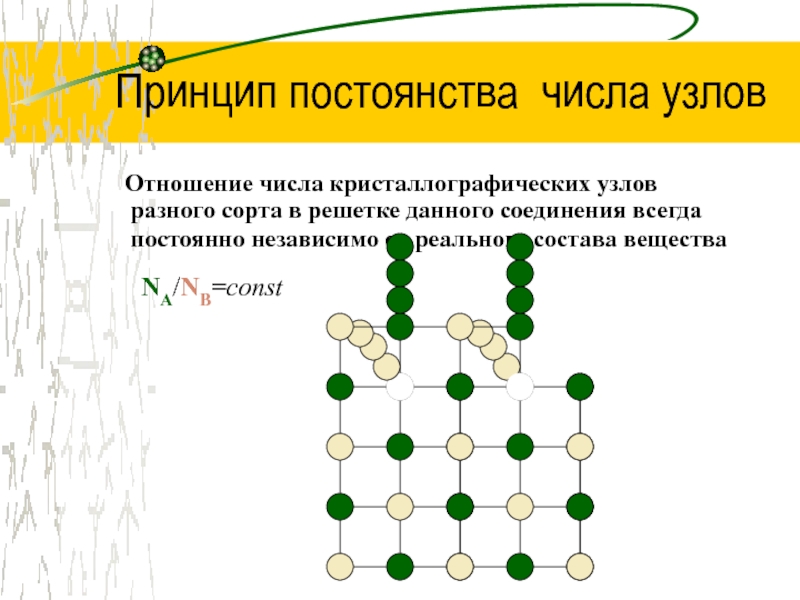
Слайд 13Принцип постоянства числа узлов
Отношение числа кристаллографических узлов разного
сорта в решетке данного соединения всегда постоянно независимо от реального
состава вещества
NA/NB=const
Слайд 14Квазихимическая реакция
(закон действия масс)
Квазихимическая реакция – реакция, в
которой структурные единицы кристалла ведут себя как химические компоненты
АВS+AV=VB+A1+δBS
Согласно закону действующих масс
квазихимическую реакцию можно записать
AV=VB
Квазихимическая реакция
(принцип постоянства числа узлов)
Однако, соблюдение принципа постоянства отношения числа узлов различного сорта требует, чтобы к противовес каждой вакансии в подрешетке В образовался соответствующий узел в подрешетке А
AV=VB+AA
Слайд 16Закон сохранения заряда
(принцип электронейтральности кристалла)
Рассмотрим ионный кристалл A+B- при растворении
в нем атома А
В действительности кристалл электрически нейтрален
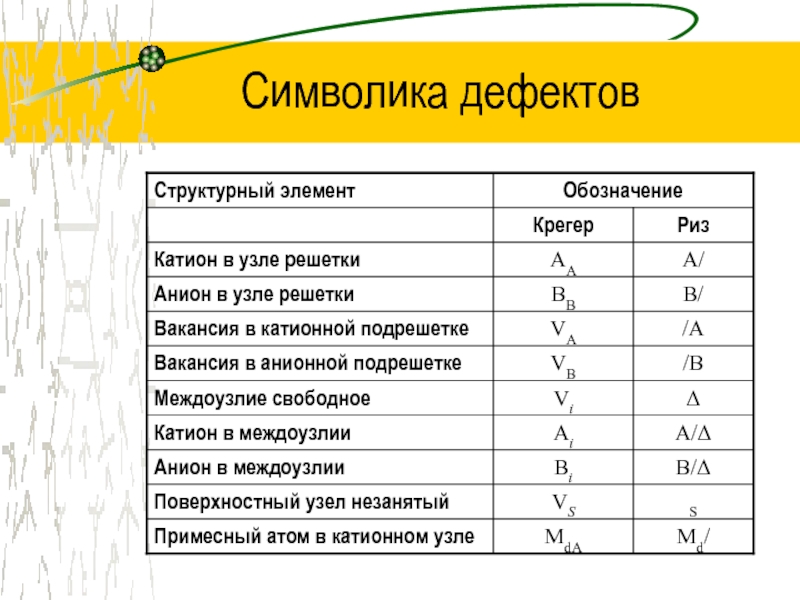
Слайд 17Эффективный заряд
Эффективный заряд – разность между реальным зарядом структурного дефекта
и зарядом структурной единицы в идеальном кристалле
× -
нейтральный эффективный заряд
’- отрицательный эффективный заряд
• - положительный эффективный заряд
Слайд 18Закон сохранения заряда
(принцип электронейтральности кристалла)
С учетом представлений об эффективном заряде
реакция растворения будет выглядеть следующим образом
Согласно определению эффективного заряда своя
частица в регулярном узле является электрически нейтральной
Сумма всех положительных эффективных зарядов должна быть равна сумме всех отрицательных эффективных зарядов
Слайд 19Электронные дефекты
Избыточный свободный электрон ( е´ ) присоединяется к атому
(или иону), расположенному в узле решетки, и придает ему дополнительный
эффективный отрицательный заряд. По кристаллу такой электрон перемещается за счет хаотических скачкообразных перескоков от одного атома к другому
AA’AA→ AAA’A→ AAAA’
Недостающие электроны – «дырки» ( h∙ ) – ведут себя аналогично, придавая атомам дополнительный эффективный положительный заряд
Обозначение концентраций - электронов – [е´ ]=n
- «дырок» – [h∙ ]=p
Слайд 20Нейтральные атомные дефекты
свободные узлы, которые в идеальном кристалле заняты
- вакансии
атомы в местах, которые в идеальном кристалле свободны
– междоузельные атомы
атомы находятся в местах, предназначенных в идеальном кристалле другим атомам - анти-структурные (анти-сайтовые) дефекты
кристаллической решетки
Слайд 22Тепловой беспорядок по Френкелю
В кристалле имеется N – катионных узлов,
Ni – междоузлий, n – частиц переходит из узлов в
междоузлия, тогда
Слайд 23Тепловой беспорядок по Френкелю
Допуская, что количество дефектов на порядки меньше
количества регулярных частиц в кристалле, имеем
Учитывая, что
получаем
Слайд 24Тепловой беспорядок по Шоттки
Учитывая,что
Слайд 25Химический потенциал дефектов
Уравнение Гиббса-Дюгема для описания состояния фазы, находящейся в
равновесии имеет вид
Фаза кристалла с дефектами, находится
в равновесии с паром или расплавом. При этом выбор компонента фазы с точки зрения термодинамики – произвольный.
Для фазы кристалла это могут быть
Катионы или анионы в узле
Частицы в междоузлии
Вакансии в обеих подрешетках и т.п.
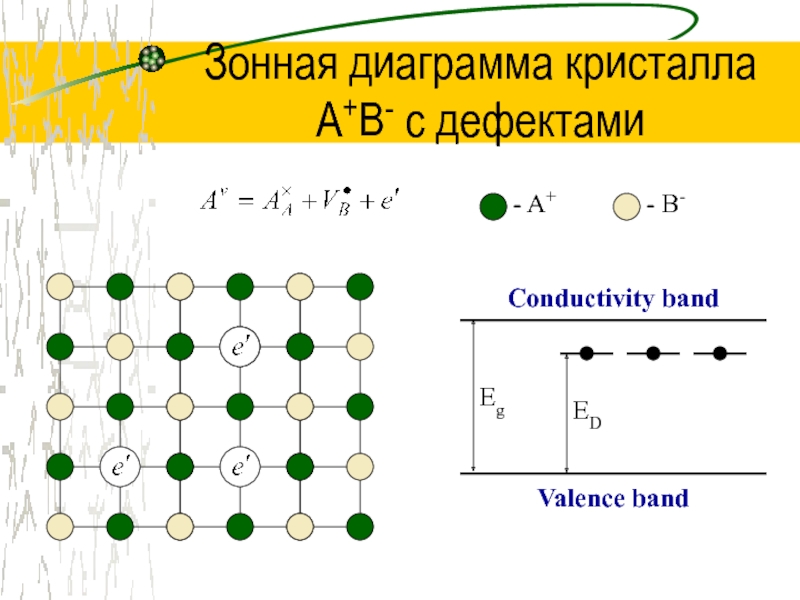
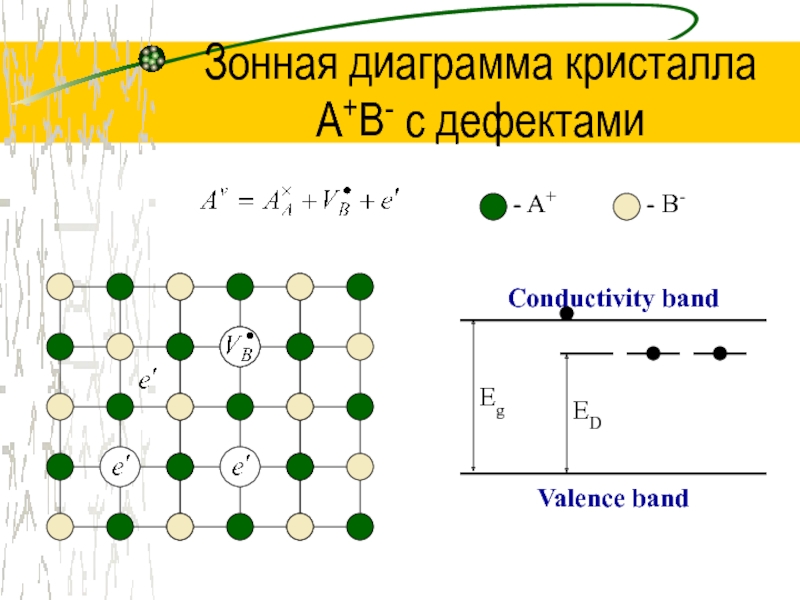
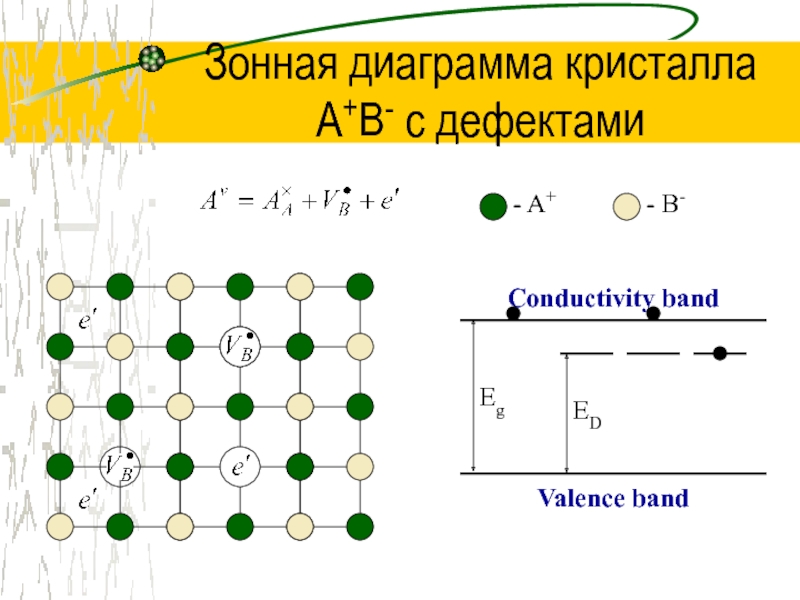
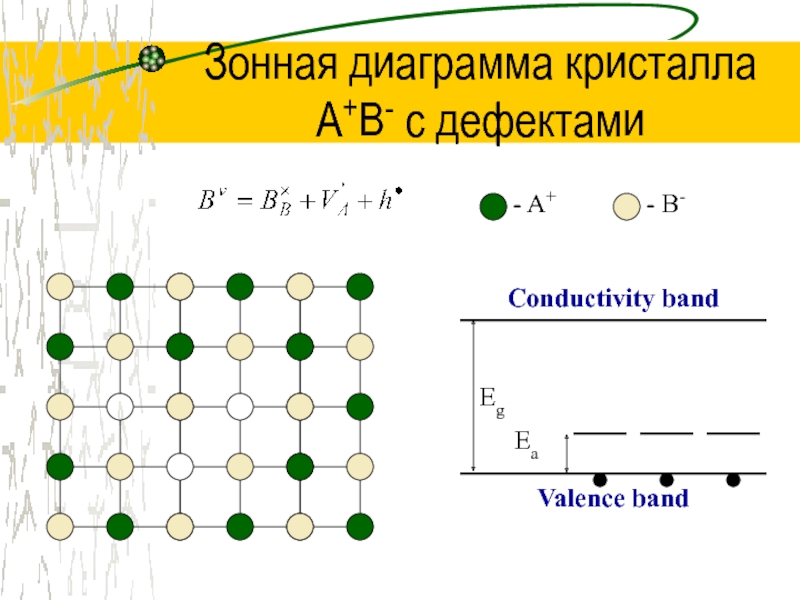
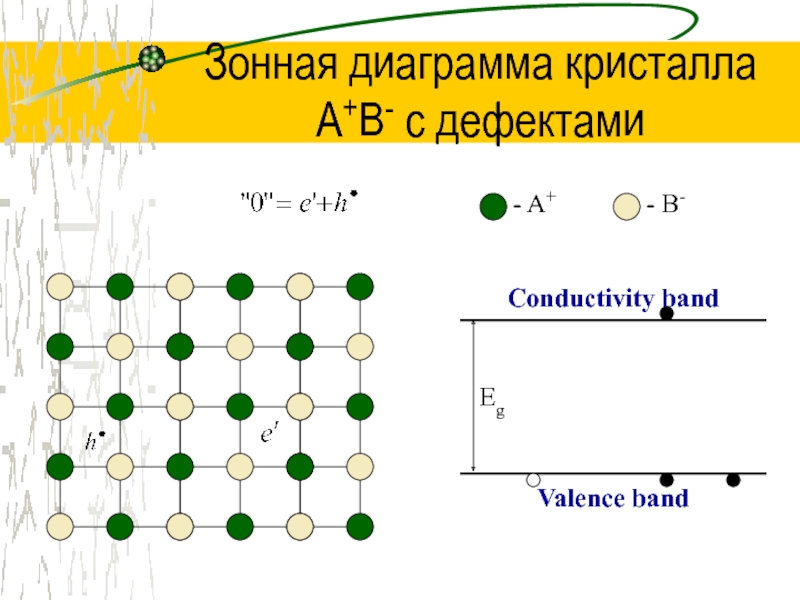
Слайд 26Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
ED
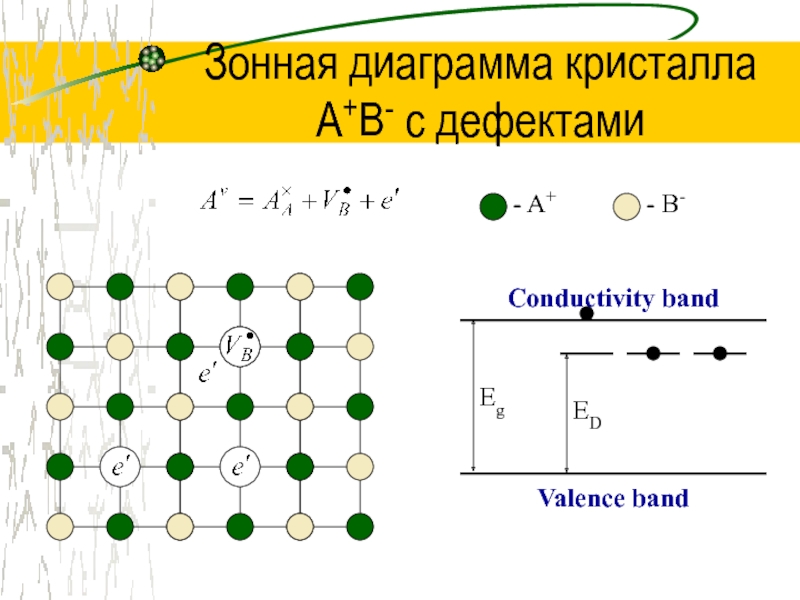
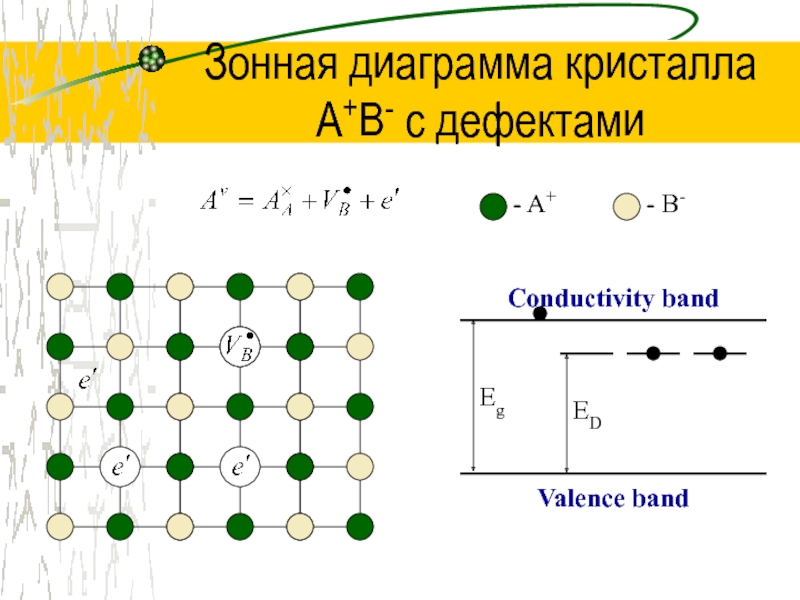
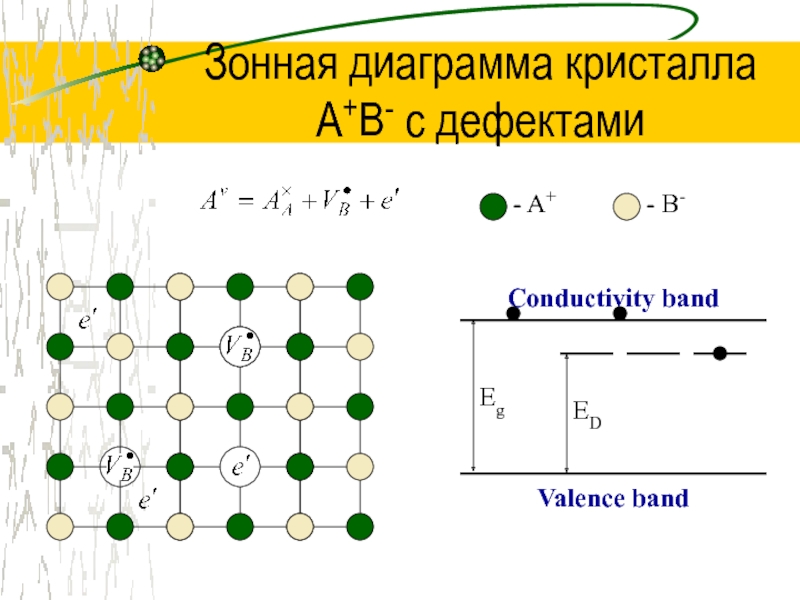
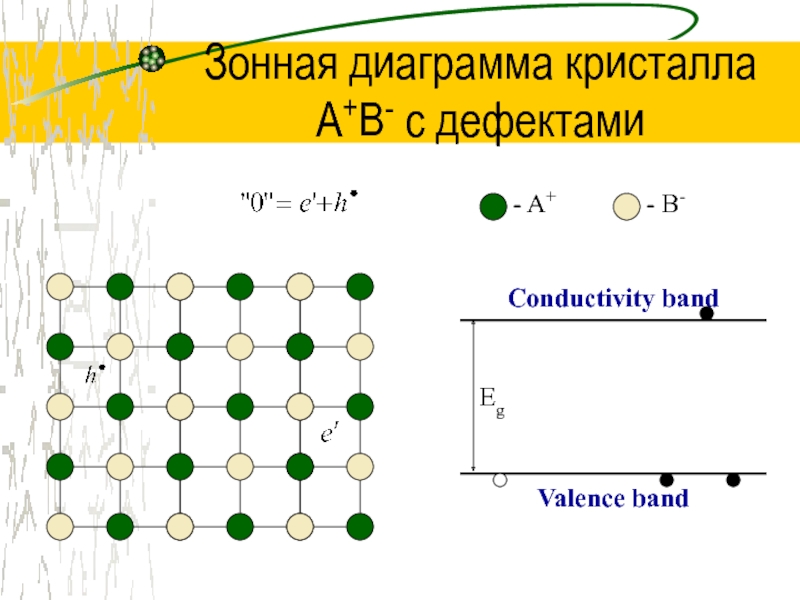
Слайд 27Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
ED
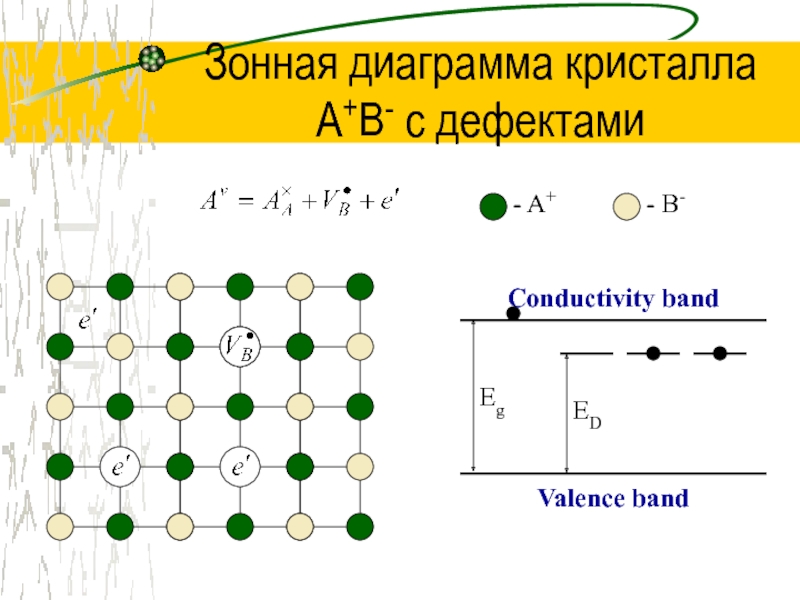
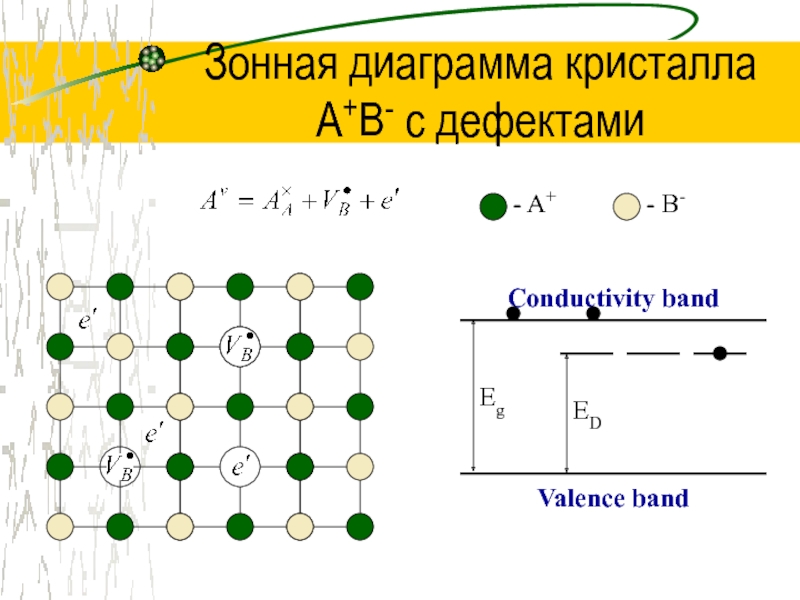
Слайд 28Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
ED
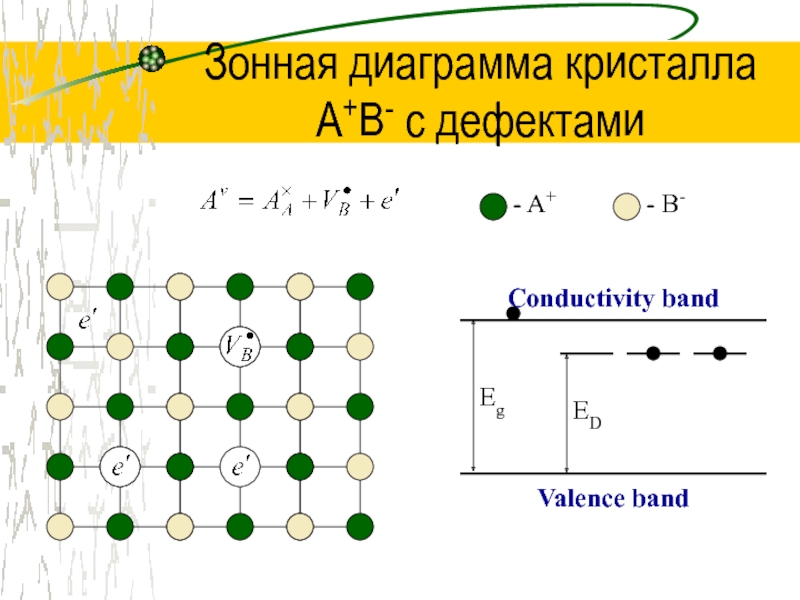
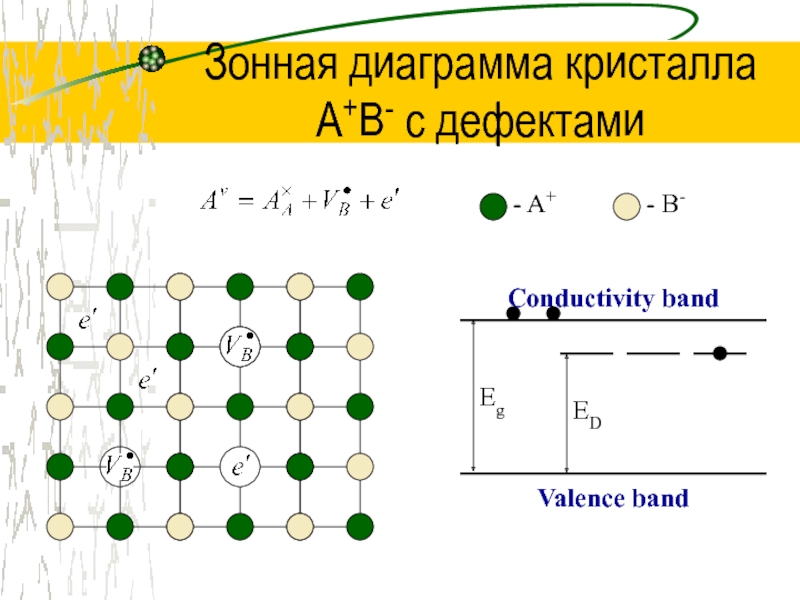
Слайд 29Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
ED
Слайд 30Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
ED
Слайд 31Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
ED
Слайд 32Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
ED
Слайд 33Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
ED
Слайд 34Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
ED
Слайд 35Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
ED
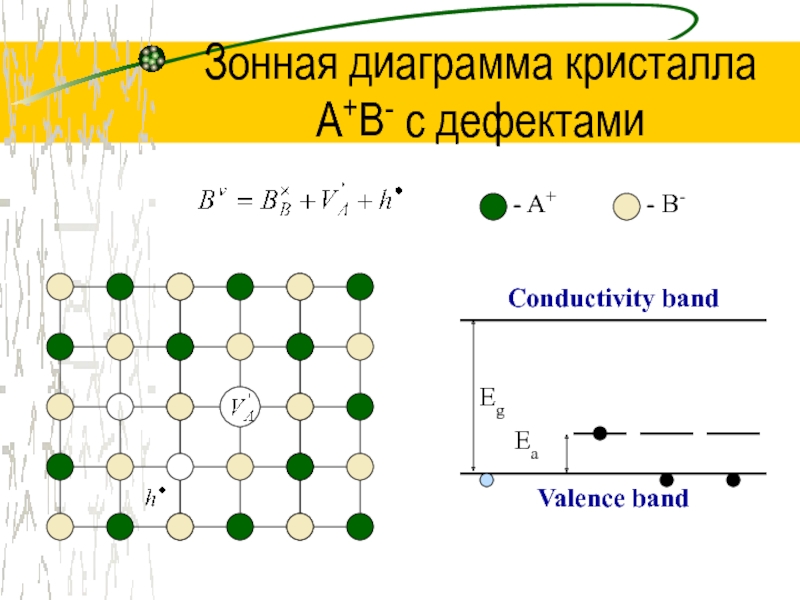
Слайд 36Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
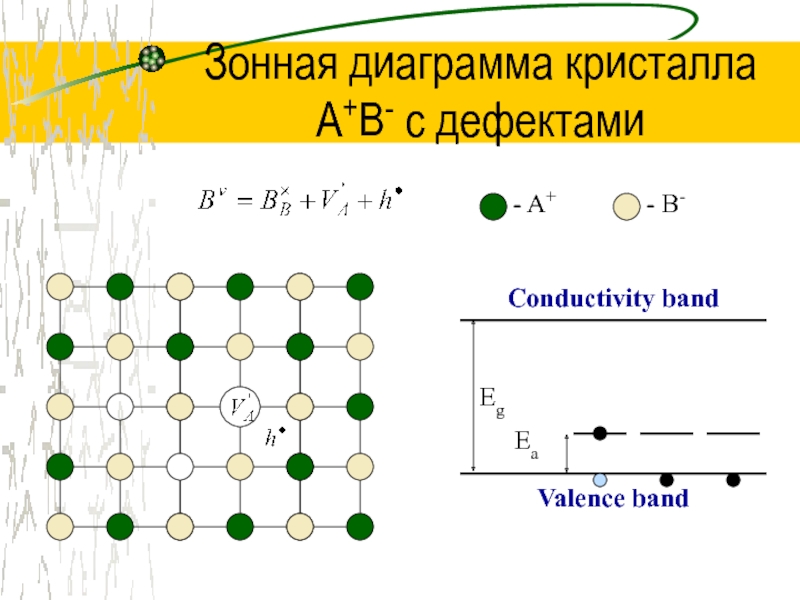
Conductivity band
Valence band
Eg
Ea
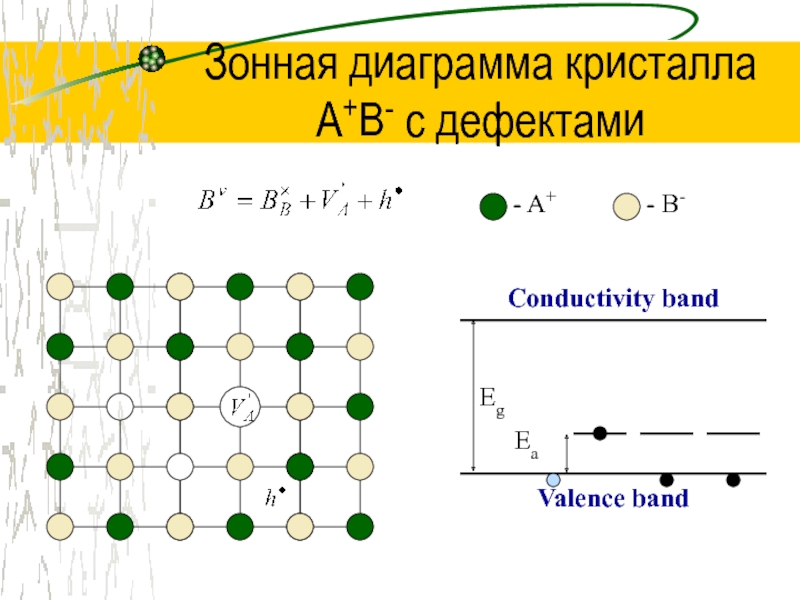
Слайд 37Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
Ea
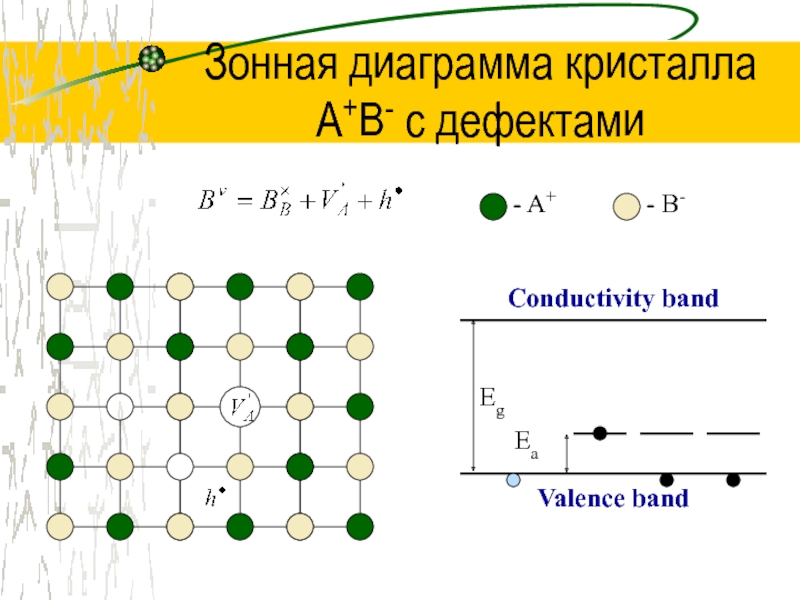
Слайд 38Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
Ea
Слайд 39Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
Ea
Слайд 40Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
Ea
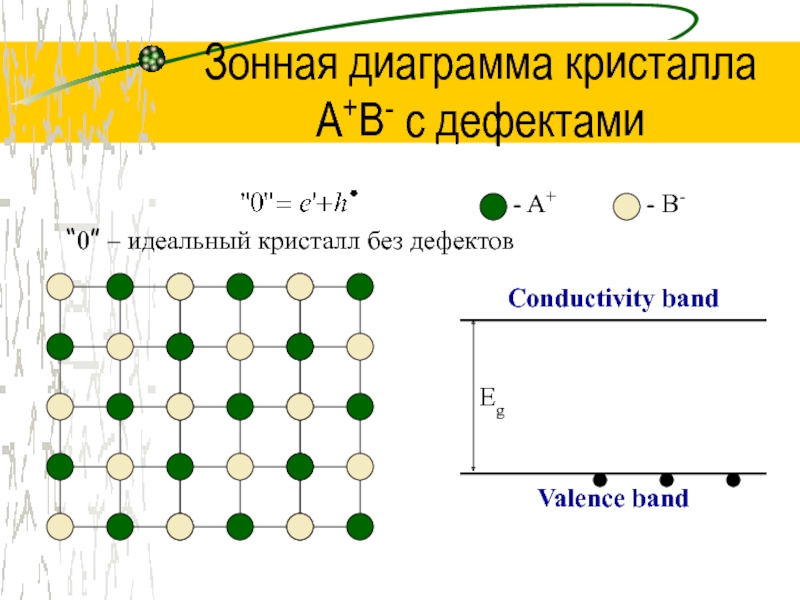
Слайд 41Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
“0” –
идеальный кристалл без дефектов
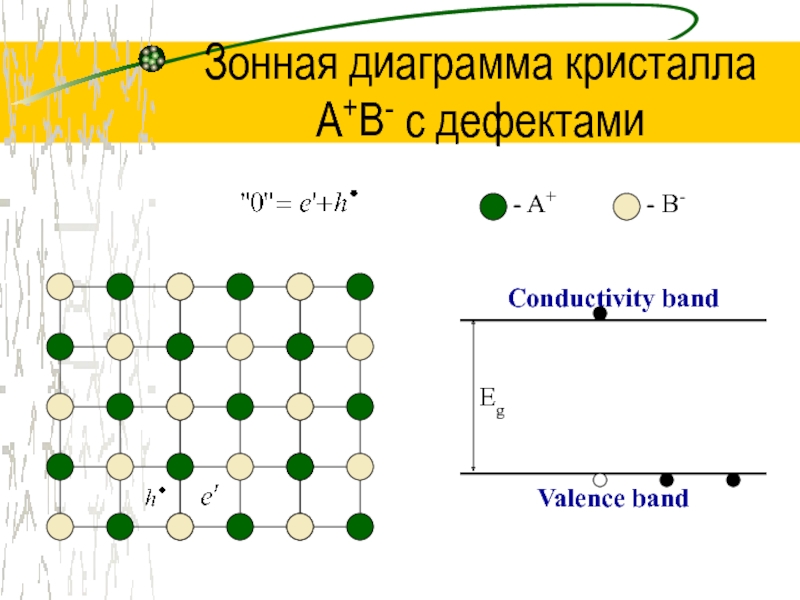
Слайд 42Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
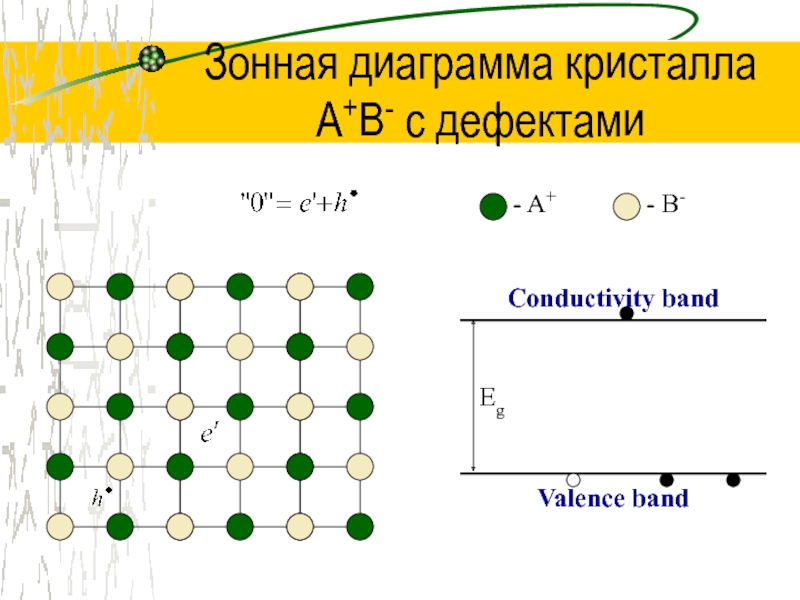
Слайд 43Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
Слайд 44Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
Слайд 45Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
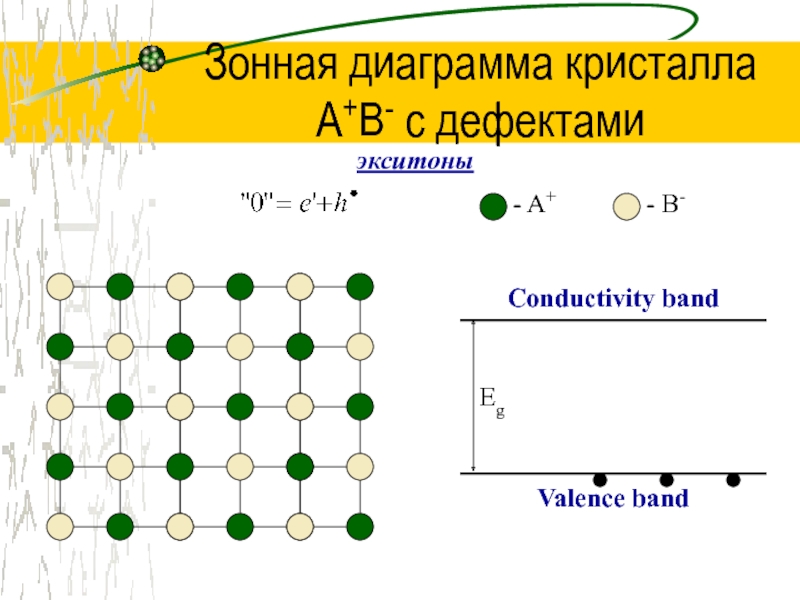
Слайд 46Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
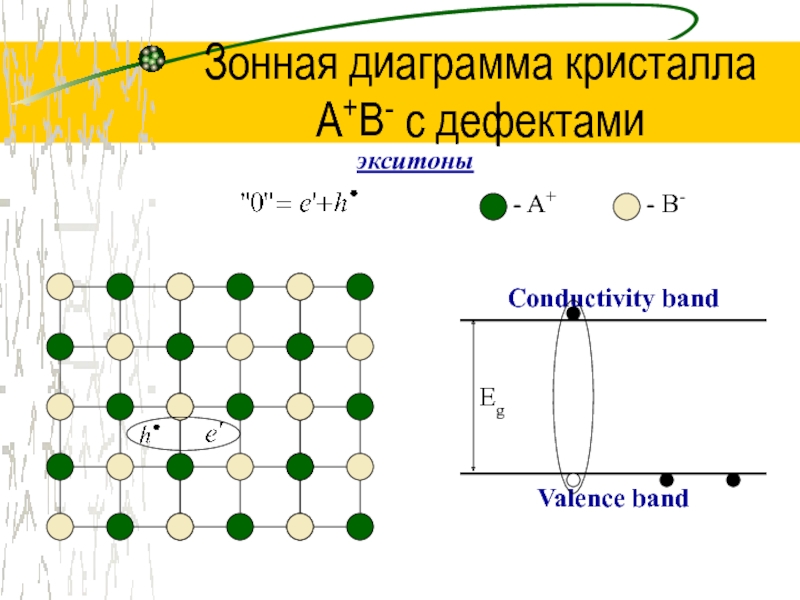
экситоны
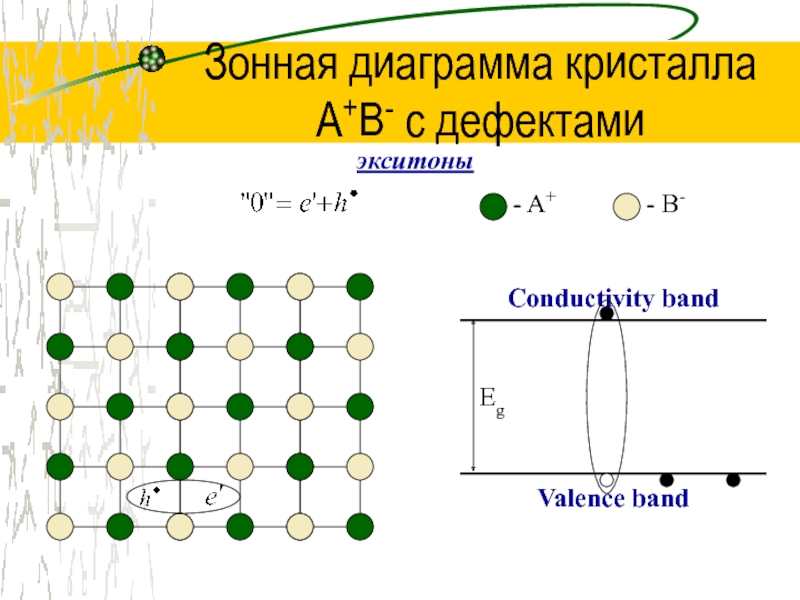
Слайд 47Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
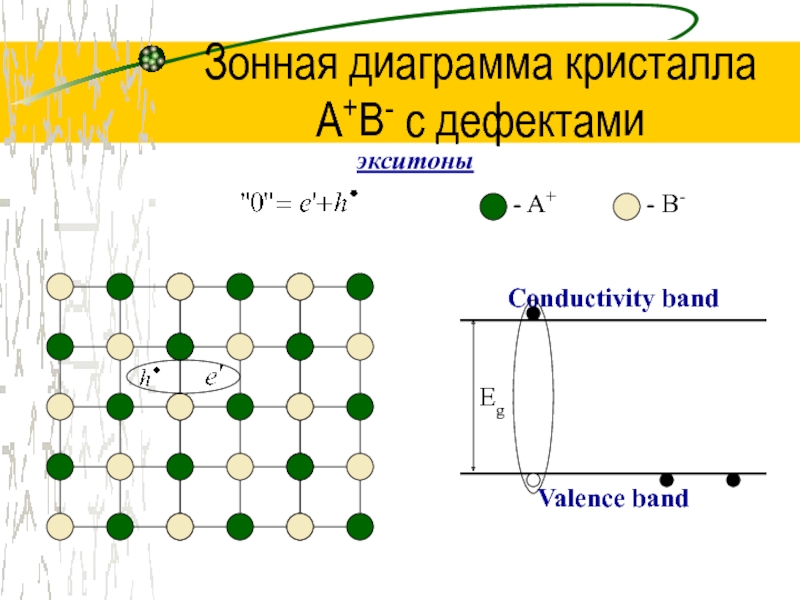
экситоны
Слайд 48Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
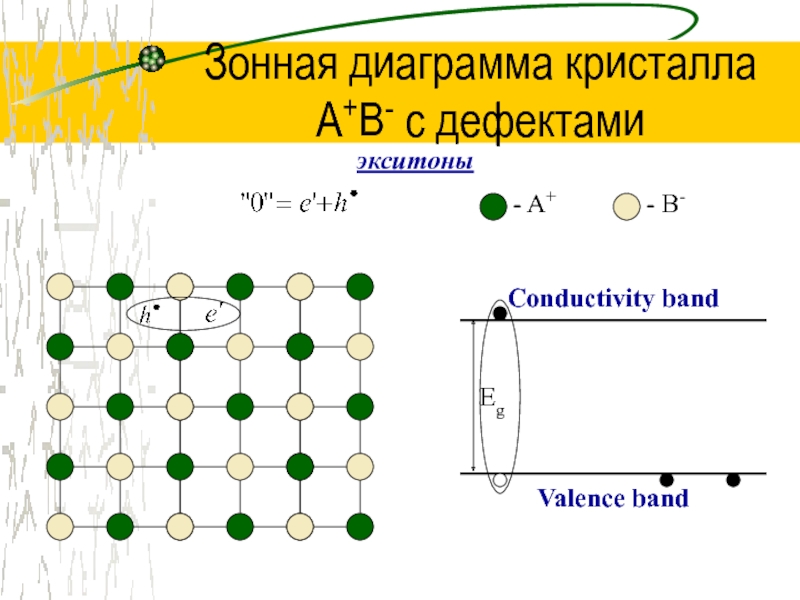
экситоны
Слайд 49Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
экситоны
Слайд 50Зонная диаграмма кристалла
A+B- с дефектами
- A+
- B-
Conductivity band
Valence band
Eg
экситоны
Слайд 51Равновесие дефектов в нестехиометрическом кристалле
Тепловое равновесие
Слайд 52Равновесие дефектов в нестехиометрическом кристалле
Тепловое разупорядочение
По Шоттки
По Френкелю
Слайд 53Равновесие дефектов в нестехиометрическом кристалле
Тепловое равновесие
Фазовые равновесия кристалла с сосуществующей
фазой («кристалл-пар», «кристалл-расплав»)
Слайд 54Равновесие дефектов в нестехиометрическом кристалле
Равновесие «кристалл – пар»
Слайд 55Равновесие дефектов в нестехиометрическом кристалле
Внутрикристаллические реакции дефектов
Тепловое равновесие
Фазовые равновесия кристалла
с сосуществующей фазой («кристалл-пар», «кристалл-расплав»)
Слайд 56Равновесие дефектов в нестехиометрическом кристалле
Внутрикристаллические реакции дефектов
(термическая ионизация)
Слайд 57Равновесие дефектов в нестехиометрическом кристалле
Тепловое равновесие
Фазовые равновесия кристалла с сосуществующей
фазой («кристалл-пар», «кристалл-расплав»)
Внутрикристаллические реакции дефектов
Равновесие электронного разупорядочения
Слайд 58Равновесие дефектов в нестехиометрическом кристалле
Равновесие электронного разупорядочения
Слайд 59Равновесие дефектов в нестехиометрическом кристалле
Условие электронейтральности кристалла
с разупорядоченностью
по
Шоттки
по Френкелю
Слайд 60Равновесие дефектов в нестехиометрическом кристалле
Разупорядоченность по Шоттки
Слайд 61Равновесие дефектов в нестехиометрическом кристалле
Полное условие электронейтральности
Разупорядоченность по Шоттки
Слайд 62Равновесие дефектов в нестехиометрическом кристалле
Слайд 63Равновесие дефектов в нестехиометрическом кристалле
Слайд 64Равновесие дефектов в нестехиометрическом кристалле
Слайд 65Диаграмма Броуэра
ln pA
ln [ ]
[VB]
[VA]
n
[VA’]
[VB•]
p
p
n
pA≈ pB
pA>>pB
pA


































![Атомистическая теория Диаграмма Броуэраln pAln [ ][VB][VA]n[VA’][VB•]ppnpA≈ pBpA>>pBpA Диаграмма Броуэраln pAln [ ][VB][VA]n[VA’][VB•]ppnpA≈ pBpA>>pBpA](/img/thumbs/a42291785d315e7f7d5fcb1c5c20d4a8-800x.jpg)