Слайд 1Фармацевтическая химия.
Предмет, классификация лекарственных веществ, стандартизация и сертификация лекарственных средств.
Слайд 2Фармацевтическая химия – это наука, которая изучает:
1 - способы получения
лекарственных веществ (ЛВ);
2 - физические и химические свойства ЛВ;
3 -
взаимосвязь строения ЛВ с действием на организм (фармакологическим действием);
4 - методы контроля качества лекарственных средств (ЛС):
а) - качественный анализ (идентификация или определение подлинности ЛВ),
б) - определение чистоты ЛС (определение примесей или доброкачественность ЛС),
в) - количественный анализ ЛС (определение количественного содержания ЛВ в ЛС и лекарственных формах (ЛФ) и препаратах (ЛП);
5 - условия хранения и изменения ЛВ при хранении.
В мире в настоящее время используется более 15000 лекарственных средств.
Слайд 3Классификация лекарственных веществ
1. Химическая – по характеру структуры ЛВ:
а) – ЛВ неорганической природы (соединения галогенов, кислорода, углерода, бора,
серы, азота, кальция, магния, серебра, меди и т.д.);
б) – ЛВ органической природы
- алифатические (алициклические) ЛВ (производные альдегидов, спиртов, карбоновых кислот и т.д.),
- ароматические ЛВ (производные фенолов, ароматических кислот, аминопроизводных и т.д.),
- гетероциклические ЛВ (производные фурана, пирана, тиазола, пиридина и т.д.).
2.Фармакологическая - по характеру действия ЛВ на организм (противомикробные, успокаивающие ЛС и т.д.).
Слайд 4Государственные законы и положения, регламентирующие качество ЛС в РФ
1. Закон «Основы законодательства в РФ об
охране здоровья граждан» от 22 июля 1993 года.
На основе этого закона разработан и утвержден в 1998 году
2. Федеральный закон «О лекарственных средствах», который включает в себя:
I - Основные положения о стандартизации в здравоохранении.
II – Основные положения сертификации ЛС в РФ.
Первая часть закона «О лекарственных средствах» «Основные положения стандартизации в здравоохранении» рассматривается в нескольких главах.
Слайд 51 глава. Содержит общие термины и понятия, используемые в здравоохранении.
1.1. В фармации широко используются следующие термины:
Лекарственное вещество – это
индивидуальное вещество (субстанция) синтетического, растительного, микробного или животного происхождения, оказывающее действие на организм.
Лекарственное средство – это индивидуальное вещество или комплекс веществ с определенным фармакологическим действием.
Лекарственная форма – это технологическая форма лекарственного средства или лекарственного вещества.
Лекарственный препарат – это дозированная технологическая форма лекарственного вещества или лекарственного средства.
Слайд 61.2. Глава содержит понятия о видах нормативной документации (НД).
В
фармации используют следующие виды нормативной документации:
- Государственная фармакопея РФ,
сейчас действует ГФ XII, ч.1 от 2007 года. ГФ XII, ч.1 включает ОФС на методы анализа ЛС и лекарственные формы, а также частные фармакопейные статьи (ФС) на ЛС. В работе используется также ГФ ХI, ч.1 и 2., которая содержит ОФС на методы анализа и лекарственные формы и ФС на растительное лекарственное сырье. Действует на всей территории РФ.
- Фармакопейная статья (ФС) - включает нормативы по контролю качества ЛВ, ЛС, ЛП и ЛФ. Действует на всей территории РФ.
Слайд 7 - Общая фармакопейная статья (ОФС) – включает нормативы на
лекарственные формы (например, таблетки, инъекционные растворы и т.д.), методы анализа
ЛВ, ЛС и ЛП (например, нитритометрия, спектрофотометрия в УФ области и т.д.). Действует на всей территории РФ.
- Фармакопейная статья предприятия (ФСП) – включает нормативы по контролю качества ЛВ, ЛС, ЛП и ЛФ, выпускаемых на конкретном предприятии. Действует на предприятии.
- ГОСТЫ – включают нормативы на сырье и др. материалы, используемые при производстве ЛВ, ЛС, ЛФ и ЛП.
Существуют также другие виды нормативной документации, используемой в фармации и здравоохранении.
1.3. В первой главе рассматриваются также термины сферы обращения ЛС (например, термин «предприятие», «фармацевтическая деятельность» и т.д.).
Слайд 82глава. Рассматривает государственное регулирование отношений в сфере обращения ЛС, т.е.
где и каким образом проводится разработка, получение и доставка ЛС
до потребителя.
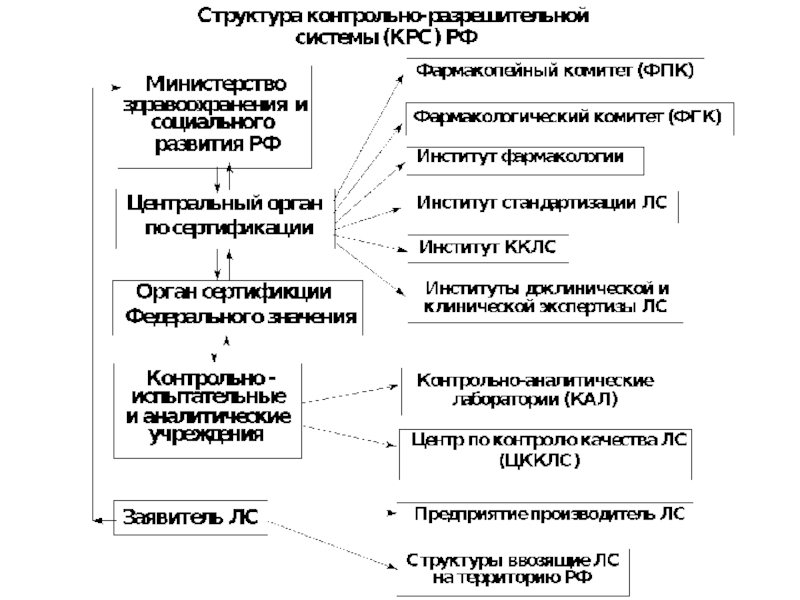
3глава. Рассматривает структуру и функции государственной системы контроля качества ЛС, которые включают различные научно-исследовательские институты (НИИ), лаборатории по контролю качества ЛС, экспертные советы и т.д. (см. структуру далее в «сертификации ЛС»).
4 глава. Рассматривает порядок производства ЛВ, ЛС, ЛФ и ЛП на предприятиях и в аптеках.
5 глава. Рассматривает порядок регистрации ЛВ, ЛС, ЛФ и ЛП в РФ.
Слайд 9Вторая часть закона «О лекарственных средствах» включает «Основные положения сертификации
ЛС в РФ».
Сертификация – это процесс установления и применения стандартов.
Стандарт
– это эталон или образец, принимаемый как исходный для сравнения с ним других аналогичных объектов. В фармации к стандартам относятся различные виды нормативной документации (НД) (например ГФ, ФС, ОФС и т.д., см. выше).
Контроль качества ЛВ, ЛФ, ЛС и ЛП производимых в РФ и ввозимых в страну (импортных) проводится в соответствии с приказом №734 от 30 октября 2006 г. Такие лекарственные средства называют «готовые ЛС».
Контроль качества ЛФ, изготавливаемых в аптеке осуществляется в соответствии с приказами №214 от 16 июля 1997 г. и №305 от 16 октября 1997 г. Такие лекарственные формы называются «эстемпоральные ЛФ), их готовят по заявке (требованию) лечебных учреждений и рецептам врачей.