Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Ивановский фармацевтический колледж Аналитическая химия
Содержание
- 1. Ивановский фармацевтический колледж Аналитическая химия
- 2. Аналитическая химияНаука о методах и средствах определения химического состава вещества путем проведения аналитического анализа
- 3. Качественный анализ –
- 4. Структура анализаПо природе анализируемого объекта органический и неорганический анализПо характеру решаемых задач качественный, количественный, структурный анализ
- 5. Методы анализаХимические: в основе метода
- 6. Методы анализаПо массе анализируемой пробы в гмакроанализ
- 7. Теоретические основы аналитической химииЭлектролитическая диссоциация – распад
- 8. Теоретические основы аналитической химииТипы химических реакций, применяемых
- 9. Реакции нейтрализацииВзаимодействие кислот и гидроксидов с образованием
- 10. Типы химических реакцийРеакции замещения:АС + Б =
- 11. Типы химических реакцийОбразование комплексных соединенийNaZn[(UO2)3(CH3COO)]9NaK2[Co(NO2)6]
- 12. Типы химических реакцийОкислительно-восстановительные реакции основаны на процессах
- 13. Окислительно-восстановительные реакцииУравниваются методами:ПолуреакцийЭлектронного балланса
- 14. Качественный анализС помощью аналитических реакций отвечает на
- 15. Качественный анализАналитические реакции должны:Сопровождаться аналитическим эффектомБыть чувствительными,
- 16. Способы выполнения аналитических реакций Пробирочный способ –
- 17. Методы выполнения аналитических реакцийРастираниеВыпариваниеНагреваниеОсаждениеФильтрованиеРастворение Возгонка Плавление
- 18. Методы качественного анализаСистематический качественный анализ: пробу разделяют
- 19. Аналитические реакции
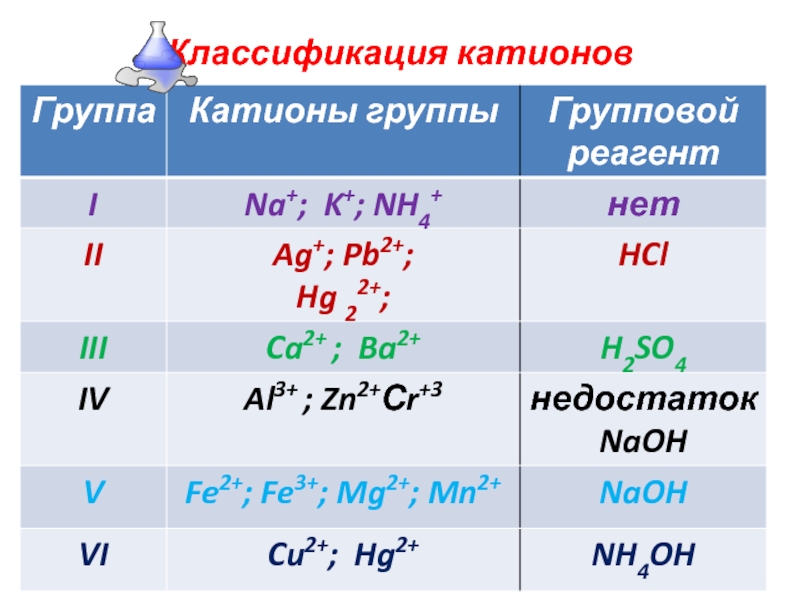
- 20. Классификация катионов
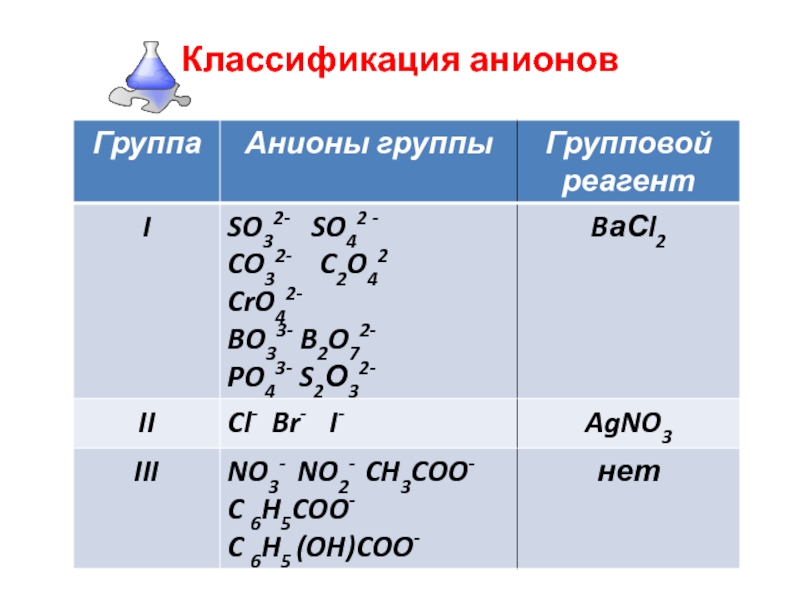
- 21. Классификация анионов
- 22. Скачать презентанцию
Аналитическая химияНаука о методах и средствах определения химического состава вещества путем проведения аналитического анализа
Слайды и текст этой презентации
Слайд 1
Ивановский фармацевтический колледж
Аналитическая химия
Введение в аналитическую химию
Введение в качественный анализ
Слайд 2Аналитическая химия
Наука о методах и средствах определения химического состава вещества
путем проведения аналитического анализа
Слайд 3 Качественный анализ – раздел аналитической химии
по обнаружению, идентификации и определению составных частей анализируемого вещества
Количественный анализ – определение количественного содержания составных частей анализируемого объекта или их количественных соотношенийПри проведении аналитического анализа необходимо строгое соблюдение инструкций по технике безопасности и охране труда, а также методик проведения исследований
Слайд 4Структура анализа
По природе анализируемого объекта органический и неорганический анализ
По характеру
решаемых задач качественный, количественный, структурный анализ
Слайд 5Методы анализа
Химические:
в основе метода лежат химические реакции
Физико-химические:
основаны на изменениях физических показателей в результате
химического воздействия на аналитический объектФизические:
основаны на изменениях физических показателей в результате физического воздействия на аналитический объект
Биологические:
основаны на изменениях биохимических реакций живых организмов
Слайд 6Методы анализа
По массе анализируемой пробы в г
макроанализ
1,0 – 10,0
полумикроанализ
0,05 – 0,5
Быстро выполняемый анализ называется экспресс-анализом
Слайд 7Теоретические основы аналитической химии
Электролитическая диссоциация – распад электролитов на ионы
Кислоты
диссоциируют на катионы водорода и анионы кислотного
остаткаГидроксиды
диссоциируют на катионы металла и анионы гидроксильных групп
Соли
диссоциируют на катионы металла и и анионы кислотного остатка
Слайд 8Теоретические основы аналитической химии
Типы химических реакций, применяемых в аналитической химии:
Реакции
нейтрализации
Реакции замещения
Реакции обмена
Реакции соединения
Реакции разложения
Реакции комплексообразования
Окислительно-восстановительные реакции
Слайд 9Реакции нейтрализации
Взаимодействие кислот и гидроксидов с образованием воды
рН – водородный
показатель, если
рН = 7, среда раствора нейтральная
если
рН > 7, среда раствора щелочнаяесли рН < 7, среда раствора кислая
Среда раствора влияет на цвет индикаторов
Слайд 10Типы химических реакций
Реакции замещения:
АС + Б = СБ + А
Реакции
обмена:
АВ + ДС = АС + ДВ
Реакции разложения:
АВ = А
+ ВРеакции соединения:
А + В = АВ
Слайд 11Типы химических реакций
Образование комплексных соединений
NaZn[(UO2)3(CH3COO)]9
NaK2[Co(NO2)6]
Слайд 12Типы химических реакций
Окислительно-восстановительные реакции основаны на процессах окисления и восстановления
Окисление
– процесс Отдачи электронов, химический объект является восстановителем
Восстановление – процесс
присоединения электронов, химический объект является окислителемСлайд 13Окислительно-восстановительные реакции
Уравниваются методами:
Полуреакций
Электронного балланса
Слайд 14Качественный анализ
С помощью аналитических реакций отвечает на вопросы:
Из каких ионов
состоит данный аналитический образец?
Из каких веществ состоит данный аналитический образец?
Слайд 15Качественный анализ
Аналитические реакции должны:
Сопровождаться аналитическим эффектом
Быть чувствительными, т.е. показывать аналитический
эффект при очень малых количествах определяемого вещества
Быть селективными, т.е. давать
аналитический эффект с группой ионовБыть необратимыми
Иметь достаточную скорость реакции
Слайд 16Способы выполнения аналитических реакций
Пробирочный способ – выполняется в пробирке
Капельный способ
– проводится на предметном стекле или фильтровальной бумаге
Микрокристаллоскопический способ –
проводится с применением микроскопаПирохимический способ – окрашивание пламени спиртовки (на грифеле, в выпарительной чашке)
Слайд 17Методы выполнения аналитических реакций
Растирание
Выпаривание
Нагревание
Осаждение
Фильтрование
Растворение
Возгонка
Плавление
Слайд 18Методы качественного анализа
Систематический качественный анализ: пробу разделяют на несколько «аналитических
групп», затем каждый ион открывают «своими реакциями». Реакции для разделения
пробы называют групповыми, реакции для отдельных ионов – характерными.Дробный качественный анализ: компоненты пробы устанавливают в отдельных пробах с помощью характерных реакций.









![Ивановский фармацевтический колледж Аналитическая химия Типы химических реакцийОбразование комплексных соединенийNaZn[(UO2)3(CH3COO)]9NaK2[Co(NO2)6] Типы химических реакцийОбразование комплексных соединенийNaZn[(UO2)3(CH3COO)]9NaK2[Co(NO2)6]](/img/thumbs/365677a722391f5e7dff858e0946e9c4-800x.jpg)