Разделы презентаций
- Разное
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Жиры
Содержание
- 1. Жиры
- 2. Слайд 2
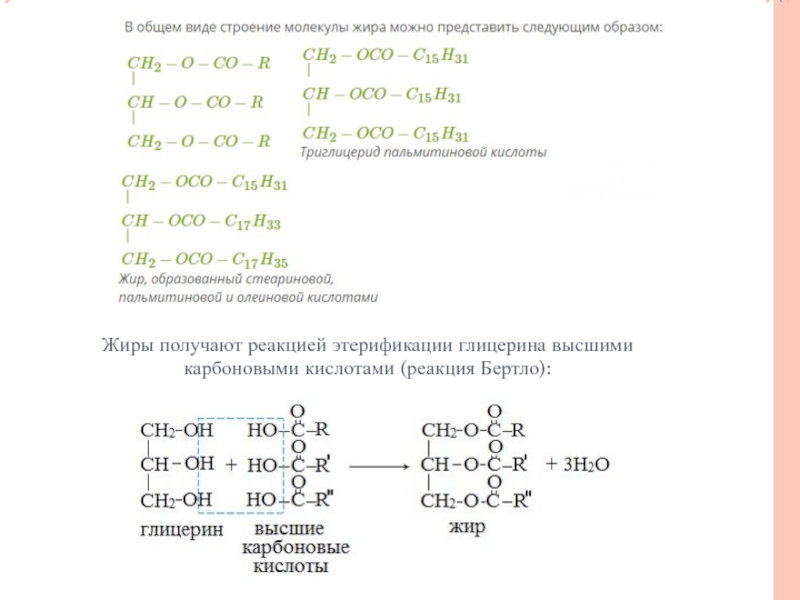
- 3. Жиры получают реакцией этерификации глицерина высшими карбоновыми кислотами (реакция Бертло):
- 4. Слайд 4
- 5. Слайд 5
- 6. Слайд 6
- 7. THANK U, NEXT
- 8. Углеводы
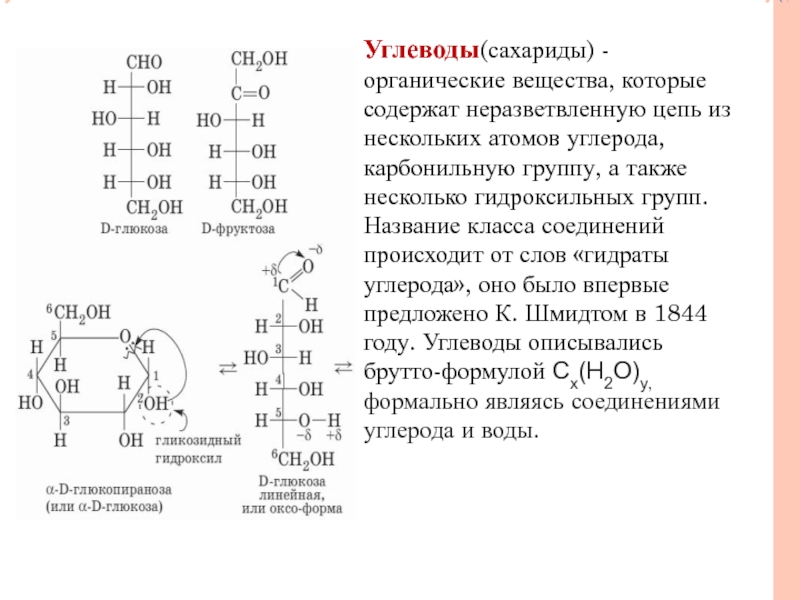
- 9. Углеводы(сахариды) - органические вещества, которые содержат неразветвленную
- 10. Гидролиз углеводов в организмеГидролиз – реакция обменного
- 11. По способности к гидролизу на мономеры углеводы
- 12. Биологическое значение углеводовУглеводы выполняют пластическую функцию, то
- 13. Белки, их строение и функции Цели. Расширить
- 14. В настоящее время различают первичную, вторичную и третичную
- 15. Вторичная структура белка – форма полипептидной цепи
- 16. Третичная структура белка – реальная трехмерная конфигурация
- 17. Четвертичная структура – соединенные друг с другом макромолекулы белков образуют комплекс
- 18. Химические свойства1. Денатурация – разрушение вторичной и третичной
- 19. Процентное содержание элементов в белках
- 20. Функции белков1. Каталитическая (ферментативная) . Все ферменты
- 21. 5. Сократительная и двигательная. Пример: актин и
- 22. Вывод: Все белки являются полипептидами, но не
- 23. Спасибо за внимание=)
- 24. Скачать презентанцию
Жиры получают реакцией этерификации глицерина высшими карбоновыми кислотами (реакция Бертло):
Слайды и текст этой презентации
Слайд 3Жиры получают реакцией этерификации глицерина высшими карбоновыми кислотами (реакция Бертло):
Слайд 9Углеводы(сахариды) - органические вещества, которые содержат неразветвленную цепь из нескольких
Слайд 10Гидролиз углеводов в организме
Гидролиз – реакция обменного разложения веществ водой.
Гидролиз происходит под воздействием ферментов.
Ферменты – это биокатализаторы, которые работают
как в клетке, так и за ее пределами и в этом они сходны с неорганическими катализаторамиСлайд 11По способности к гидролизу на мономеры углеводы делятся на две
группы: простые (моносахариды) и сложные (олигосахариды и полисахариды). Сложные углеводы,
в отличие от простых, способны гидролизоваться с образованием простых углеводов, мономеров. Простые углеводы легко растворяются в воде.Слайд 12Биологическое значение углеводов
Углеводы выполняют пластическую функцию, то есть участвуют в
построении костей, клеток, ферментов. Они составляют 2-3% от веса.
Углеводы являются
основным энергетическим материалом.Пентозы (рибоза и дезоксирибоза) участвуют в построении АТФ.
Углеводы выполняют защитную роль в растениях.
Слайд 13Белки, их строение и функции
Цели. Расширить знания о белках
как природных полимерах, о многообразии их функций во взаимосвязи со
строением и свойствами.Белки входят в состав всех живых организмов. Роль белков заключается в том, что они являются катализаторами химических реакций, протекающих в живых организмах.
Слайд 14В настоящее время различают первичную, вторичную и третичную структуру белковой молекулы:
Первичная
структура белка – последовательность соединения аминокислот в полипептидной цепи.
Слайд 15Вторичная структура белка – форма полипептидной цепи в пространстве, т.е.
способ скручивания цепи за счет образования водородных связей между амино-
и карбонильной группами.Слайд 16Третичная структура белка – реальная трехмерная конфигурация закрученной спирали в
пространстве. Определяющими факторами образования и удерживания третичной структуры белка являются
связи между боковыми радикалами аминокислотных остатков (дисульфидные мостики –S–S–).Слайд 18Химические свойства
1. Денатурация – разрушение вторичной и третичной структуры белка, происходящее
при нагревании или при взаимодействии с растворителями. Первичная структура при
денатурации сохраняется.2. Гидролиз белков в кислой или щелочной средах, приводящий к разрушению первичной структуры белка и образованию аминокислот.
3. Качественная реакция на белки – фиолетовое окрашивание при действии солей меди (II) в щелочном растворе (биуретовая реакция на пептидную связь).
При нагревании белков и пептидов с растворами кислот, щелочей или при действии ферментов протекает гидролиз. Гидролиз белков сводится к расщеплению полипептидных связей:
Слайд 20 Функции белков
1. Каталитическая (ферментативная) . Все ферменты - белки. Ни
одна реакция в организме не проходит самопроизвольно, каждая при участии
своего фермента.2. Транспортная. Пример: гемоглобин переносит кислород от легких к тканям и СО2 от тканей к легким. В клеточных мембранах есть белки, переносящие глюкозу, аминокислоты внутрь клетки.
3. Пищевая и запасная (резервная) . Пример: яичный альбумин - источник питания. Казеин молока и глиадин пшеницы - источник аминокислот.
4. Рецепторная. Пример: белки биомембран.
Слайд 215. Сократительная и двигательная. Пример: актин и миозин - белки
мышечной ткани.
6. Структурная. Пример: кератин волос, ногтей, коллаген (соединительная ткань)
, эластин (сосуды) , фосфолипопротеины (белки биологических мембран). 7. Защитная. Пример: антитела сыворотки крови - образуются в ответ на поступление в организм чужеродных веществ (антигенов).
8. Регуляторная. Пример: инсулин регулирует содержание глюкозы в крови.
9. Когенетическая. Совместно с нуклеиновыми кислотами участвуют в хранении и передаче наследственной информации.